INTRODUCCIÓN
Más del 80% de los aneurismas de aorta abdominal infrarrenales con indicación de tratamiento se excluyen actualmente mediante un abordaje endovascular. 1 Para tal fin se han desarrollado dos alternativas técnicas: la estándar y las técnicas complejas. La anatomía arterial, especialmente la que se corresponde con el segmento visceral de la aorta, es el factor decisivo. La reparación endovascular debe sellarse en una aorta sana para proporcionar una reparación duradera. Por tanto, cuando el aneurisma tiene un segmento sano para sellado infrarrenal, se utiliza un abordaje estándar, el cual se acompaña de una baja tasa de complicaciones. 2) (3
Por el contrario, el desarrollo de métodos endovasculares para pacientes con compromiso de la aorta visceral ha supuesto un cambio radical. El abordaje complejo, en que la zona de sellado compromete o está en contacto con el segmento de la aorta de donde emergen las arterias mesentéricas o renales, implica la utilización de dispositivos que permitan respetar el origen de esas arterias. Es especialmente en estos procedimientos en donde los resultados están específicamente relacionados con un algoritmo diagnóstico y terapéutico avanzado.
Presentamos nuestra experiencia con un enfoque técnico global (algoritmo terapéutico) en la reparación endovascular de los pacientes con aneurismas aórticos complejos.
MATERIAL Y MÉTODOS
Selección de Pacientes
Estudio observacional retrospectivo que evaluó resultados a 30 días y 3 años en pacientes con aneurismas complejos tratados por vía endovascular mediante: colocación de endoprótesis con fenestraciones (Fenestrated Endovascular Aneurysm Repair, FEVAR), endoprótesis con ramas (Branched Endovascular Aneurysm Repair, BEVAR), colocación de endoprótesis estándar reforzadas con EndoAnchors (EndoSuture Aneurysm Repair, ESAR), o endoprótesis estándar con stents en paralelo o chimeneas para preservar las arterias viscerales (Chimney Endovascular Aneurysm Repair, ChEVAR). La decisión de la técnica fue determinada con base fundamentalmente en la anatomía arterial. Fueron excluidos los pacientes en emergencia.
Definiciones y puntos finales
Aneurisma de aorta con anatomía compleja es un aneurisma de aorta abdominal yuxtarrenal, pararrenal, paravisceral o toracoabdominal (AATA), que, por instrucciones para uso de endoprótesis estándar, no es candidato para exclusión mediante la sola colocación de una endoprótesis bifurcada estándar infrarrenal (EVAR).
Para el diagnóstico y tratamiento de estos pacientes nos hemos basado en tres algoritmos fundamentales.
Algoritmo de imágenes
Se evaluó a los pacientes mediante angioTC con inyección de contraste por via endovenosa, excepto en aquellos con un clearence de creatinina menor que 30 ml/min, en los cuales se prefirió la vía intraarterial con catéter aórtico para disminuir la cantidad de contraste inyectado (menos de 60 ml para estudios toracoabdominales).
Durante la cirugía también se utilizaron distintas herramientas imagenológicas, para disminuir la cantidad de contraste y de radiación: fusión de imágenes (Vessel Navigator, Azurion/Allura Xper FD20, Philips Healthcare), tomografía intraoperatoria de haz cónico (Xpert-CT, Philips) y ecografía intravascular (IVUS Vulcano, Philips).
Los pacientes fueron evaluados con una angioTC antes del alta para verificar exclusión del aneurisma, integridad de los dispositivos y permeabilidad de los vasos colaterales de la aorta. Solo en aquellos con insuficiencia renal se realizó Doppler y tomografía sin contraste.
Para seguimiento, en ausencia de endoleak, los controles se realizaron mediante angioTC y Doppler a los 6 y 12 meses y luego anualmente. De haber endoleak, el seguimiento fue realizado según el tipo, característica del paciente y comportamiento del saco aneurismático.
Algoritmo terapéutico
FEVAR incluye una serie de dispositivos aórticos que pueden ser hechos a medida por un fabricante de tecnologías (Custom Made Devices, CMD, Cook Medical, Bloomington, Ind) o por un médico en el quirófano (Physician Modified Stent Graft, PMSG). Las fenestraciones son orificios en el material protésico del dispositivo que se corresponde con una rama aórtica visceral (tronco celíaco, mesentérica superior o arterias renales), permitiendo así que la prótesis se apoye más proximal de lo que permitiría una configuración estándar. Se hace entonces coincidir el orificio/fenestración de la endoprótesis con el origen de la arteria a respetar. Para sellar y específicamente anclar la fenestración, se colocan stents dentro de las mismas hacia la arteria respetada. El FEVAR fue indicado en pacientes con cuello infrarrenal corto, menor de 5 mm de longitud, y diámetro aórtico visceral menor de
36 mm. (Figura 1)

Fig.1. De izquierda a derecha. Imagen angiográfica donde se visualiza la endoprótesis fenestrada en posición, con introductores y guías colocadas en las arterias renales y mesentérica superior. Abajo izquierda: canulación de la arteria renal derecha. Medio: Endoprótesis fenestrada (FEVAR) con los stents desplegados en renales y mesentéricas. Abajo derecha: Angiografía final. Derecha: Fotografía de endoprótesis fenestrada hecha en el quirófano con una fenestración central para la arteria mesentérica superior
BEVAR. El injerto ramificado estándar (Zenith tBRANCH, Cook Medical, Dinamarca) consiste en una endoprótesis tubular con cuatro ramas en disposición caudal, con una ubicación en los ejes longitudinal y axial estándar, basado en archivos de tomografías de pacientes con aneurismas toracoabdominales. Se requiere también de un stent adicional, puente, para conectar y sellar la rama de la endoprótesis con el vaso visceral. Se indicó en pacientes con aneurismas toracoabdominales tipo IV (Figura 2).
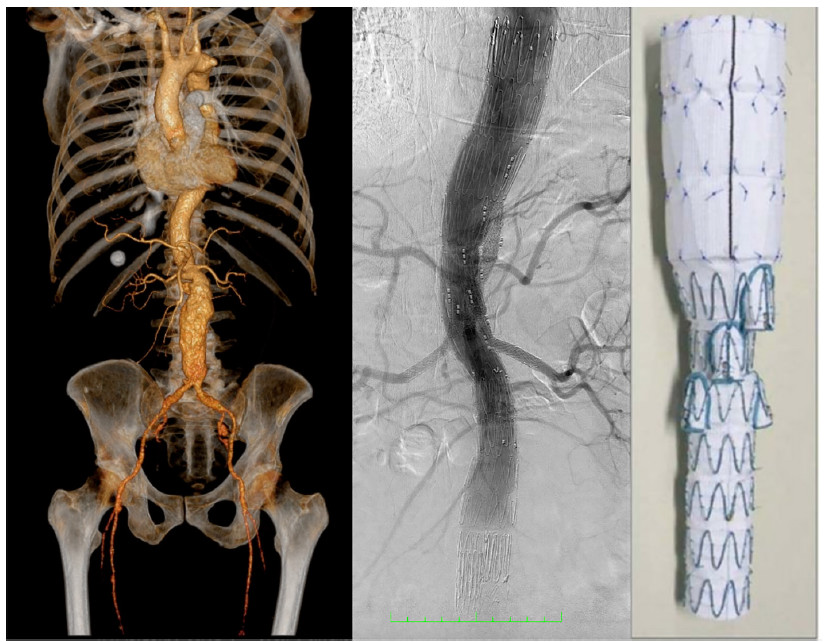
Fig. 2 Izquierda: Angiotomografía de un paciente con aneurisma yuxtavisceral. Centro: Angiografía final con la endoprótesis ramificada hacia tronco celíaco, mesentérica superior y ambas renales. Derecha: Fotografía de la endoprótesis ramificada
ESAR. Los EndoAnchors (Heli-FX™ EndoAnchor™ system, Medtronic Inc, Minneapolis, USA). son endosuturas que refuerzan el contacto entre la endoprótesis y la pared arterial a nivel del cuello. El procedimiento implica atornillar pequeñas grapas helicoidales por vía endovascular, simulando la fuerza de una anastomosis quirúrgica suturada a mano. Se utilizó este abordaje en pacientes con posibilidad de una aposición (contacto) correcta entre la endoprótesis y la aorta infrarrenal de al menos 10 mm, pero con un cuello de más de 30mm de diámetro, cuellos cónicos, en forma de gota o reloj de arena, todas características tomográficas que se asocian a un riesgo aumentado de dilatación del cuello proximal a mediano plazo. También, en pacientes previamente intervenidos, con crecimiento del saco aneurismático por endoleak tipo II y dilatación del cuello de más de 10% o más de 32 mm de diámetro.
ChEVAR. Los stents en chimeneas aseguran el flujo de entrada a través de un stent cubierto colocado en la rama visceral de forma paralela a la endoprótesis. Se indicó en pacientes con cuello corto, de 5 a 10mm pero menor de 28 mm de diámetro, especialmente en pacientes de riesgo alto no solo de ruptura del aneurisma (dolor o mayor de 70 mm) sino también de alto riesgo quirúrgico (ASA IV).
Análisis estadístico
Los datos continuos se presentan como media y desviación estándar (DE). Los datos categóricos como porcentajes. Los datos continuos se compararon test de t o Wilcoxon según su distribución. Se emplearon test para datos apareados al comparar las dimensiones antes y después de la intervención. Los datos categóricos con test de chi cuadrado o test exacto de Fisher según correspondiera. Se definió la supervivencia libre de eventos mediante análisis de supervivencia, con la confección de curvas de Kaplan Meier. El análisis estadístico se realizó con el software SPSS 25.0 para Windows. (SPSS, Inc., Chicago, IL).
RESULTADOS
Se evaluaron en forma consecutiva los últimos 50 pacientes sometidos a procedimientos endovasculares por patología aórtica compleja, de los cuales 44 fueron hombres (88%) y 3 (6%) estaban complicados al momento de la presentación (sintomáticos o rotos y contenidos). La edad promedio fue de 71,3 ± 11,6 años, mientras que el diámetro aneurismático promedio fue de 69,6 ± 16,6 mm (FEVAR 68,5 mm, BEVAR 66,4 mm, ESAR 72.3 mm, ChEVAR 79,8 mm. p = 0,418). Doce pacientes (24%) presentaban un EVAR previo. En este subgrupo, la indicación de tratamiento se dio por endoleak IA (n = 4, 33,3%), migración (n=2, 16,7%) y dilatación del cuello proximal (n = 6, 50%).
Los procedimientos realizados incluyeron: 22 FEVAR (17 PMSG y 5 CMD), 11 BEVAR, 6 ChEVAR y 11 ESAR.
La tasa de éxito técnico fue del 100% sin presencia de endoleak I o III, con permeabilidad adecuada de las ramas. Tres pacientes fallecieron durante los primeros 30 días del perioperatorio, uno en el postoperatorio inmediato por ateroembolia mesentérica (BEVAR), un segundo paciente en el día 22 por neumonía (paciente con aneurisma roto y contenido) y otro por una taquicardia ventricular al día 8, estos dos secundarios a un ChEVAR.
Complicaciones durante el seguimiento
Durante un promedio de seguimiento de 17 meses (rango de 1 a 48), cuatro pacientes presentaron un endoleak tipo IA, tres de los cuales recibieron un FEVAR (todos con un ESAR secundario previo, tratados durante el seguimiento por dilatación del cuello proximal), y un cuarto, con un ChEVAR previo, que fue corregido mediante embolización del “gutter” y colocación de EndoAnchors.
En cinco pacientes se presentó una oclusión de la arteria renal (3 BEVAR y 2 PMSG). Tres fueron corregidas. Un cuarto paciente de alto riesgo permaneció asintomático sin tratamiento y el quinto presentó una oclusión de la arteria renal en un riñón ya atrófico, por lo que tampoco recibió tratamiento.
En el análisis de supervivencia, la supervivencia global fue del 88,6% al año y 77,3% a los 3 años, libre de reoperación del 86,5% al año y 61,3% a los tres años, mientras que la permeabilidad primaria del vaso fue del 91,3% al año y 79,9% a los tres años.
Comportamiento del saco aneurismático
En el global el saco aneurismático sufrió un achicamiento no significativo de 68,3 mm ± 15,6 mm a 66,9 mm ±17,6 mm (p = 0,69). Sin embargo, sabiendo el pequeño número de pacientes de la serie, se desglosó la información tomográfica por procedimiento. Los pacientes con BEVAR desarrollaron un achicamiento del saco de 64,9 mm± 8,12 mm a 59 mm± 8,2 mm (p = 0,14) y los FEVAR de 60,17 mm ± 11,1 mm a 54,17 mm ± 9.9 mm (p = 0,31). Específicamente los aumentos del saco aneurismático se desarrollaron en los pacientes con endoleak tipo IA que fueron reparados y tres pacientes con endoleak II actualmente en observación.
DISCUSIÓN
Esta serie muestra la experiencia de un centro especializado en el tratamiento de pacientes con aneurismas de aorta. Apoyado en una selección basada en criterios anatómicos y clínico-quirúrgicos, se trata de la primera publicación en nuestro medio que muestra un enfoque global del paciente con un aneurisma de aorta complejo. La aplicación de un protocolo bien establecido permitió tratar a este grupo de pacientes, con alto riesgo quirúrgico, incluso durante la pandemia, con una tasa de morbilidad y mortalidad perioperatorias similar a los estándares internacionales.
Se calcula que el 50% de los pacientes con aneurismas de aorta abdominal no son candidatos a reparación endovascular con los dispositivos disponibles actualmente en el mercado debido a su anatomía desfavorable. 4 Esto incluye a los pacientes con cuellos cortos o angulados, extensión aneurismática a la arteria ilíaca interna o afectación aneurismática de la aorta yuxtarrenal, paravisceral y toracoabdominal (aorta compleja). Los buenos candidatos quirúrgicos pueden tolerar una cirugía abierta convencional. 5) (6 Sin embargo, en una reciente presentación en el Charing Cross International Symposium en Londres el 27 de abril de 2023, el equipo quirúrgico de la Universidad de Brescia, después de equiparar covariables, sobre 204 pacientes con aneurismas toracoabdominales, determinó que la mortalidad a 30 días de la cirugía abierta fue del 13% versus 5% para el tratamiento endovascular complejo, paraplejía 10% versus 3%, complicaciones respiratorias graves del 18% versus 7%, cardíacas del 42% versus 26% y renales graves de 27% versus 6% para el tratamiento endovascular. Esto muestra un mundo real con estadísticas actuales, tecnología avanzada y en un grupo quirúrgico con experiencia en ambos abordajes.
Las técnicas aórticas endovasculares complejas se diseñaron para ampliar la zona de sellado proximal desde el segmento infrarrenal hasta la aorta yuxta o suprarrenal, sorteando así la limitación que supone la ausencia o escasa longitud del segmento aórtico infrarrenal. La primera opción para estos pacientes ha sido y sigue siendo, desde nuestros inicios en 2011, la colocación de una endoprótesis fenestrada (FEVAR). Desde entonces, la evolución significó una mejor selección de los pacientes, cambios innovadores en el diseño de las endoprótesis, un importante desarrollo en tecnología de imágenes y la aplicación de protocolos estandarizados para los cuidados perioperatorios. Es claro que la atención de estos pacientes no empieza ni termina en el quirófano, y de ahí la importancia de un cuidado multidisciplinario, del cual depende el éxito global del procedimiento.
Las endoprótesis fenestradas, específicamente tienen la necesidad de ser armadas a medida. La anatomía arterial es única para cada paciente, y si se necesita un contacto preciso entre el orificio de la prótesis y el origen de la arteria a respetar. Dicha información es obtenida de la tomografía y debe volcarse a un plano para la construcción de la endoprótesis. La producción industrial de estos dispositivos (Cook Medical en nuestro caso) implica una cierta demora en su disponibilidad (tiempo de autorización, producción, traslado) que puede ser demasiado largo para pacientes con necesidades urgentes (aneurismas de más de 7cm, sintomáticos o rotos). La forma de responder frente a este problema fue entrenarse en la fabricación de endoprótesis, pero fenestradas en quirófano, lo que otorga la enorme ventaja de la disponibilidad casi inmediata de una endoprótesis a medida. 7 Para tal fin, dos miembros del equipo fueron entrenados en la Clínica Mayo (Rochester, Minnesota). Esto nos permitió diseñar dichas endoprótesis con variables como cantidad, ubicación y tamaño de las fenestraciones o diseñarlas para ser canuladas desde un abordaje femoral o subclavio. Así, podemos acceder desde craneal a vasos con orientación caudal, y también evitar colocar un introductor voluminoso en una arteria femoral, lo cual podría genera isquemia de extremidades. 8 Sin embargo, la evidencia publicada y nuestra propia experiencia determinan que este tipo de endoprótesis modificadas en el quirófano debe ser indicada en casos excepcionales. El estudio presentado por el Dr. Oderich, de la Clínica Mayo determinó que la táctica actual evolucionó de los dispositivos construidos en el quirófano a casi exclusivamente los manufacturados por la industria (CMD) Los CMD se realizaron con mayor éxito técnico, sin mortalidad y con menos eventos adversos serios. 9 En nuestra serie, ninguno de los pacientes que recibió un CMD desarrolló complicaciones.
También es importante recalcar el estricto seguimiento que se necesita de estos pacientes. Como se muestra en la sección de resultados, este abordaje se acompaña de una tasa no menor de reoperaciones: casi un 10% de pacientes recibieron un segundo procedimiento por inestabilidad de rama (oclusión o endoleak). Pero, la mayoría fueron cirugías menores y no afectaron la supervivencia. 10) (11) (12) (13
También, una meta del servicio fue intentar disminuir la necesidad del FEVAR en un específico grupo de pacientes. En aquellos pacientes con cuellos proximales por fuera de las instrucciones para uso, pero que el análisis tomográfico nos permitía predecir que teníamos una zona de contacto de 10mm, preferimos no utilizar el FEVAR como primera opción. 14 La experiencia obtenida con los EndoAnchors nos permitió un sellado adecuado, sin mortalidad ni endoleak IA a mediano plazo, cuando los EndoAnchors fueron implantados en el procedimiento primario. Al igual que en el registro ANCHOR estos resultados siguen siendo prometedores. 15 En cambio, cuando ya fueron colocados frente a dilatación del cuello proximal, en algunos casos, la consecuente dilatación terminó en un endoleak proximal, que tuvo que ser reparado mediante FEVAR.
El ChEVAR fue relegado a una estricta indicación anatómica y clínica. Conocemos la mayor incidencia de endoleak IA asociada a esta técnica, y es por esto por lo que somos muy selectivos para su uso. 16
Por último, la realización de BEVAR no fue en el contexto de cuellos dilatados sino francamente aneurismáticos, aneurismas yuxta/pararrenales, donde la aorta visceral dilatada significaba más de 5mm de distancia entre la endoprótesis y el origen de la arteria visceral. 17
La isquemia medular es una complicación devastadora, y es conocida la asociación entre su incidencia y mortalidad. 18 En 2019, publicamos nuestro protocolo para su prevención, analizando 29 pacientes. 19 Desde entonces, no hemos tenido casos de paraplejía temprana ni tardía.
Aunque las actuales guías internacionales no se traducen directamente en recomendaciones para el tratamiento complejo, es lógico y razonable suponer que los beneficios de un enfoque endovascular serán aún mayores al aplicarlo en pacientes con aneurismas yuxta, pararrenales o toracoabdominales. 20) (21 Es bien sabido que, debido a su edad y comorbilidades, especialmente estos pacientes tienen una esperanza de vida limitada más allá de la cirugía. Podría argumentarse, entonces, que la calidad de vida es una métrica mejor que la supervivencia para evaluar los resultados.
Limitaciones
Como limitaciones, se trata de un seguimiento a mediano plazo y en el contexto de una pandemia, lo cual dificultó relativamente el seguimiento de los pacientes. También es de resaltar la cantidad de pacientes analizada (50 pacientes) que, pudiendo ser un valor representativo para nuestro país, no nos permite llegar a recomendaciones robustas, sino al hecho de demostrar las posibles ventajas de la centralización de patologías por experiencia y tecnología aplicada.
CONCLUSIONES
En conclusión, esta presentación muestra un enfoque global en el cual distintas técnicas no se contraponen, sino que se complementan para lograr un tratamiento efectivo y duradero a mediano plazo en pacientes con aneurismas de aorta complejos. El objetivo no es comparar las técnicas, ya que tienen indicaciones distintas, sino buscar un resultado final, que es el tratamiento miniinvasivo de pacientes con una gran complejidad técnica.















