INTRODUCCIÓN
La afectación cardiovascular en pacientes con tirotoxicosis es caracterizada por la presentación de arritmias, fenómenos embólicos, eventos coronarios e insuficiencia cardiaca®. Alrededor del 6 % de los pacientes presentan insuficiencia cardiaca® y un porcentaje menor al 1 %, cardiomiopatía dilatada que es secundaria a hipertiroidismo<3). En la enfermedad de Graves, cada vez hay mayor evidencia de que un sustrato autoinmune induce el desarrollo de miocarditis, como principal causa de cardiomiopatía, sumado al estado de alto gasto cardiaco característico de dicha enfermedad®. Se describe el caso de una paciente con miocarditis autoinmune inducida por hipertiroidismo secundario a enfermedad de Graves.
CASO CLÍNICO
Se presenta a una paciente de 28 años con un cuadro clínico de un mes de evolución de dolor abdominal difuso de predominio en hipocondrio derecho, asociado a deposiciones diarreicas y disnea de esfuerzo progresiva. No refiere historia previa de hipertensión arterial, diabetes mellitus o enfermedad cardiopulmonar. Un mes antes del comienzo de los síntomas, le realizaron cesárea por embarazo gemelar, presentando diagnóstico de hipertiroidismo durante el segundo trimestre de la gestación, tratada con metimazol a dosis de 5 mg/día hasta finalizar el embarazo. Al examen físico de ingreso, se encontraba afebril, con frecuencia respiratoria de 28 respiraciones por minuto, tensión arterial de 100/60 mmHg y una frecuencia cardiaca regular, de 120 latidos por minuto. Presentaba orbitopatía leve, no activa. A nivel del cuello, se describió un bocio grado 2, que se define como aquel que es visible cuando el cuello está en posición normal y cuando se palpa es consistente con una tiroides agrandada (Clasificación OMS)<5. El abdomen se evidenciaba distendido con hepatomegalia 2 cm por debajo de reborde costal derecho.
El laboratorio inicial evidenció TSH <0,015 uUI/ml (0,465 4,66), T4 libre 4,62 ng/dl (0,78-2,19), anticuerpos (Ac) anti- TPO 1265 Ul/ml (<15), Ac anti-receptor TSH 5,57 UI/L (<1,5) y Ac anti-tiroglobulina negativo, conteo leucocitario, hemoglobina, plaquetas, función renal y electrolitos normales. Las transaminasas se encontraban levemente elevadas (TGP 95 U/L y TGO 81 U/L), por lo que, se realizó ecografía abdominal evidenciando hepatomegalia con ecogenicidad normal. En el ecocardiograma transtorácico presentaba ventrículo izquierdo levemente dilatado con hipoquinesia global y fracción de eyección del ventrículo izquierdo (FEVI) del 17 %. La ecografía de tiroides describía un bocio difuso sin lesiones focales (Foto 1). Se le realizó gammagrafía de tiroides con 5 mCi Tc99 con hallazgo de un bocio difuso con índice de atrapamiento de 38 (VN 2,5-4,5) consistente con enfermedad de Graves. Por lo cual, la impresión diagnóstica fue cardiomiopatía asociada a enfermedad de Graves.
Se inició tratamiento específico de la insuficiencia cardiaca con fracción de eyección reducida (inhibidor de enzima convertidora de angiotensina, betabloqueador y antagonista mineralocorticoide), además de metimazol como antitiroideo de elección. A las dos semanas de iniciado el tratamiento, en el control ecocardiográfico había mejorado su FEVI a 27 %. Se decidió optimizar el tratamiento para insuficiencia cardiaca adicionando inhibidor de receptor de angiotensina e inhibidor de la enzima neprilisina (valsartán/sacubitrilo). Posteriormente, se realizó resonancia magnética cardiaca con hallazgos compatibles con miocarditis aguda como causa de la miocardiopatía (Fotos 2 y 3). No se identificaron síntomas previos que sugirieran infecciones virales. Debido a los nuevos hallazgos y en el contexto de la paciente, se arribó al diagnóstico final de miocarditis autoinmune inducida por hipertiroidismo.
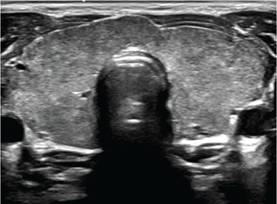
Foto 1: Ecografía de tiroides. Se reconoce la glándula tiroides en su posición anatómica usual. La misma se observa aumentada de tamaño en forma difusa con marcada heterogeneidad de su parénquima sin definir francas lesiones focales sólidas o quísticas ni calcificaciones.

Foto 2: Resonancia magnética cardiaca. Hallazgo de patrón de realce tardío con gadolinio subepicárdico y edema miocárdico transmural. Hallazgos compatibles con miocarditis aguda como etiología de la miocardiopatía.
Se manejó con esquema de esteroides a dosis altas consistente en metilprednisolona 500 mg/día por vía endovenosa durante tres días y continuando con prednisolona a 0,5 mg/kg/día por vía oral, con un plan de descenso en seis semanas. A las 4 semanas del tratamiento, se realizó un nuevo ecocardiograma con mejoría de la FEVI a 42 %, encontrándose clínica y bioquímicamente eutiroidea. Dada la respuesta clínica favorable, se continuó su tratamiento de forma ambulatoria. Cuatro meses después, en un nuevo ecocardiograma se registró una FEVI de 55 % y la paciente se encontraba clínicamente asintomática.
DISCUSIÓN
En el hipertiroidismo es conocida la afectación cardiaca, con un aumento en la morbilidad y mortalidad cardiovascular. El riesgo de insuficiencia cardiaca es elevado en pacientes mayores de sesenta años, siendo rara la afectación en pacientes jóvenes con hipertiroidismo de corta evolución. Sólo una pequeña proporción de los casos de insuficiencia cardiaca presentan disfunción sistólica®. Dicho compromiso, no se correlaciona con un nivel sérico específico de hormonas tiroideas, lo que supone un mecanismo fisiopatológico alterno®. Durante el puerperio es conocido el aumento en los títulos de anticuerpos antitiroideos, lo que puede empeorar la presentación clínica inicial®. En una serie de 11 pacientes llevados a biopsia endomiocárdica, en ausencia de etiología viral, sólo en el 18 % se ha identificado infiltrado inflamatorio linfocitario sugestivo de miocarditis autoinmune<8). Luego de la introducción de la resonancia magnética cardiaca, como único método diagnóstico no invasivo para la identificación de miocarditis®, se ha correlacionado la presencia de hallazgos sugestivos de miocarditis con un infiltrado linfocitario significativo en 3 de 5 pacientes llevados a biopsia endomiocárdica<4). El proceso fisiopatológico subyacente aún es desconocido. Distintos estudios han identificado mRNA de receptor de TSH en cardiomiocitos, lo que sugiere un proceso autoinmune compartido con la orbitopatía, pero este hallazgo no ha sido consistente00-®. En el tratamiento de la tormenta tiroidea se indican glucocorticoides con el propósito de reducir la conversión periférica de T4 a T3<13), entre otros efectos. Mientras que, en el contexto de pacientes con cardiomiopatía dilatada y considerando el sustrato autoinmune subyacente, se propone el uso de glucocorticoides como terapia inmunosupresora<14-15). La mayoría de los pacientes logran recuperar la función sistólica con el uso de terapia específica (metimazol, tratamiento cardiológico y en algunos casos terapia inmunosupresora)<6). A la fecha no se han identificado características clínicas que permitan predecir la ocurrencia de una cardiomiopatía persistente®. El diagnóstico diferencial incluyó la cardiomiopatía periparto, una patología sin hallazgos específicos por resonancia magnética cardiaca y en la que se ha descrito la presencia de realce tardío luego del gadolinio como marcador de mal pronóstico<16). La respuesta adecuada a la terapia antitiroidea e inmunosupresora, una vez que se confirmó
la presencia de miocarditis por resonancia magnética cardiaca, permitió excluir la cardiomiopatía periparto<17).
CONCLUSIÓN
En este caso clínico el aumento de la autoinmunidad en el puerperio y la presencia de orbitopatía podrían avalar la sospecha diagnóstica de cardiomiopatía de origen autoinmune según fuera descripto previamente. Cabe destacar la adecuada respuesta a las terapias antitiroidea e inmunosupresora, una vez que se tuvo evidencia de miocarditis por resonancia magnética. La intervención oportuna puede impactar favorablemente en la recuperación de la función cardiaca. Finalmente, resaltamos la importancia de la sospecha temprana dado la baja frecuencia de este tipo de presentación y el acceso a herramientas diagnósticas no invasivas como la resonancia magnética cardiaca en forma precoz.
Declaración de Conflictos de Intereses:
Los autores declaran no tener conflictos de interés.
Consideraciones éticas: Los autores declaran que no se realizó algún estudio experimental ni aparecen datos personales con los cuales pueda ser identificado el paciente.
Apoyo financiero: Recursos propios de los autores.














