Introducción
El colangiocarcinoma (CC) es una neoplasia maligna primaria del epitelio de las vías biliares. Su incidencia ha sido reportada menor al 2% de todas las neoplasias malignas en el cuerpo, considerándose un tumor raro, y el segundo tumor maligno del hígado más frecuente después del carcinoma hepatocelular (HCC).1,2
Se manifiesta generalmente con ictericia, dolor, anorexia, pérdida de peso y fatiga, entre la sexta y séptima décadas de la vida, siendo ligeramente más frecuente en el género masculino que en el femenino, con una proporción de 1.3/1. Su prevalencia varía de una región a otra, siendo mayor en el Noreste Asiático y menor en Australia.1,2
Etiología
La mayoría de los CC no tienen una etiología conocida o un factor de riesgo asociado a su presentación. Sin embargo, se han reportado múltiples factores de riesgo que pueden predisponer su desarrollo, principalmente en pacientes jóvenes. La inflamación crónica del ducto biliar es el principal factor de riesgo.1
Los pacientes con diagnóstico de colangitis esclerosante primaria tienen entre un 10 y un 20% más de riesgo de desarrollar la neoplasia y, de ser así, generalmente sucede dentro de los dos años posteriores al diagnóstico de colangitis.1
Otros factores de riesgo, como las anomalías congénitas del ducto biliar, han sido descritos, especialmente la enfermedad de Caroli y los quistes del colédoco. Esos últimos, a partir de la segunda década de la vida, tienen un incremento del riesgo a desarrollar CC (10-15%).1
Se han descrito otros factores, como la litiasis hepática, la papilomatosis biliar, las infecciones por parásitos como el Clonorchis sinensis y el Opistorchis viverrini, la exposición a tóxicos como el dióxido de Torio, así como también la cirrosis hepática por hepatitis B y C, la esteatosis hepática y el síndrome metabólico.1
Histopatogenia
La mayoría de los CC son del tipo histológico adenocarcinoma ductal, aunque puede también encontrarse del tipo papilar, mucinoso, mucoepidermoide y del tipo cistoadenocarcinoma.3,4
Dentro de esos el 90% al 95% de los adenocarcinomas son de pobre a moderada diferenciación, con estroma desmoplásico y alta expresión de mucina.3
Diagnóstico
La presentación clínica del CC es inespecífica. Los pacientes, en su mayoría, se vuelven sintomáticos en estadios avanzados de la enfermedad, por ello es importante una alta sospecha clínica, acompañada de una adecuada interpretación combinada de las diferentes modalidades diagnósticas dentro de las que se encuentran las imágenes proporcionadas por tomografía computada (TC) y la resonancia magnética (RM).3
Todo en conjunto juega un rol sumamente importante para tener un diagnóstico concordante, realizar la estadificación y evaluar la resecabilidad para poder escoger la terapia adecuada en cada caso, sin dejar de lado que en algunas ocasiones el diagnóstico se realiza por un hallazgo incidental imagenológico.
Clasificación
El CC puede originarse desde cualquier porción del epitelio del ducto, es decir desde los ductos terminales hasta la ampolla de Vater, así como también de las glándulas perihiliares.3,4,5,6
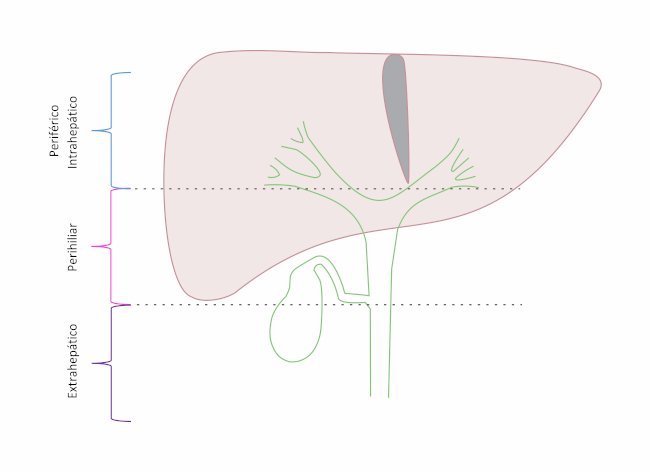
Clásicamente, los CC se clasifican, según su localización anatómica (Fig. 1) en: periférico intrahepático (CCi), perihiliares (CCp) y extrahepático (CCe). Los CCi se originan periféricamente a los ductos biliares de segundo orden y representan el 20 al 25% de los casos. Los CCp se originan en uno de los ductos hepáticos principales, ya sea desde el conducto hepático común o a partir de su bifurcación (Tumores de Klatskin), correspondiendo al 50% - 60% de los casos. Finalmente, los CCe (Fig. 2) se originan en el ducto biliar desde la inserción del conducto cístico hasta la ampolla de Vater, presentándose en el 20% a 25% de los pacientes.3,4,5,6
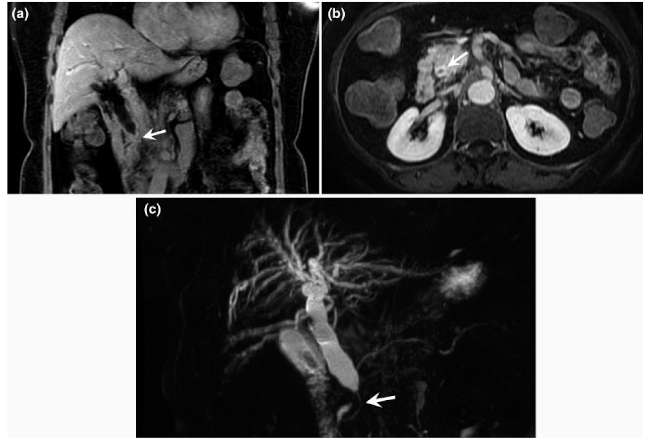
Fig. 2 CC extrahepático. (a) Imagen coronal y axial (b) de RM en secuencia potenciada enT1 con saturación grasa post inyección de gadolinio, que evidencia engrosamiento e impregnación parietal del colédoco distal con disminución del calibre luminal (flecha). (c) Colangiopancreatografía por RM (CPRM) con Reconstrucción de Proyección de Máxima Intensidad (MIP) 3D donde se demuestra engrosamiento del conducto colédoco distal causando estenosis abrupta a ese nivel (flecha) y dilatación ductal proximal por encima de la lesión.
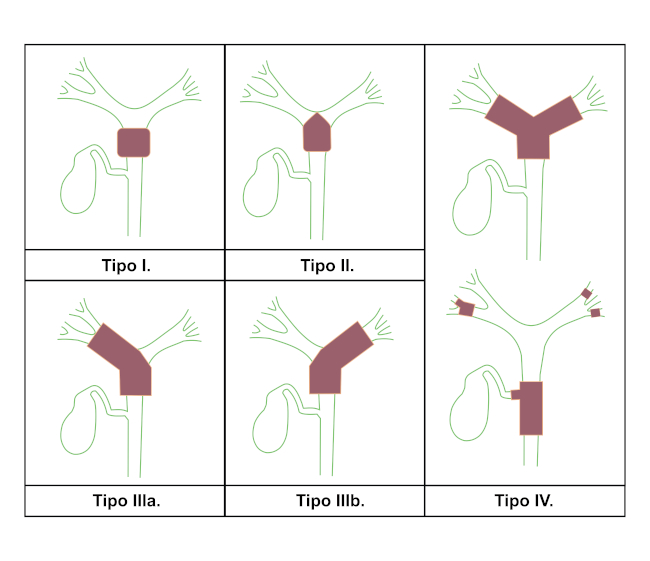
De acuerdo al compromiso anatómico longitudinal de la vía biliar, los CCp, también llamados Tumores de Klatskin (Fig. 3), se sub-clasifican según el sistema de Bismuth - Carlette.7,8
Tipo I (Fig. 4): Tumor que afecta el conducto hepático común.
Tipo II (Fig. 5): Tumor que compromete la bifurcación del conducto hepático y los conductos hepáticos principales derecho e izquierdo, causando obstrucción a nivel del hilio.
Tipo IIIa y IIIb: Tumor que se extiende hasta los ductos secundarios intrahepáticos derechos e izquierdos respectivamente, sin obstrucción ductal contralateral.
Tipo IV (Fig. 6): Tumor que afecta los ductos intrahepáticos secundarios y terciarios de ambos lóbulos, causando obstrucción bilateral.
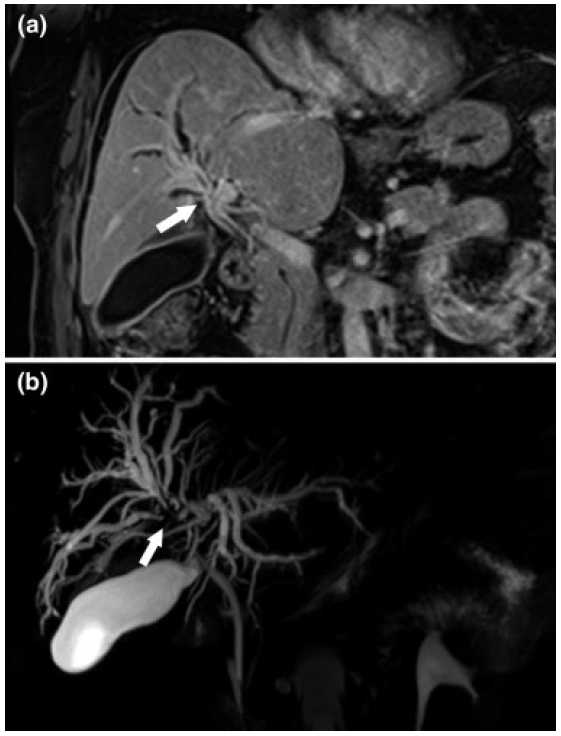
Fig. 6 CC periductal Bismuth - Carlette Tipo IV. (a) Imagen coronal de RM en secuencia potenciada en T1 con supresión de la grasa post inyección de gadolino, donde se observa lesión infiltrativa en el conducto hepático común y los conductos hepáticos derecho e izquierdo, evidenciándose el realce parietal post contraste endovenoso (flecha) e imagen de CPRM MIP 3D (b), donde se aprecia la interrupción abrupta de la vía biliar a nivel del conducto hepático común, además de la dilatación de las vías biliares intrahepáticas.
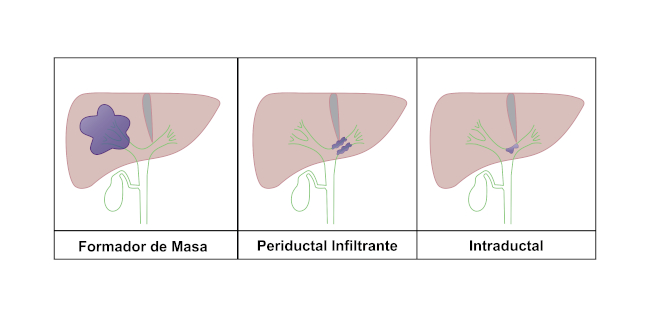
En la década de 1990, el Liver Cancer Study Group of Japan propuso clasificar los CC según el patrón de crecimiento del tumor (Fig. 7) en: formador de masa, periductal infiltrante e intraductal, debido a que la morfología permite una mejor interpretación radiológica, además de ser un indicador importante del comportamiento de la neoplasia, determinando el pronóstico y el enfoque terapéutico que se le dará.7,8
Colangiocarcinoma Formador de Masa
El CC formador de masa invade el parénquima hepático extendiéndose a través de los canales portovenosos.
En los estudios de TC (Fig. 8a) sin contraste endovenoso se presenta como una masa hipodensa, homogénea, de márgenes lobulados e irregulares. En el estudio con inyección de contraste endovenoso (Fig. 8b), en fase arterial el patrón de realce generalmente es periférico, fino e irregular, mostrándose hipodenso o isodenso en fase venosa portal, con una impregnación gradual centrípeta en fase tardía. Esos hallazgos están relacionados con la composición histológica de la masa, donde la porción periférica está compuesta por células viables del tumor y el centro se compone de estroma desmoplásico, tejido necrótico, mucina o escasas células viables. Es así como los tumores con necrosis central o mucina no realzan en fase tardía, permaneciendo hipodensos en las tres fases.7,8
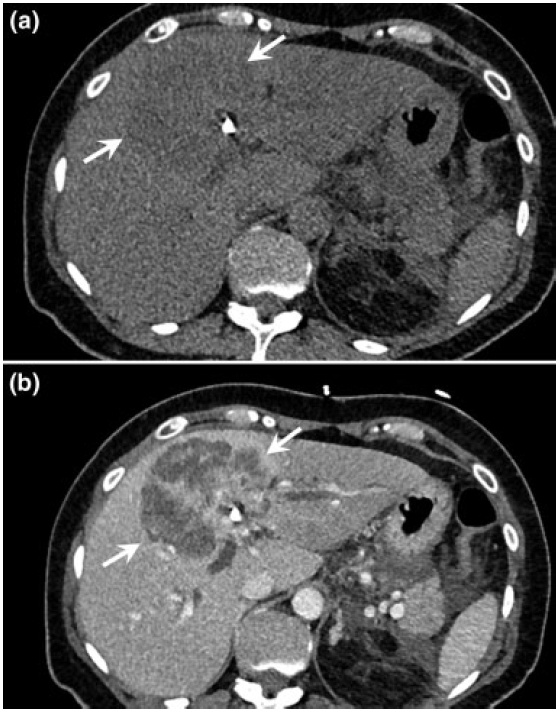
Fig. 8 CC formador de masa. Imágenes axiales de TC, donde se evidencia una gran masa ligeramente hipodensa en fase previa a la inyección de contraste endovenoso (a) que compromete el segmento anterior del lóbulo hepático derecho y el segmento medial del lóbulo hepático izquierdo (flecha) con impregnación centrípeta post inyección de contraste en fase portovenosa (b) (flecha).
Además, se ha visto que el patrón de realce depende en cierto grado del tamaño del tumor. Por ejemplo, los tumores menores de 1 cm de diámetro pueden demostrar realce homogéneo, simulando un HCC. La demostración de lavado en la fase venosa y tardía presente en los carcinomas hepatocelulares ayudaría a diferenciarlo del CC.7,8
Otros hallazgos secundarios visibles en TC incluyen: la retracción capsular, la dilatación de las vías biliares situadas periféricamente a la masa, la litiasis hepática intratumoral, los nódulos satélites, la atrofia lobar, el encajonamiento vascular sin trombo tumoral y las adenopatías.7,8
En estudios de RM, el CC formador de masa se muestra como una masa hipointensa a isointensa en secuencias ponderadas enT1, mientras que en secuencias ponderadas enT2 se muestra con leve a moderada hiperintesidad, dependiendo de la proporción de fibrosis/mucina. El patrón de realce tras la inyección de gadolinio es similar a la TC, presentando un realce fino, periférico e irregular en fase arterial temprana (Fig. 9a), con realce progresivo centrípeto en fase tardía (Fig. 9b). En los tumores predominantemente fibróticos el realce solo podría ser visible en fase tardía.8
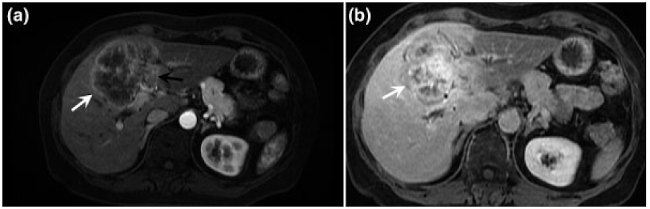
Fig. 9 CC formador de masa. Imágenes axiales de RM en secuencias potenciadas con saturación de la grasa en T1 con gadolinio fase arterial (a) y fase portovenosa (b), que muestran una masa intrahepática lobulada con impregnación progresiva y centrípeta (flecha blanca) con infiltración de la vena porta izquierda (flecha negra).
Los hallazgos secundarios identificados en TC han sido descritos también en RM; las secuencias ponderadas con saturación grasa en T1 y T2 son especialmente útiles en la detección de adenopatías.7,8
Colangiocarcinoma Periductal Infiltrante
Los CC periductales infiltrantes pueden afectar desde los conductos de segundo orden hasta la inserción del conducto cístico. Se caracteriza por su crecimiento a lo largo del conducto biliar dilatado o estenosado, manifestándose como una lesión elongada, espiculada o como una anomalía de la rama.7,8
En la TC, se puede observar un engrosamiento difuso periductal asociado a aumento de la impregnación del medio de contraste en fases arterial y venosa, ya sea en un ducto anormalmente dilatado o estenosado como también podría haber dilatación de los ductos periféricos. Debido a que el tumor posee una histología esclerosante puede estar presente un marcado realce en fase tardía.8
Entre los diagnósticos diferenciales se deben tener en cuenta los linfonodos metastásicos periportales de los tumores extrahepáticos que, a diferencia del CC, no presentan dilatación ductal lobar o segmentaria.7,8
La RM es considerada el mejor método de diagnóstico imagenológico para el diagnóstico del CC periductal infiltrante. Se manifiestan como un engrosamiento periductal hipointeso en T1, mientras en T2 podrían ser hipointensos o hiperintensos dependiendo del grado de esclerosis o fibrosis. Posterior a la inyección de contraste endovenoso, muestran impregnación importante en fase tardía.7,8,9
La detección del tumor en estadios iniciales es muy difícil debido a la apariencia benigna de la estenosis. Se ha visto que la presencia de engrosamiento parietal mayor a 5 mm, la estenosis asimétrica abrupta y de márgenes irregulares son hallazgos indicadores de malignidad.7,8,9
Se ha visto que la exactitud de la evaluación del compromiso de los ductos con TC es de 86%, con una sensibilidad y especificidad para el compromiso de la vena porta de 89% y 92%, para la arteria hepática de 83% y 93% y para el compromiso de los linfonodos es de 61% y 88%, respectivamente.10 La evaluación mediante RM es similar a la TC, aunque la Colangiopancreatografía por Resonancia Magnética (CPRM) delimita con mayor exactitud la extensión del tumor a nivel de los ductos.10,11
Colangiocarcinoma Intraductal
Es un tumor de crecimiento lento, de pronóstico relativamente favorable y frecuentemente resecable quirúrgicamente, debido a que se encuentra confinado a nivel intraductal. Es el CC menos frecuente y representa entre el 8 y el 18% de los casos según lo descrito en la literatura.11,12
Se manifiesta frecuentemente con una marcada dilatación ductal difusa asociada o no a una masa de aspecto papilar o bien una masa polipoidea dentro de una dilatación ductal localizada. Las lesiones de pequeño tamaño son imperceptibles con los métodos de diagnóstico por imágenes. Además, pueden verse cálculos intraductales debido a la mayor predisposición para desarrollar los mismos.11,12
RM con Secuencia Potenciada de Difusión (DWI)
La evaluación con secuencias de DWI es sumamente útil en la detección de una estenosis ductal de origen maligno, en la diferenciación entre el HCC y el CC, así como también en la evaluación del compromiso ductal y afectación intrahepática en el caso de los CC perihiliares.13,14,15 Un estudio realizado por Park y col.,13 demostró que las secuencias de DWI con valores b altos (800 second mm2), ayudan a distinguir la estenosis de la vía biliar de etiología benigna de la estenosis biliar de etiología maligna y, consecuentemente, prevenir biopsias o cirugías innecesarias en casos de estenosis benignas. En este estudio, se obtuvo un rango de precisión diagnóstica del 91,3% - 94,2% en evaluaciones con DWI adicionalmente a la RM convencional vs un rango de precisión del 78,3% - 81,2% para las evaluaciones que se realizaron únicamente con imágenes de RM convencional.
En estudios con secuencias de DWI la mayoría de los CC son marcadamente hiperintensos en comparación con el parénquima hepático normal adyacente. Un estudio evidenció que los valores de ADC de los CC fueron menores que los valores de ADC del parénquima hepático normal [(1,042 10 -3 mm2/s ± 0,2210 -3 mm2/s) vs (1,362 10 -3 mm2/s ± 0,187 10 -3 mm2/s) (p < 0,0001)].14
Además, otros estudios han demostrado que los CC formadores de masa pueden ser diferenciados de los HCC, especialmente en tumores menores a 3 cm de diámetro, mediante la morfología en target sign (Fig. 10) que presentan los CCi en secuencias de DWI, demostrando significativa restricción en difusión en la periferia e hipointensidad central, debido al mayor componente fibrótico. Esa característica es el equivalente al típico patrón de realce que muestran los CC formadores de masa visualizados en secuencias dinámicas de RM.14,15
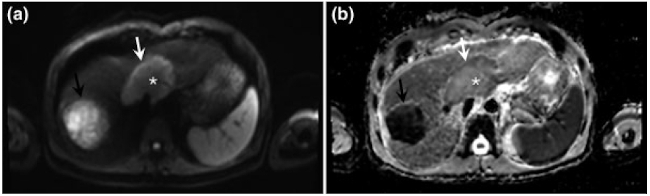
Fig. 10 CC formador de masa. RM en secuencias de DWI (a) y Mapa ADC correspondiente (b) que muestran el signo de target sign en un paciente con CC formador de masa. Nótese la intensidad de señal heterogénea, con hiperintensidad lineal periférica (flecha blanca) e hipointensidad central correspondiente al área de fibrosis central (asterisco). En el segmento VII-VIII se evidencia además un hematoma secundario a ablación de un nódulo metastásico (flecha negra).
También se ha descrito que las secuencias de DWI con valores b altos, adicionales a las secuencias dinámicas con inyección de ácido gadoxético (contraste hepatoespecífico) aumentan significativamente la sensibilidad en la detección de la extensión ductal o invasión intrahepática en los tumores perihiliares, en comparación a la caracterización de la lesión únicamente con secuencias dinámicas, lo que es útil en la evaluación de la resecabilidad tumoral.16
Evaluación Preoperatoria del Colangiocarcinoma
Es imprescindible identificar los criterios de resecabilidad tumoral, debido a que el único tratamiento curativo potencial para esta enfermedad, es la resección del tumor con márgenes negativos.17,18
Al momento del diagnóstico, más del 50% presentan linfonodos positivos y de 10% al 20% tienen compromiso peritoneal, por lo que requiere una minuciosa evaluación de la extensión local y a distancia.17,18
En aquellos pacientes candidatos a resección tumoral, es indispensable indicar la localización del tumor, las variantes anatómicas de las arterias hepáticas, venas porta y suprahepáticas, así como también las de los ductos biliares para así poder determinar el abordaje quirúrgico. Localmente, es importante evaluar el nivel de obstrucción, el compromiso vascular, la existencia de atrofia de lóbulos hepáticos. Además, debe incluirse la evaluación de los pulmones y las posibles metástasis peritoneales.17,18
Entre los criterios de irresecabilidad tumoral que el radiólogo debe indicar se encuentran.17,18
Infiltración más allá de las ramas ductales de segundo orden en ambos lóbulos
Invasión de la vena porta principal (Fig. 11) o la arteria hepática propia
Atrofia de un lóbulo hepático con compromiso vascular contralateral
Combinación de compromiso vascular extenso en un lóbulo y compromiso de ramas ductales secundarias del lóbulo contralateral
Compromiso de linfonodos: celiacos, para-aórticos, peri-pancreáticos, mesentéricos superiores, pancreatoduodenales
Metástasis a distancia (hepática, pulmonar, peritoneal)17,18
En resumen, las contraindicaciones generales para la resección quirúrgica del tumor incluyen: afectación bilateral, multifocal, metástasis a distancia y las comorbilidades asociadas al riesgo quirúrgico.
Volumetría Hepática (Fig. 12)
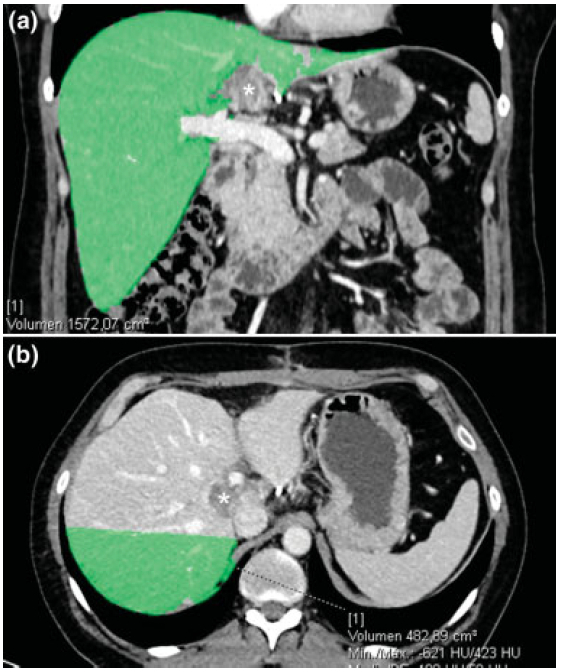
Fig. 12 Volumetría hepática. Imagen coronal (a) y axial (b) de TC en un paciente con CC tipo formador de masa (asterisco) que compromete los segmentos I, IV y VIII, en un hígado sano, resecable con plan de hepatectomía izquierda ampliada. Se realiza medición con reconstrucción volumétrica encontrándose un volumen residual de los segmentos VI y VII de 482 ml, lo que corresponde a un 27% del total, resultando un CC operable sin necesidad de una embolización de la vena porta previa a la hepatectomía.
Los avances en el ámbito quirúrgico hacen posible la realización de hepatectomías en pacientes con neoplasias primarias o metástasis. Para ello es necesario calcular el volumen hepático residual, debido a que un volumen residual pequeño causaría insuficiencia hepática posterior a la hepatectomía.19
El volumen hepático residual normal en pacientes sanos sometidos a hepatectomías se considera igual o mayor al 20% del volumen total, ascendiendo a 40% en pacientes con hepatopatía crónica. En el caso de tener un volumen remanente por debajo de lo normal, lo indicado es realizar una embolización portal preoperatoria, a fin de hipertrofiar el futuro remante hepático, lo que se logra aproximadamente luego de cuatro semanas.19
Pronóstico
El CC es una neoplasia de mal pronóstico, con una supervivencia, a los 5 años sin tratamiento, de 1% y de 11% a 31% con tratamiento quirúrgico.2 Presenta una recurrencia entre el 60% al 90% posterior a la resección quirúrgica.20
Conclusión
El CC es un tumor maligno poco frecuente que se manifiesta de diversas formas. Sus características histológicas y su comportamiento, tanto en la TC como en la RM con contraste endovenoso, hacen que sea fácilmente reconocible. La resección quirúrgica con margen negativo es el objetivo principal para lograr el tratamiento curativo, por lo que los estudios dinámicos de TC y RM son los mejores métodos diagnósticos para su evaluación. Es por todo ello que los radiólogos debemos saber reconocer e indicar en el reporte un CC potencialmente resecable.