El timoma de ubicación cervical es una entidad infrecuente (4%) y se debe a una anomalía en el desarrollo embrionario. El timo se origina de la tercera bolsa faríngea y, durante la 5ª semana de gestación, migra junto con las paratiroides inferiores hasta alcanzar su posición definitiva. Por eso, los ectópicos pueden localizarse en cualquier lugar del trayecto de descenso, siendo más frecuente cerca del polo inferior de la tiroides, desde el ángulo de la mandíbula hasta el mediastino superior.1
Existen 2 sistemas de clasificación aceptados universalmente:
▪ 1. Índice de Masaoka (1981) revisado por Koga (1994). Fue descripto para los timomas mediastínicos y está basado en la invasión capsular. Los categoriza en 4 estadios1:
▪ Estadio I: completamente encapsulado y sin signos de invasión macroscópica y microscópica.
▪ Estadio II: invasión microscópica capsular en tejido adiposo mediastinal o pleura.
▪ Estadio III: invasión macroscópica de órganos o vasos adyacentes.
▪ Estadio IVa: diseminación a otros órganos de la cavidad torácica.
▪ IVb: extensión a distancia.
▪ Los factores pronósticos más relevantes están dados por el índice de Masaoka-Koga, por el tipo histológico y por la resección completa del tumor2.
▪ 2. La OMS clasifica los tumores tímicos según la celularidad microscópica en diferentes tipos3:
▪ Tipo A: células epiteliales ovales o fusiformes; la sobrevida a 15 años cercana al 100%.
▪ Tipo AB: o también llamado timoma mixto: células redondas o poligonales y presentan rasgos característicos del timoma tipo A con un componente linfocitario de densidad variable.
▪ Tipo B: B1 timoma predominantemente cortical, B2 timoma cortical, B3 carcinoma tímico bien diferenciado, según la proporción de linfocitos y del aumento de la atipía citológica de las células epiteliales. Sobrevida a 15 años es del 90%.
▪ Tipo C: atipía citológica y pérdida de las características organotípicas del timo; este último término es sinónimo de carcinoma tímico, que generalmente se encuentra avanzado al momento del diagnóstico, con una sobrevida del 35% a los 5 años.
Mujer de 70 años, con obesidad grado II, antecedente de enfermedad pulmonar obstructiva crónica (EPOC) y exfumadora de 1 paq/year, sin antecedentes heredofamiliares de relevancia. Consulta por presentar un tumor lateral de cuello izquierdo de 6 años de evolución, con aumento progresivo en el último año, sin otros síntomas clínicos, ni antecedentes de enfermedad tiroidea. El examen físico muestra un tumor laterocervical izquierdo de aproximadamente 7 × 5 cm, duro elástico, adherido a planos profundos en zona II-III de los niveles ganglionares del cuello. Presenta laboratorio con anticuerpos tiroideos negativos. Hormonas tiroideas dentro de parámetros normales. Ecografía y eco-Doppler de tiroides y partes blandas que informa glándula tiroides con disminución de tamaño, ecoestructura heterogénea sin identificar imágenes nodulares y vascularización conservada. En región cervical lateral izquierda, describe la masa de 70 ×40 × 45 mm hipoecoica, heterogénea, con escasa vascularización en su interior, de bordes regulares. Adyacentes a la masa, describe imágenes de aspecto ganglionar, la mayor de 25 × 8 mm. La punción ecoguiada mostró presencia de material hemático con tejido linfoide y acúmulo de células epiteliales, con leve anisocariosis y nucléolo evidente. La inmunohistoquímica dio CD3 + positivo difuso en células linfoides; CK (AE1AE3) positivo en células epiteliales. Diagnóstico: hallazgos histológicos e inmunofenotípicos compatibles con timoma. Anticuerpos antirreceptores de acetilcolina negativos. La tomografía computarizada (TC) de macizo facial, cuello y tórax informa, en región lateral izquierda, una formación de 47 × 43 × 72 mm que realza con contraste endovenoso, desplaza ventralmente la carótida primitiva y en sentido posterior la vena yugular interna (Fig. 1), cubierto parcialmente por el músculo esternocleidomastoideo. Hacia la derecha alcanza el espacio parafaríngeo y se ubica por detrás de los cartílagos laríngeos y el hueso hioides. Presencia de adenopatías en la cadena yúgulo carotídea izquierda; la de mayor tamaño es de 11 × 7 mm. En el sector inferior del lóbulo superficial de la glándula parótida izquierda se detecta una imagen redondeada de 13 ×10 mm similar, que podría corresponder a una adenopatía intraparotídea. Mediastino y axilas, libres de adenomegalias. En mediastino posterior se observa variante anatómica de arteria subclavia derecha que cruza por detrás del esófago (arteria lusoria).
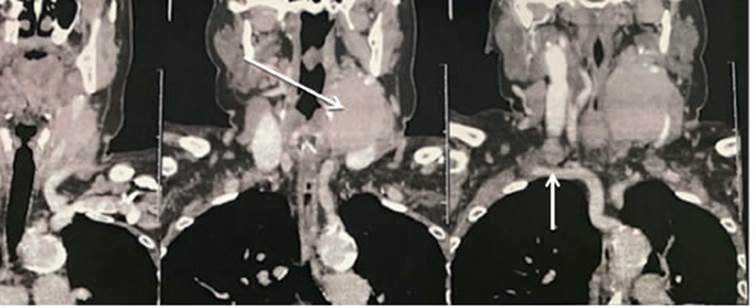
FIGURA 1 Tomografía de cuello con contraste endovenoso en la que se se señala, con la flecha larga, formación con densidad de partes blandas, con realce de contraste endovenoso, de 47 × 43 × 72 que desplaza ventralmente a la carótida primitiva y en sentido posterior a la vena yugular interna, alcanzando el espacio parafaríngeo hacia la derecha. Como variante anatómica se señala con flecha corta la arteria subclavia derecha aberrante que cruza por detrás del esófago (arteria lusoria)
Se planificó el tratamiento quirúrgico con abordaje cervical izquierdo en fecha 12/04/2021. Se realizó incisión cervical submandibular arciforme (Fig. 2), y se evidenció una masa tumoral laterocervical de 7 × 6 cm sólida, de bordes regulares, en íntimo contacto y desplazando a la vena yugular interna, la carótida primitiva y su bifurcación. Hacia cefálico se ponía en contacto con la parótida. Por disección subadventicial se separó el tumor de los vasos carotídeos. Prosiguiendo la disección podálica se identificó el nervio vago. Se separaron la vena yugular interna y el X par, y se preservaron ambas estructuras (Fig. 2). Se completó la tumorectomía en bloque junto con el polo inferior de la parótida izquierda y los ganglios adyacentes (véase Fig. 2 A y B). La biopsia intraoperatoria describió una neoplasia constituida por células ahusadas con gran componente de linfocitos pequeños acompañantes. Se hallaba el tumor encapsulado y se difirió el diagnóstico. La paciente dada de alta el segundo día posquirúrgico, sin complicaciones ni secuelas; el último control fue tres meses después, sin particularidades clínicas.
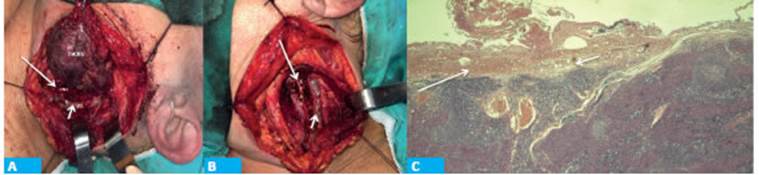
FIGURA 2 A y B. Se evidencia el tumor en contacto con la vena yugular interna (flecha corta) en su región posterior y en contacto con el X par craneal (flecha larga).X par: nervio vago. VYI: vena yugular interna. C: A la microscopia (en aumento 10x con tinción H&E), timoma AB de la clasificación de la OMS, constituído por proliferación de células ahusadas con numerosos linfocitos pequeños sin evidencia microscópica de invasión capsular
Resultado de la biopsia diferida informó pieza quirúrgica de 7 × 6 cm sólida, lobulada, parda, de consistencia aumentada; por la microscopia se lo clasificó en un timoma AB de la clasificación de la OMS, constituido por proliferación de células ahusadas con numerosos linfocitos pequeños (Fig. 3). La lesión se encontraba encapsulada. Seis ganglios linfáticos estuvieron libres de lesión. Las tinciones con inmunohistoquímica demostraron positividad en los elementos epiteliales con citoqueratina y en los elementos linfoides con CD5 y CD3. Con CD20 se marcaron escasos linfocitos. La marcación con Ki67 fue del 3%. La masa fue diagnosticada como timoma estadio I acorde con la clasificación de Masaoka staging system of thymoma y tipo AB de la OMS.
Dado que el timoma es una neoplasia frecuente del mediastino anterosuperior, su ubicación ectópica plantea un desafío en el diagnóstico por lo inusual de esa localización. Su incidencia máxima ocurre entre la tercera y quinta década de la vida. Los síntomas de presentación guardan relación con los efectos locales de masa o asociados a síndromes sistémicos, el más frecuente la miastenia grave. La diferenciación entre timomas benignos y malignos se basa en la presencia de la invasión macroscópica de las estructuras adyacentes, metástasis o signos microscópicos de invasión capsular.3
El diagnóstico preoperatorio de este tipo de tumores es dificultoso debido a su baja frecuencia, a que no existen signos patognomónicos de enfermedad y a que los resultados histológicos por punción previa pueden resultar de carácter inespecífico al basarse primordialmente el diagnóstico en el descarte de otras patologías4. Los diagnósticos diferenciales deben hacerse con masas congénitas en el cuello y lesiones adquiridas como adenomas tiroideos, adenopatías cervicales, neoplasias linfoproliferativas, quiste dermoide o epidermoide, o lesiones inflamatorias5.
En los casos malignos, la resección completa y el grado de invasión (Masaoka-Koga) son los que determinan el pronóstico y la sobrevida. En etapas avanzadas o enfermedad recurrente, la quimioterapia sistémica produce altas tasas de respuesta. El presente caso se interpretó como estadio I según el índice de Masaoka-Koga y tipo AB de la clasificación de la OMS. Debido a que el tumor fue resecado por completo, no se agregó otro tratamiento complementario. La paciente continúa con controles periódicos, sin evidencia de complicaciones postoperatorias alejadas ni de recidiva.











 texto em
texto em 


