Introducción
En Argentina la babesiosis bovina es una enfermedad causada por dos protozoarios del Phylum Apicomplexa: Babesia bovis y Babesia bigemina(Späth, 1986). Estos agentes son transmitidos por la garrapata común del bovino, Rhipicephalus microplus, y producen, entre otros trastornos, cuadros de anemia hemolítica (Guglielmone, 1995). A nivel regional, la babesiosis, junto a la anaplasmosis —causada por la rickettsia Anaplasma marginale— integran el complejo “Tristeza bovina”, el cual constituye uno de los problemas sanitarios de mayor relevancia en los rodeos bovinos del Noroeste argentino (Späth, 1986; Aráoz et al., 2017). Si bien la infección por estos agentes produce cuadros clínicos similares, B. bovis puede causar signología nerviosa (babesiosis cerebral), dada su capacidad para inducir la oclusión de capilares cerebrales con eritrocitos parasitados (Hadani et al., 1982). La sensibilidad del ganado a Babesia spp. varía según la edad: los bovinos jóvenes son parcialmente resistentes a los efectos clínicos de la primo infección con estos agentes, mientras que la primo infección en ganado de mayor edad suele producir enfermedad severa (Trueman y Blight, 1978; Levy et al., 1982; Guglielmone, 1995). Sobre esta base, si la totalidad de los bovinos de un hato se infectan —y desarrollan inmunidad específica— antes del desvanecimiento de la resistencia inespecífica, se establece un escenario de estabilidad enzoótica, una situación epidemiológica donde la ocurrencia de babesiosis clínica es escasa en presencia de altos niveles de trasmisión de Babesia spp. (Mahoney y Ross, 1972). En el contexto contrario —o de inestabilidad enzoótica—, con niveles más bajos de transmisión de Babesia spp., las primo infecciones ocurren con frecuencia luego del desvanecimiento de la tolerancia inespecífica, con la consiguiente aparición de brotes de babesiosis.
Si bien es una característica de gran relevancia en la epidemiología de las babesiosis, la resistencia de los terneros a la enfermedad clínica no es un fenómeno absoluto, existen descripciones de cuadros de babesiosis por B. bovis en terneros (De Vos et al., 1976; Kessler et al., 1983; Yeruham et al., 2003; Santarosa et al., 2013; Oliveira et al., 2018). Esta información es sin embargo limitada para la Argentina, donde al presente se reporta un único caso de babesiosis por B. bovis en un feto abortado de ocho meses (Alcaraz et al., 2004).
Este trabajo describe dos casos de babesiosis cerebral en terneros menores de 15 días de edad de sendos rodeos, destacándose los aspectos clínicos, patológicos, epidemiológicos y de diagnóstico.
Materiales y Métodos
El primer caso ocurrió en octubre de 2017 en un establecimiento de cría bovina (E1) ubicado en el departamento Rosario de Lerma, provincia de Salta (24°51'36,5"S; 65°36'51,7"W), donde un ternero de ocho días de edad presentó un cuadro de severo decaimiento y murió al día siguiente de iniciados los signos. El segundo caso ocurrió en noviembre de 2017, en otro establecimiento de cría (E2) ubicado en el departamento Santa Bárbara, provincia de Jujuy (23°48'19,7"S; 64°25'42,5"W), donde se registró la muerte de cuatro terneros, 15 vacas y 15 natimortos. Los vacunos afectados presentaban fiebre (40,5ºC), decaimiento y debilidad al nacimiento en el caso de las crías. Se estudió solo uno de los terneros, con edad estimada en 15 días, pero también dos de las vacas afectadas. Los lotes de madres estaban compuestos por 190 y 150 vientres en E1 y E2, respectivamente.
Los dos terneros y las dos vacas en E2 fueron sometidos a necropsia, colectándose muestras de órganos para estudios histopatológicos, extendidos de sangre y de corteza cerebral para exámenes parasitológicos y tejidos para estudios moleculares.
Las muestras para histopatología fueron fijadas en formol bufferado al 10%, procesadas por las técnicas clásicas de inclusión en parafina y luego teñidas con Hematoxilina-eosina. Adicionalmente, sobre algunos cortes de corteza cerebral, se efectuaron tinciones especiales con Giemsa para identificar hemoparásitos en los capilares nerviosos (Silva et al., 2018). Los extendidos de sangre se obtuvieron de vasos sanguíneos superficiales tanto ante como post-mortem y luego se procesaron por técnicas ya descriptas (Benavides Ortiz et al., 2012). Los extendidos de corteza cerebral se confeccionaron según la técnica descripta por Hadani et al. (1982). A partir de muestras de tejido de ambos terneros se efectuó la extracción de ADN mediante el método convencional de fenol-cloroformo y luego se realizó una PCR anidada, mediante la amplificación de fragmentos del gen 18SrRNA específico para B. bovis. Los oligonucleótidos utilizados para la primera vuelta (781 pb) fueron Bovis-for 5´AACCTGGTTGATCCTGCCAGTA´3 (Thompson et al., 2018) y RLB-R2 5´CTAAGAATTTCACCTCTGACAGT´3 (Gubbels et al., 1999); para la segunda vuelta (132 pb) se utilizaron Bovnew18sfor 5´CAGGTTTCGCCTGTATAATTGAG´3 (Thompson, com. pers.) y RLB-R2. Las condiciones y los programas de ciclado están descriptos en Thompson et al. (2018). Como controles positivos se incorporaron muestras de ADN de B. bovis obtenidos de una cepa atenuada y otra patógena cultivadas in vitro; y como control negativo se utilizó una muestra para el control de contaminación a la que no se adicionó ADN.
Adicionalmente, se extrajeron muestras de sangre para serología de 20 vacas en cada establecimiento (E1 y E2), entre ellas la madre del ternero sometido a necropsia en E1. La presencia de anticuerpos específicos contra B. bovis y B. bigemina en estas muestras se determinó por la técnica de ELISA indirecto descripta por Echaide et al. (2004), mientras que los anticuerpos contra A. marginale se determinaron por la técnica de ELISA de doble paratope (Sarli et al., 2019). Por último, se obtuvieron también extendidos de sangre periférica en nueve vacas del E1 y seis vacas del E2, los cuales se procesaron de igual forma que para los terneros (Benavides Ortiz et al., 2012).
Resultados
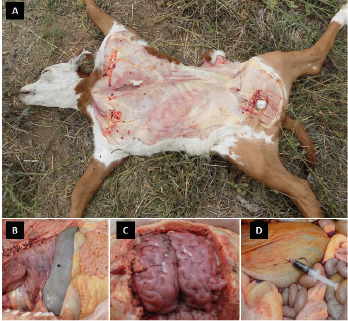
Los hallazgos de necropsia fueron similares en los terneros del E1 y E2, observándose ictericia difusa (Figura 1A), esplenomegalia (Figura 1B) y coloración ocre del hígado. Ambos encéfalos mostraron congestión cerebral difusa, que otorgaba una coloración rosada al tejido nervioso (Figura 1C). En el ternero del E2 se apreció orina en vejiga teñida de coloración oscura (aparente hemoglobinuria) (Figura 1D), lo cual no pudo determinarse en el ternero del E1 ya que su vejiga había sido predada. El examen histopatológico mostró congestión de los capilares corticales del sistema nervioso central, con degeneración moderada y necrosis aislada de los cuerpos neuronales. En dichos capilares se identificaron estructuras compatibles con hemoparásitos intraeritrocitarios. Tanto en los extendidos sanguíneos como cerebrales de ambos terneros se observó abundante presencia de estructuras intra-eritrocitarias compatibles morfológicamente con B. bovis (Figura 2). Por último, los estudios moleculares (PCR) fueron positivos a B. bovis en las muestras extraídas de los dos terneros. Por otra parte, los hallazgos anátomo-patológicos en las vacas sometidas a necropsia del E2 coincidieron con los observados en los terneros (ictericia, esplenomegalia y hemoglobinuria). Un 95% de las vacas muestreadas en el E1 presentó anticuerpos contra B. bovis, un 42% contra B. bigemina y un 74% contra A. marginale. En las vacas muestreadas en el E2, esos valores fueron de 4% para B. bovis, 2% para B. bigemina y 54% para A. marginale. Finalmente, el examen de los extendidos de sangre de las vacas muestreadas arrojó resultados negativos en el E1, mientras que cinco de seis extendidos (83,3%) fueron positivos a B. bovis en el E2.
Discusión
A la necropsia las lesiones en los terneros fueron similares a las informadas en otros casos de babesiosis cerebral (Barros et al., 2006; Marin y Aguirre, 2017). A su vez, los análisis complementarios confirmaron dicho cuadro en ambos terneros. Como ya se dijo, la ocurrencia de babesiosis en terneros es poco frecuente (Guglielmone et al., 1992). Esto se debería a la presencia de mecanismos de defensa inespecíficos durante los primeros meses de vida, que permiten cursar las primo-infecciones sin signos clínicos en los terneros, resultando en una inmunidad adquirida contra la babesiosis que persiste por toda su vida (Levy et al., 1982). No obstante, distintos reportes documentan la ocurrencia de casos clínicos asociados a la infección por B. bovis en terneros menores a los 15 días de vida (De Vos et al., 1976; Kessler et al., 1983; Santarosa et al., 2013; Oliveira et al., 2018).

Figura 2. Ternero de 15 días (del establecimiento E2) A- Encéfalo, congestión de los capilares de la corteza cerebral (20x, H&E). B- Congestión de los capilares de la corteza cerebral con numerosos eritrocitos parasitados por Babesia bovis (azul oscuro) (40x, Giemsa) C- Extendido de corteza cerebral con abundante presencia de Babesia bovis. D- Extendido de sangre periférica con eritrocitos parasitados con estructuras intraeritrocitarias compatibles morfológicamente con Babesia bovis (100x, Giemsa).
Como se dijo, el contexto epidemiológico posee gran relevancia en la ocurrencia de brotes de babesiosis, incidiendo principalmente la edad de los bovinos, factores ambientales, fluctuaciones estacionales en la población del vector (R. microplus) y la situación de estabilidad enzoótica (o no) del rodeo (Guglielmone, 1995). Esta última puede determinarse en base a pruebas serológicas para cohortes de terneros de 7-9 meses de edad, pero no en bovinos adultos, dado que estas pruebas subestiman la proporción de ellos naturalmente protegidos contra Babesia spp. Esto es debido a que ocurre una caída de los niveles de anticuerpos circulantes cuando vacunos —que desarrollaron inmunidad específica en el pasado— no sufren reinfecciones por largos períodos de tiempo (Aguirre et al., 1993, Torioni, com. pers). No obstante, el empleo de técnicas serológicas en adultos sí permite algunas inferencias cuando la gran mayoría de los bovinos presenta anticuerpos contra Babesia spp. En el presente trabajo, la ausencia de casos clínicos de babesiosis en adultos a pesar de altos niveles de transmisión de B. bovis (95% de vacas positivas por serología) hacen suponer una condición de estabilidad enzoótica en E1. Sin embargo, la ocurrencia de un brote de babesiosis clínica con mortandad de 15 vacas evidencia una situación de inestabilidad enzoótica en E2. En síntesis, podría concluirse que las dos muertes descriptas en terneros ocurrieron en situaciones epidemiológicas distintas: la primera (E1) como un caso individual en una población epidemiológicamente estable a B. bovis y la segunda (E2) dentro de un brote en una población susceptible a la babesiosis por B. bovis.
La infección por B. bovis tiene un periodo de prepatencia de aproximadamente unos siete días: su inoculación al vacuno se produce por los estadios larvarios de R. microplus entre las 24-72 horas post-fijación (Solari y Quintana, 2013). Sumado a esto, diversos autores describen la vía transplacentaria como otra posible forma de transmisión (De Vos et al., 1976; Yeruham et al., 2003, Alcaraz et al., 2004). En base a estas consideraciones, se puede presumir una infección post-natal como más probable en el ternero de 15 días (E2). Téngase en cuenta que el individuo tenía una edad que doblaba el período de pre-patencia de B. bovis y que el caso ocurrió en el contexto de un brote con gran exposición a estadios infestantes de R. microplus evidenciable tanto en el ternero como en los adultos. Por el contrario, la vía de transmisión transplacentaria podría ser tomada como más probable en el ternero de 8 días (E1). La madre de este último resultó serológicamente positiva a B. bovis, pero el parásito no pudo observarse en el extendido sanguíneo de la vaca. Esto no permite concluir sobre la ocurrencia de una infección pre-natal, aunque tampoco descartarla por completo, dada la posible infección crónica de la vaca. En esta condición, no siempre se registra la presencia de parasitemia por métodos clásicos (Vanzini y Ramírez, 1994), requiriéndose técnicas más sensibles, como la prueba PCR, para detectar B. bovis en la sangre de los portadores crónicos (Fahrimal et al., 1992), técnica que no pudo ser practicada.
Como ya se señaló, la babesiosis —particularmente por B. bovis— constituye una noxa relevante para los bovinos —sobre todo adultos— del NOA (Späth, 1986; Aráoz et al., 2017). Este trabajo describe, por primera vez en Argentina, la ocurrencia de babesiosis (B. bovis) en terneros, la que debería considerarse para el diagnóstico diferencial ante casos clínicos compatibles con esta hemoparasitosis en terneros de zonas enzoóticas