Introducción
El accidente cerebrovascular (ACV) es una patología caracterizada por la aparición repentina de déficit neurológico debido a una lesión focal en el sistema nervioso central como consecuencia de la perturbación de la circulación cerebral.1,2,3
En la población pediátrica, la incidencia de ACV es baja. Esta afecta entre 2 a 13 por cada 100.000 niños y es una de las 10 causas más frecuentes de mortalidad.4,5
Las fases de recuperación del ACV pueden clasificarse en hiperaguda (<24hs), aguda (1 a 7 días), subaguda temprana (7 días a 3 meses), subaguda tardía (3 a 6 meses) y crónica (>6 meses).6 En la fase subaguda, puede existir mejoría, ya que existe una reorganización cerebral que puede ser modulada por técnicas de rehabilitación a través del fenómeno de plasticidad neuronal.7
Los déficits neurológicos y las convulsiones son frecuentes y se presentan en el 40-90% de los casos.8,9,10 Las deficiencias neurológicas pueden ocasionar alteraciones cognitivas, sensoriales y/o motoras. Estas últimas comprometen la fuerza, la coordinación, las funciones motoras gruesas y/o los movimientos de los dedos, además puede haber distonía o hemiparesia.11,12)
El ACV genera un impacto en la condición de la salud y ocasiona deterioro en las funciones y estructuras corporales, limitaciones en la actividad y restricciones en la participación.11,12 Un estudio realizado en niños con ACV reportó un 13% de discapacidad moderada a grave y una mortalidad cercana al 38%.13 Vázquez López et al. evaluaron la funcionalidad en niños con ACV y enfermedades cardíacas e informaron un 65% de déficit moderado a grave.14 Otro estudio en niños con ACV evaluó los resultados funcionales al alta de un centro de rehabilitación y reportaron cambios significativos en los dominios de cuidado personal y en la movilidad según la Escala de Independencia Funcional en Niños (WeeFIM, por sus siglas en inglés).15
A pesar de haber un aumento en la incidencia de ACV en esta población16, no hemos encontrado estudios que describan la independencia y movilidad funcional durante el período de rehabilitación en la fase subaguda. Asimismo, consideramos relevante brindar información sobre estos cambios y dar a conocer datos locales sobre el ACV en esta población.
Por tales motivos, el objetivo de este estudio fue describir los cambios en la independencia y movilidad funcional en una muestra de niños con secuelas neurológicas secundarias a ACV en la fase subaguda que ingresaron a un instituto de rehabilitación de la provincia de Buenos Aires, Argentina.
Materiales y método
Diseño
Se realizó un estudio observacional, descriptivo, retrospectivo y longitudinal con la información recolectada de sujetos pediátricos con diagnóstico de ACV internados en un centro de rehabilitación de la provincia de Buenos Aires, Argentina, entre el 1 de febrero de 2005 y el 28 de febrero de 2023.
Criterios de elegibilidad
Se incluyeron sujetos de 4 a 18 años de edad con diagnóstico de ACV en la fase subaguda (>7 días y <6 meses de evolución).6 Este período coincide con el inicio de la rehabilitación temprana en nuestra institución. Todos participaron de un programa de rehabilitación integral intensivo, conformado por un equipo interdisciplinario de profesionales (médicos pediatras, neuropediatras, neuroortopedistas, fisiatras, psiquiatras, kinesiólogos, terapistas ocupacionales, fonoaudiólogos, neuropsicólogos, psicopedagogas, musicoterapeuta, rehabilitadora visual y psicólogos). El programa constaba de tres etapas: (1) evaluación inicial y planteamiento de objetivos, (2) tratamiento y re-evaluaciones periódicas con ajustes de objetivos y (3) evaluación previa al alta. Los objetivos y la toma de decisiones se realizaron de manera interdiscipinaria tras un análisis exhaustivo de la situación del sujeto. En relación a la kinesiología, se realizaron 2 sesiones diarias de lunes a viernes y una sesión los sábados, con una duración de 30 a 60 minutos. La descripción completa del programa de rehabilitación se detalla en el Material Complementario. Se excluyeron aquellos sujetos con registros incompletos y quienes ingresaron con alteración de la conciencia, ya que no fue posible administrar las evaluaciones FMS y WeeFIM.
Recolección de datos
Las variables del estudio se recolectaron por medio de las historias clínicas de los sujetos y de los informes en los que se describe el tratamiento realizado y todos los resultados obtenidos de las evaluaciones. La información de interés fue volcada a la plataforma de recolección de datos MAWE® Data Collection Tools (www.mawetools.com), con acceso exclusivo a las investigadoras.
Variables
Las variables clínicos-demográficas registradas fueron edad, sexo, tipo de ACV, tiempo de evolución del ACV, hemisferio cerebral afectado (derecho, izquierdo, ambos), regiones cerebrales comprometidas, factores de riesgo [arteriopatía malformación arteriovenosa (MAV), arteriopatía no MAV, enfermedad cardíaca, otras comorbilidades], compromiso motor (hemiparesia derecha, hemiparesia izquierda, cuadriparesia), tono muscular (hipotonía, hipertonía, ataxia, sin alteración del tono) y compromiso del rango de movimiento articular.
Las variables de resultado registradas fueron la independencia y movilidad funcional. La independencia funcional es la capacidad que poseen las personas para realizar las actividades de la vida diaria (AVD) sin supervisión, dirección o asistencia personal activa. Fue evaluada por medio de la WeeFIM al ingreso y egreso del centro de rehabilitación.17 Esta escala tiene siete categorías, en orden de menor a mayor independencia: (1) asistencia total (realiza menos del 25% de la actividad), (2) máxima asistencia (realiza entre el 25 y 49% de la actividad), (3) moderada asistencia (realiza entre el 50 y el 74% de la actividad), (4) mínima asistencia (realiza más del 75% de la actividad), (5) requiere supervisión (ayudas verbales y/o pautas), (6) independencia con modificaciones (utiliza tiempo extra o adaptaciones) e (7) independencia completa (en tiempo y seguridad).
La movilidad funcional se refiere a la capacidad por la cual un individuo se mueve dentro del entorno para lograr la interacción con la familia y la sociedad día a día. Se utilizó la FMS para el registro de la movilidad funcional al ingreso y egreso del sujeto. Esta escala califica la movilidad funcional teniendo en cuenta los dispositivos de ayuda marcha que el/la niño/a podría requerir en tres distancias distintas: movilidad en 5 m (distancia corta, por ejemplo, en el hogar), movilidad en 50 m (distancia media, por ejemplo, en la escuela) y movilidad en 500 m (distancia larga, por ejemplo, en la comunidad). Esta escala otorga puntajes del 1 al 6 para cada distancia. Cada puntaje representa lo siguiente: (1) usa silla de ruedas, (2) usa caminador o andador, (3) usa bastones canadienses, (4) usa bastones, (5) es independiente en superficies niveladas o (6) es independiente en todas las superficies.18
Otras variables que se registraron fueron el tiempo de internación, el cuadro motor al alta y el equipamiento requerido al egreso para el desplazamiento (ortesis, bastón, andador y/o silla de ruedas).
Consideraciones éticas
El desarrollo y la conducción de esta investigación se ajustan con los valores éticos fundados en el respeto por la dignidad de las personas, el bienestar y la integridad física y mental de quienes participan en ella según lo establece la Guía de Investigaciones en Salud (Resolución 1480/2011) y las pautas éticas internacionales para la investigación relacionada con la salud de seres humanos, elaboradas por el Consejo de Organizaciones Internacionales de las Ciencias Médicas y en colaboración con la Organización Mundial de la Salud.
Según la Resolución 1480/11 del Ministerio de Salud de la Nación, esta investigación es de bajo riesgo, considerando la relación riesgo beneficio de los principios éticos de beneficencia y no maleficencia.
Los datos fueron recolectados siguiendo la normativa de Protección de Datos Personales, artículos 2, 4-9 y 13-16 de la Ley 25.326, los cuales se refieren a la conservación de la confidencialidad de la información recabada, resguardo de la identidad y privacidad de los sujetos. Este resguardo fue garantizado en la obtención, elaboración y divulgación de los datos.
Al ingreso a la institución se les brindó a los tutores un consentimiento informado en el cual aceptaban el uso de las historias clínicas, las fotografías y los videos con el propósito de promover los conocimientos, la atención, la investigación y la educación médica. Este protocolo fue evaluado y aprobado por el Comité de Ética e Investigación del Instituto FLENI Escobar (fecha de aprobación 15/07/2022; #009/22).
Análisis estadístico
Las variables categóricas se reportaron como número de presentación y porcentaje. Las variables continuas que asumieron una distribución normal se reportaron como media y desvío estándar (DE). De lo contrario, se utilizaron mediana y rango intercuartílico (RIQ). Para determinar la distribución de las variables continuas se utilizó la prueba de Shapiro-Wilk. Se realizó estadística inferencial exploratoria para comparar los puntajes de la FMS y WeeFIM entre el ingreso y egreso. Para ello se utilizó la prueba t de Student para muestras pareadas o la prueba de los rangos con signo de Wilcoxon, según correspondiera. Se consideró significativo un valor p<0,05. Para el análisis de los datos se utilizó el software IBM SPSS Macintosh, versión 25.0 (IBM Corp., Armonk, NY, USA).
Resultados
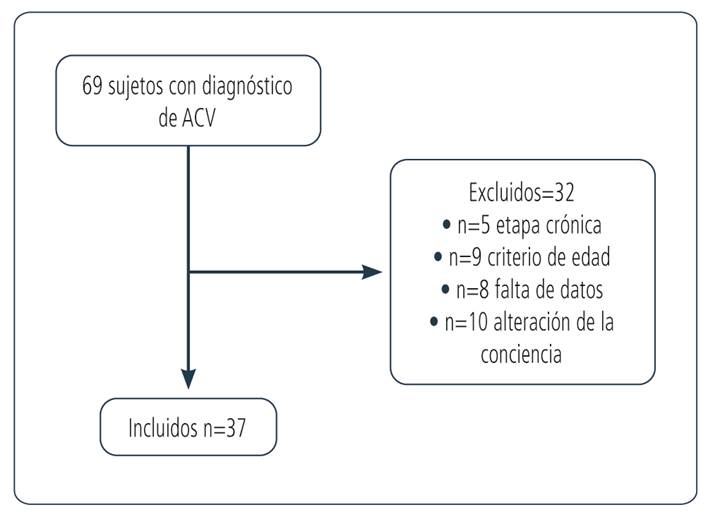
En el período comprendido entre el 1 de febrero de 2005 y el 28 de febrero de 2023 un total de 69 sujetos requirieron internación en nuestra institución para iniciar rehabilitación post ACV. Del total, 32 fueron excluidos, por lo cual la muestra quedó conformada por 37 sujetos. En la Figura 1, se presenta el diagrama de flujo de los sujetos.
Del total de sujetos, 21/37 (56,8%) fueron mujeres y la media de edad de la muestra fue 10,9 (DE 4,1) años. Al ingreso al centro de rehabilitación, la mediana del tiempo de evolución de la enfermedad fue de 30 (RIQ 19-57) días. Dentro de los factores de riesgo, 17/37 (45,9%) sujetos presentaron ACV secundario a MAV.
Las regiones cerebrales comprometidas con mas frecuencia fueron la parietal y la temporal. La primera se observó en 16/37 (43,2%) sujetos y la segunda en 15/37 (40,5%) sujetos. El hemisferio izquierdo se vio afectado en 26/37 (70,3%) sujetos, el hemisferio derecho en 9/37 (24,3%) sujetos y fue bilateral en 2/37 (5,4%) sujetos. El resto de las características al ingreso se observan en la Tabla 1.
Tabla 1 Características de los sujetos al ingreso.
| Variables | n=37 |
|---|---|
| Edad, media (DE), años | 10,9 (4,1) |
| Sexo femenino, n (%) | 21 (56,8) |
| Tipo ACV, n (%) | |
| Isquémico | 16 (43,2) |
| Hemorrágico | 21 (56,8) |
| Tiempo de evolución del ACV, mediana (RIQ), días | 30 (19-57) |
| Factores de riesgo, n (%) | |
| Arteriopatía MAV | 17 (45,9) |
| Arteriopatía no MAV | 6 (16,2) |
| Enfermedad cardíaca | 4 (10,8) |
| Otras comorbilidades | 6 (16,2) |
| Hemisferio afectado, n (%) | |
| Derecho | 9 (24,3) |
| Izquierdo | 26 (70,3) |
| Ambos | 2 (5,4) |
| Compromiso motor, n (%) | |
| Hemiparesia derecha | 23 (62,2) |
| Hemiparesia izquierda | 11 (29,7) |
| Cuadriparesia | 6 (16,2) |
| Tono muscular, n (%) | |
| Hipotonía | 17 (45,9) |
| Hipertonía | 14 (37,8) |
| Ataxia | 3 (8,1) |
| Sin alteración | 3 (8,1) |
| Compromiso del ROM, n (%) | 4 (10,8) |
ACV: accidente cerebrovascular; MAV: malformación arteriovenosa; ROM: siglas en inglés de rango de movimiento; DE: desvío estándar; RIQ: rango intercuartílico.
En este estudio, hemos utilizado la FMS para evaluar la movilidad en diferentes distancias. Al ingreso, la mayoría de los sujetos requerían el uso de silla de ruedas: 26/37 (70,3%) para movilizarse en distancias cortas, 32/37 (86,5%) para movilizarse en distancias medias y 33/37 (89,2%) para movilizarse en distancias largas. Al egreso, y luego de una mediana de 2,8 (RIQ 1,5-3,7) meses de internación, la mayoría era independiente al menos en superficies niveladas: 29/37 (78,4%) para movilizarse en distancias cortas, 22/37 (59,4%) para movilizarse en distancias medias y 20/37 (54%) para movilizarse en distancias largas (Tabla 2). Al comparar el puntaje de la FMS al ingreso y egreso, las diferencias resultaron estadísticamente significativas en las 3 distancias (p<0,001). Al egreso, 22/37 (59,5%) sujetos requirieron al menos un dispositivo de asistencia para la marcha (n=11 ortesis, n=1 bastón, n=6 andador, n=12 silla de ruedas). En el Material Complementario, se presenta la magnitud de los cambios en las categorías de la FMS al ingreso y egreso.
Tabla 2 Cambios en la movilidad funcional (n=37).
| Variables | Ingreso | Egreso | valor p |
|---|---|---|---|
| FMS 5 metros | <0.001 | ||
| Usa silla de ruedas | 26 (70,3) | 3 (8,1) | |
| Usa un andador o caminador | 2 (5,4) | 4 (10,8) | |
| Usa bastones canadienses | 0 (0) | 0 (0) | |
| Usa bastones (1 o 2) | 0 (0) | 1 (2,7) | |
| Independiente en superficies niveladas | 6 (16,2) | 10 (27) | |
| Independiente en todas las superficies | 3 (8,1) | 19 (51,4) | |
| FMS 50 metros | <0.001 | ||
| Usa sillas de ruedas | 32 (86,5) | 12 (32,4) | |
| Usa un andador o caminador | 0 (0) | 3 (8,1) | |
| Usa bastones canadienses | 0 (0) | 0 (0) | |
| Usa bastones (1 o 2) | 0 (0) | 0 (0) | |
| Independiente en superficies niveladas | 3 (8,1) | 6 (16,2) | |
| Independiente en todas las superficies | 2 (5,4) | 16 (43,2) | |
| FMS 500 metros | <0.001 | ||
| Usa sillas de ruedas | 33 (89,2) | 17 (45,9) | |
| Usa un andador o caminador | 0 (0) | 0 (0) | |
| Usa bastones canadienses | 0 (0) | 0 (0) | |
| Usa bastones (1 o 2) | 0 (0) | 0 (0) | |
| Independiente en superficies niveladas | 3 (8,1) | 5 (13,5) | |
| Independiente en todas las superficies | 1 (2,7) | 15 (40,5) |
Los datos numéricos expresan recuentos y porcentajes (%). FMS: siglas en inglés de escala de movilidad funcional.
De los 26/37 (70,3%) sujetos que al ingreso utilizaban silla de ruedas para movilizarse en distancia cortas, al egreso 3/26 (11,5%) la continuaron utilizando y 19/26 (73%) lograron una marcha independiente sin ayuda marcha. En las distancias largas, 33/37 (89,2%) sujetos requerían al ingreso silla de ruedas y al egreso 17/33 (51,5%) la continuaron utilizando y 16/33 (48,4%) alcanzaron una marcha independiente sin ayuda marcha. En la Tabla 3, se observa el cambio del requerimiento de ayuda marcha en todas las distancias. Para facilitar la interpretación, los 6 niveles de la FMS fueron agrupados en 3 categorías: 1 (silla de ruedas), 2-4 (independientes con ayuda marcha) y 5-6 (independientes sin ayuda marcha).
Tabla 3 Cambios del requerimiento de ayuda marcha en todas las distancias según la FMS.
| Ingreso | 5 metros | 50 metros | 500 metros | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2-4 | 5-6 | total | 1 | 2-4 | 5-6 | total | 1 | 2-4 | 5-6 | total | ||
| Egreso | 1 | 3 | 0 | 0 | 3 | 12 | 0 | 0 | 12 | 17 | 0 | 0 | 17 |
| 2-4 | 4 | 1 | 0 | 5 | 3 | 0 | 0 | 3 | 0 | 0 | 0 | 0 | |
| 5-6 | 19 | 1 | 9 | 29 | 17 | 3 | 2 | 22 | 16 | 3 | 1 | 20 | |
| total | 26 | 2 | 9 | 37 | 32 | 3 | 2 | 37 | 33 | 3 | 1 | 37 | |
Los 6 niveles de la FMS fueron agrupados en 3 categorías: 1 (silla de ruedas), 2-4 (independientes con ayuda marcha) y 5-6 (independientes sin ayuda marcha).FMS: siglas en inglés de escala de movilidad funcional.
En la Figura 2, se presenta el diagrama de cajas con los valores de ingreso y egreso de la WeeFIM, herramienta utilizada para evaluar la independencia funcional. La mediana del puntaje de la WeeFIM fue de 46 (RIQ 35,7-55) al ingreso y de 85,7 (RIQ 74,1-95,1) al egreso [mediana de cambio 32,5 (RIQ 19-45,8) puntos; p<0,001].
Discusión
Las actividades y la participación en sujetos pediátricos en la etapa subaguda de un ACV es un tema de gran interés en la literatura, aunque no ampliamente estudiado.10,13,15 En nuestro estudio, la independencia y movilidad funcional al ingreso determinó que los sujetos requerían asistencia para las AVD y equipamiento para desplazarse. Esto se justifica en el bajo puntaje observado en la WeeFIM (<50%) y en que la mayoría de los sujetos (>70%) eran usuarios de silla de ruedas en las distancias evaluadas con la FMS. Estos valores son similares a los reportados en un estudio donde se evidenció mayor dependencia al ingreso.15)
Casi la mitad de nuestra muestra presentó MAV como factor de riesgo. Esta tasa coincide con las reportadas en estudios realizados en Argentina10 y en otros países.19,20,21 En comparación con la población adulta, la presentación clínica más frecuente de la MAV en niños es la hemorragia.22 Un factor que podría explicar la baja actividad y participación al ingreso sería el mayor porcentaje de ACV hemorrágico (>50%). Según la literatura, este tipo de ACV genera mayores complicaciones que agravan el cuadro clínico, ya sea por hipertensión endocraneana, hematoma intraparenquimatoso, hemorragia subaracnoidea, entre otras.10,13
Al egreso del centro de rehabilitación, entre el 40-50% de los sujetos lograron la marcha independiente en todas las superficies y distancias evaluadas. Se observó mayor ganancia en los niveles de la FMS en las distancias cortas, en comparación con las distancias largas en las que casi la mitad de los sujetos que utilizaban silla de ruedas al ingreso continuaron requiriéndola. Esto puede explicarse porque presentaban un patrón de marcha que dificultaba el recorrido de distancias largas y se decidió indicar silla de ruedas. Estas decisiones se justifican porque consideramos que el abordaje de sujetos con patologías subagudas debe favorecer la recuperación del funcionamiento motor y no fomentar la compensación.23 En esta etapa subaguda, por medio de la plasticidad neuronal, se busca alcanzar el patrón típico perdido a través de la repetición de la correcta activación muscular y así lograr la integración.23,24 Por otro lado, para que la marcha sea una alternativa de movilidad comunitaria, hay otros factores determinantes, como la velocidad de marcha, la resistencia y el equilibrio, que impactan en la capacidad de lograrla de manera segura. Por tal motivo, los sujetos pueden no lograr la marcha independiente y requerir una silla de ruedas, especialmente en distancias largas.25
En cuanto al uso de dispositivos de ayuda marcha, el andador no fue prescrito con mayor frecuencia. Esto puede justificarse porque la mayoría presentaba una hemiparesia como compromiso motor, lo que determina el uso de ambos miembros superiores para realizar el agarre del andador. Por otro lado, el uso del bastón como ayuda marcha imposibilita la carga de peso simétrica, genera cambios en la activación muscular y altera los ángulos articulares.23,26 Por tal motivo, no es una indicación habitual en nuestra práctica clínica diaria. Sin embargo, la ortesis para miembro inferior fue el dispositivo más indicado en los sujetos. La literatura recomienda el uso de ortesis de tobillo y pie, ya que puede mejorar el equilibrio, la velocidad de marcha, la cadencia y longitud de la zancada en sujetos con ACV, además de facilitar la dorsiflexión del pie durante la fase de balanceo de la marcha.25,27
Al egreso, el porcentaje de independencia funcional en la WeeFIM aumentó un 32%. De igual manera, otras investigaciones han identificado mejoras en la independencia funcional luego del período de rehabilitación.15,25 Esto podría explicarse en cambios en el cuadro motor del sujeto y en su capacidad para colaborar en las AVD. Al ser más independiente respecto a la marcha y requerir menos dispositivos de ayuda marcha, podría colaborar más en actividades de movilidad y transferencias.
Cabe resaltar la importancia de la rehabilitación en los primeros 6 meses posteriores al ACV, ya que en esta etapa se produce mayor recuperación.6,7 La rehabilitación con un abordaje interdisciplinario favorece al sujeto, ya que cada profesional aporta desde su área específica.28 Además, los protocolos de rehabilitación de dosis altas de entrenamiento posiblemente inducen cambios plásticos estructurales, así como una reorganización de las redes neuronales29, un aumento de la excitabilidad cortical y una mejora de la función y del uso motor.30,31 Si bien es conocido el importante rol de la rehabilitación, existen otros factores que condicionan la mejora de los pacientes ajenos a la rehabilitación32: la recuperación espontánea6 y la resolución de mecanismos intrínsecos, como el edema, la restauración de la excitabilidad neuronal, entre otros.33
Como principales limitaciones de este estudio, podemos mencionar el diseño retrospectivo, que explica la falta de registro de variables que podrían ser de gran interés. Por ejemplo, hubiera sido interesante conocer el compromiso cognitivo, como en el estudio de Jung et al. en el que resultó ser un predictor para la adquisición de la marcha a los 6 meses posteriores al episodio.34 Por otro lado, el registro del equilibrio estático y dinámico en sedestación, bipedestación y marcha podría relacionarse con la estabilidad del tronco35, ya que el control de tronco es un requisito indispensable para iniciar la marcha y evaluado en los primeros meses tiene un valor predictivo para la adquisición de la marcha luego de un ACV.24 En segundo lugar, la profundidad del análisis estuvo limitada a las mediciones disponibles, por lo que un registro prospectivo y un seguimiento a largo plazo podrían aportar mayor conocimiento sobre el impacto de la rehabilitación en las actividades y la participación de esta población. En tercer lugar, al no contar con escalas específicas para ACV en pediatría que evalúen la movilidad en distintos entornos, se utilizó la FMS que fue validada en niños de 4 a 18 años con diagnóstico de parálisis cerebral.18 La WeeFIM está validada para población pediátrica, pero tampoco es una escala específica de esta patología.36,37 Finalmente, y no por ello menos importante, el diseño metodológico del estudio no permite establecer una relación causa-efecto entre la mejora de la funcionalidad y la rehabilitación. Existen muchos factores ajenos al tratamiento que podrían explicar los resultados terapéuticos observados.33
Más allá de las limitaciones, este estudio también tiene fortalezas. En primer lugar, hasta la actualidad no existen estudios realizados en nuestro país sobre la evolución de la funcionalidad en niños con ACV. En el mundo se trata de una temática relevante y una patología que está en aumento en esta población4, por lo que es necesario aportar a la comunidad científica datos argentinos. Por otro lado, si bien el tamaño muestral podría considerarse pequeño, se obtuvieron datos completos de 37 sujetos, considerando la baja prevalencia de esta enfermedad en la población pediátrica.5,15,38
Nuestros resultados son la base para que futuros estudios investiguen subgrupos de sujetos con el propósito de precisar objetivos, optimizar recursos y maximizar los beneficios de la rehabilitación neurológica. Desde una perspectiva clínica, esta investigación nos permitió reflexionar sobre la importancia de la rehabilitación y del trabajo interdisciplinario planificado. Este estudio podría aportar información a la hora de plantear objetivos de tratamiento y que estos sean alcanzables, claros y precisos, a mediano y largo plazo.
Conclusión
En esta muestra de niños con ACV subagudo internados en un centro de rehabilitación, se observaron cambios favorables en la funcionalidad luego de un programa de rehabilitación interdisciplinario e intensivo. Si bien el diseño no permite establecer causalidad, se registró mejoría en el porcentaje de independencia funcional y en la adquisición de la marcha independiente en todas las distancias. Se observó mayor ganancia en los niveles de la FMS en las distancias cortas, en comparación a las distancias largas.