Introducción
La presencia de una lesión perirradicular es generalmente la consecuencia de una pulpa necrótica e infectada por la invasión de bacterias, sus toxinas y subproductos en el interior del sistema de conductos radiculares (SCR). 1 Esta condición provoca una respuesta inflamatoria que se produce como una reacción de defensa por parte de los tejidos perirradiculares (periodonto y hueso). 3 Estas reacciones son generalmente de tipo granulomatoso (granulomas perirradiculares) y se encuentran reguladas por el sistema inmunológico, a través del cual un complejo mecanismo de interacción celular, en conjunto con otros factores, es capaz de responder a la presencia de un antígeno que ingresa en el SCR. 4 En estos casos, el tratamiento indicado consiste en la limpieza y desinfección del SCR y su posterior obturación, tras lo cual se produce generalmente la reparación de la lesión. 7
En los casos en los que no es posible eliminar la infección intraconducto, la lesión suele persistir. 4 Sin embargo, existen otros factores que pueden incidir en la persistencia de la lesión, como la presencia de conductos laterales o accesorios no tratados, ramificaciones, deltas e intercomunicaciones, 8 es decir, áreas difíciles o imposibles de acceder durante las fases de instrumentación e irrigación. Si a pesar del tratamiento endodóntico la lesión persiste, aún luego de un tiempo posoperatorio prudencial, el retratamiento es el procedimiento indicado. Otros factores localizados en los tejidos perirradiculares pueden también interferir con el proceso reparativo de la lesión, tales como la actinomicosis, 9 reacciones a cuerpo extraño, 10 cristales de colesterol (CRCo) 11 y granulomas o quistes con alto contenido de CRCo. En estos casos, el retratamiento complementado por la cirugía periapical es la indicación más adecuada. 12
El objetivo de la presente revisión fue analizar las causas que condicionan la persistencia de lesiones perirradiculares luego de un tratamiento endodóntico primario y/o retratamiento.
Desarrollo
A continuación se detallan las posibles causas de las lesiones perirradiculares persistentes.
Infección intraconducto. Una de las causas más importantes que favorecen la falta de resolución de las patologías perirradiculares de origen endodóntico es la infección del SCR, o su persistencia aún luego del tratamiento. 13 En estos casos, las bacterias pueden alojarse entre el material de obturación y la pared dentinaria, y también en el interior de los túbulos dentinarios, especialmente en el tercio apical (fig. 1). En su histórico trabajo de 1990, Nair et al. 13 , y posteriormente Fouad et al. 1 en 2005, observaron que la mayor parte de las piezas dentarias tratadas con lesiones perirradiculares persistentes (LPP) contenían una carga bacteriana importante. Nair et al. 14 observaron estos mismos resultados en una serie de tratamientos realizados en primeros molares inferiores, donde comprobaron que el 87,5% de los mismos contenían biofilms bacterianos residuales en localizaciones de difícil acceso, como las áreas de reabsorción dentinaria interna, conductos accesorios, intercomunicaciones, istmos, o cul-de-sacs.
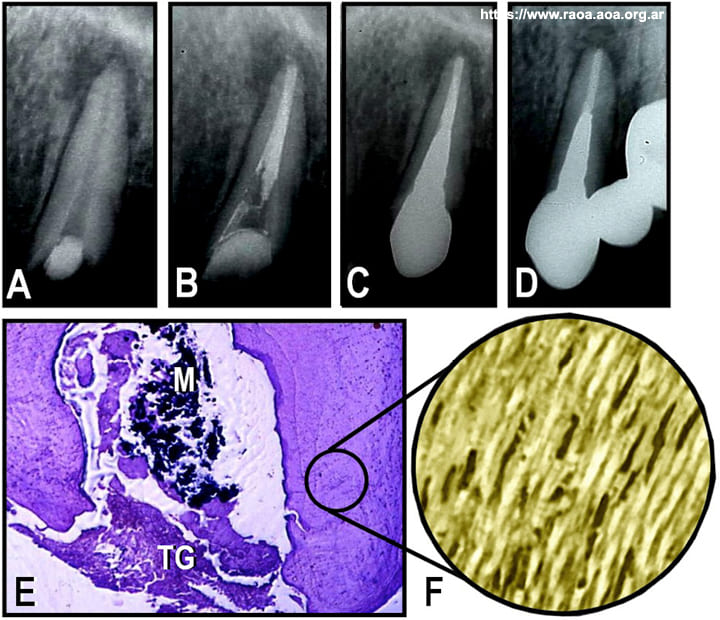
Figura 1 A: Radiografía preoperatoria de un canino superior con necrosis pulpar y lesión perirradicular. B: Radiografía posoperatoria inmediata. C: Radiografía de control 6 meses después de la operación en la que se evidencia que lesión no ha variado de tamaño. Se observa un perno muñón metálico cementado. D: A los 30 meses, se observa la persistencia del área radiolúcida. El paciente manifiesta dolor en la zona perirradicular. E: Sección histológica del ápice dentario removido mediante la cirugía periapical. Se observan restos del material de obturación (indicados con la letra M) y el tejido granulomatoso (indicado con TG). (Hematoxilina y eosina; Magnificación original X100). F: En otra sección histológica del mismo sector se observa un mayor aumento de la zona del círculo negro de la figura 1E. Se evidencia la persistencia de colonias bacterianas en los conductillos dentinarios. (Coloración de Brown & Brenn modificada; magnificación original X1000).
Los biofilms están compuestos por agregados de células microbianas, encerradas en una matriz propia y adheridas a una superficie. En el SCR los biofilms son estructuras polimicrobianas complejas, formadas por bacterias que invaden el espacio del conducto radicular y que solían ser identificadas como células adheridas a las superficies dentinarias (fig. 2).
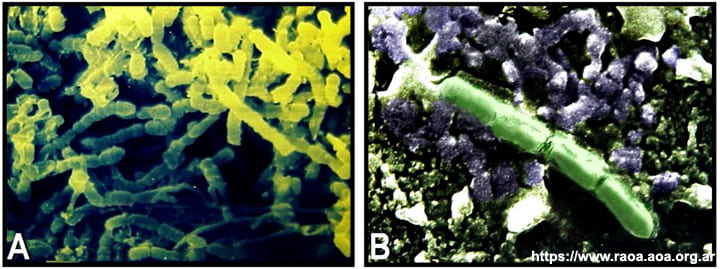
Figura 2 Imágenes de biofilms bacterianos adheridos a la superficie dentinaria en los conductos radiculares infectados. Microscopía electrónica de barrido: A: X500. B: X1500.
Luego de la introducción de técnicas más avanzadas de microscopía y biología molecular, se comprobó que eran la forma dominante de vida bacteriana en el SCR, constituyendo de esta manera la fuente principal de las infecciones endodónticas persistentes. 1
Por lo tanto, son factores determinantes para la presencia de lesiones perirradiculares que no se reparan luego de un tratamiento endodóntico. Los conductos radiculares tratados suelen contener bacterias residuales que pueden persistir durante largos períodos de tiempo, aún bajo condiciones adversas tales como la reducción de nutrientes y la acción antibacteriana de las soluciones irrigantes (SLi), como las especies Gram positivas. 15 El empleo de SLi y de una medicación intraconducto producen una simplificación de la microbiota presente en los conductos radiculares infectados, ya que solo permiten la persistencia de las bacterias más resistentes. 17 Sin embargo, el efecto de resiliencia, es decir, la capacidad de recuperación de la microbiota restante, promueve una adaptación ecológica posterior a su reducción inicial. 17 En los casos de LPP, la flora bacteriana remanente en los conductos radiculares suele presentar una prevalencia para las bacterias facultativas anaerobias Gram positivas. 17 Entre ellas se destaca el E. faecalis, una bacteria muy resistente a la acción antimicrobiana de las SLi y la mayoría de los materiales que se utilizan habitualmente como medicación intraconducto, incluso aquellos con un pH superior a 11.0.14,16. 17 Asimismo, es frecuente la presencia de levaduras como Candida albicans que, tanto en el interior del SCR como cuando son impulsadas accidentalmente a los tejidos perirradiculares durante la instrumentación (fig. 3), cumplen también un rol importante en la persistencia postratamiento de las lesiones perirradiculares. 5
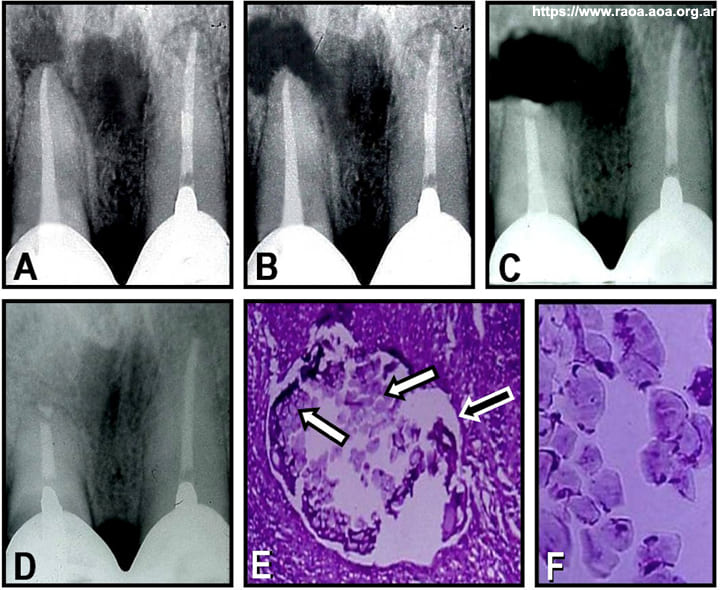
Figura 3 Tratamiento endodóntico realizado a través de una corona en el incisivo central superior derecho con lesión perirradicular. A: Radiografía posoperatoria inmediata.B: A los 9 meses, la lesión aumentó de tamaño y se observa bien circunscripta al ápice dentario. C: Radiografía posoperatoria luego de la remoción quirúrgica de la lesión. D: Radiografía de control a 2 años de la operación, donde se observa la reparación perirradicular. E: Sección histológica del material removido durante la cirugía. Se observa un tejido granulomatoso y una acumulación bacteriana compatible con infección por C. albicans (indicados con las flechas blancas), rodeado por una cápsula fibrosa irregular (indicada con la flecha negra). (Hematoxilina y eosina; magnificación original X300). F: Se observa un mayor aumento de las colonias bacterianas observadas en figura 3E. (Hematoxilina y eosina; magnificación original X850).
Es importante considerar que, durante el tratamiento, la fase de instrumentación por sí sola no resulta suficiente para obtener una debridación y desinfección adecuadas del SCR. 20 Los procedimientos de irrigación por medio de agentes químicos con propiedades antimicrobianas, como el hipoclorito de sodio (NaOCl) en diferentes concentraciones y el gluconato de clorhexidina al 2%, 20 o bien el empleo de una medicación intraconducto y de materiales de obturación con propiedades antibacterianas, constituyen un medio efectivo para la reducción del biofilm bacteriano, pero no para su eliminación total. 20 Al-Ahmad et al. 24 informaron que no fue posible eliminar (in vitro) cepas de bacterias removidas de conductos radiculares infectados y cultivadas en contacto con antibióticos como ampicilina, azitromicina, doxiciclina, clindamicina o metronidazol, y en ese sentido, se ha sugerido que las cepas que persisten luego del tratamiento desempeñan un papel importante en la falta de resolución de las lesiones perirradiculares. 25 Con respecto a esto, las bacterias anaerobias facultativas Gram positivas de los géneros Streptococcus, Lactobacillus y Actinomyces que son afectadas por las SLi durante la preparación de los conductos radiculares o con la medicación intraconducto, suelen recuperar su potencial patogénico con mucha frecuencia mediante el proceso de resiliencia previamente mencionado. 26
La complejidad morfológica del SCR y las investigaciones precedentes explican los motivos por los cuales los procedimientos de instrumentación, irrigación y desinfección resultan insuficientes para eliminar la totalidad de la carga bacteriana intrarradicular. Recientemente, una serie de investigaciones en las tación e irrigación confirmaron que, hasta el momento, e independientemente del tipo de instrumento o del procedimiento empleado, resulta imposible eliminar la totalidad de las bacterias y otros tipos de contaminantes del interior del SCR. 27
Actinomicosis. La actinomicosis periapical (AMP) es una lesión crónica de tipo granulomatoso considerada un subgrupo de una patología conocida como actinomicosis cervical. Esta lesión es progresiva, se presenta en la región de cabeza y cuello y es causada por una bacteria anaeróbica comensal llamada Actinomices israelii, que coloniza en el medio oral, en el colon y en la vagina. También son causantes de la AMP el A. naeslundii, A. odontolyticus, A. viscosus o el A. radicidentis, 33 aunque con menor frecuencia. En el medio oral, el agente A. israelii se encuentra en la placa bacteriana, en el surco gingival y en las lesiones cariosas. 34 A pesar que su prevalencia es menor del 5%, 34 la AMP es considerada como uno de los factores contribuyentes más importantes para la perpetuación de las lesiones perirradiculares postratamiento. En las infecciones endodónticas, su localización es generalmente extraradicular, aunque también es posible localizar la bacteria en el interior del SCR infectado, y es por esto que se lo ha considerado como portal de entrada principal para el desplazamiento de la bacteria hacia los tejidos perirradiculares. 9 Si bien la AMP se encuentra relacionada a los tratamientos y retratamientos endodónticos con historias repetidas de fracaso, también es posible detectar esporádicamente esta patología en casos que no han recibido tratamiento endodóntico. 5 En el examen clínico, la lesión presenta tumefacción y drenaje purulento a través de una fístula, que en ocasiones puede tener salida extraoral y reabsorción ósea de grandes dimensiones. Las colonias de A. israelii, A. viscosus o A. odontolyticus aparecen en forma de gránulos o partículas azufradas (frecuentemente calcificadas) contenidas en el exudado purulento. Con respecto a su incidencia, Esteves et al. 34 detectaron una mayor prevalencia de la AMP en personas del género femenino, especialmente en el sector anterior del maxilar inferior. Sin embargo, estas observaciones difieren con lo informado por Hirshberg et al. 35 , quienes obtuvieron que la mayor prevalencia de la lesión aparecía en personas del género masculino, y con mayor frecuencia en el maxilar superior. Cuando se desarrolla en el maxilar inferior, se encuentra generalmente asociada a la actinomicosis cervical. 35
En el examen radiográfico, las lesiones provocadas por Actinomices israelii presentan bordes bien definidos. 34 Por otra parte, presentan un mayor tamaño en comparación con lesiones provocadas por otros agentes etiológicos. 36 En el examen histológico se puede reconocer al A. israelii por presentar filamentos múltiples de disposición radial que terminan en forma de hifas, con respuesta positiva a la coloración ácido periódico Schiff, y porque las bacterias se encuentran rodeadas por un conglomerado de células inflamatorias crónicas y escasos polimorfonucleares neutrófilos. Las colonias actinomicóticas también se encuentran asociadas a los quistes de origen dentario, y en ese sentido, se ha demostrado que el aumento del número de colonias de Actinomices contribuye al aumento de tamaño de la lesión. 34 En los casos de tratamientos endodónticos con LPP, especialmente aquellos que presentan lesiones actinomicóticas, el tratamiento indicado es el retratamiento, el curetaje cuidadoso del área afectada y la prescripción de antibióticos de amplio espectro; tras lo cual, la evolución de la lesión suele ser favorable.
Reacción a cuerpo extraño. Otra de las causas de localización extraradicular responsables de las lesiones perirradiculares persistentes son las reacciones a cuerpo extraño (RCE). Las RCE son producidas por la extrusión accidental de materiales de obturación, restos de conos de papel absorbentes, restos de alimentos o cualquier otro tipo de elemento extraño en los tejidos perirradiculares. 10 Estas reacciones son generalmente asintomáticas, razón por la que estas lesiones suelen detectarse solo ocasionalmente en una radiografía de control. Esporádicamente, puede producirse una reagudización del proceso inflamatorio crónico que suele rodear al elemento extraño, y en esos casos, el paciente puede consultar al clínico a causa del dolor. Los conos de gutapercha, selladores endodónticos o conos de papel accidentalmente sobreobturados suelen inducir una respuesta localizada de los tejidos perirradiculares, caracterizada por la presencia de macrófagos que intentan fagocitar y destruir el elemento que resulta extraño al organismo (fig. 4). Al mismo tiempo, la extrusión de materiales a través del foramen puede también producir bacterias y/o restos pulpares infectados. El proceso de RCE se desarrolla en varias etapas consecutivas:
1. Absorción de proteínas, 2. Inflamación (reclutamiento de macrófagos y formación de células gigantes multinucleadas, 3. Formación de tejido fibroso envolvente.
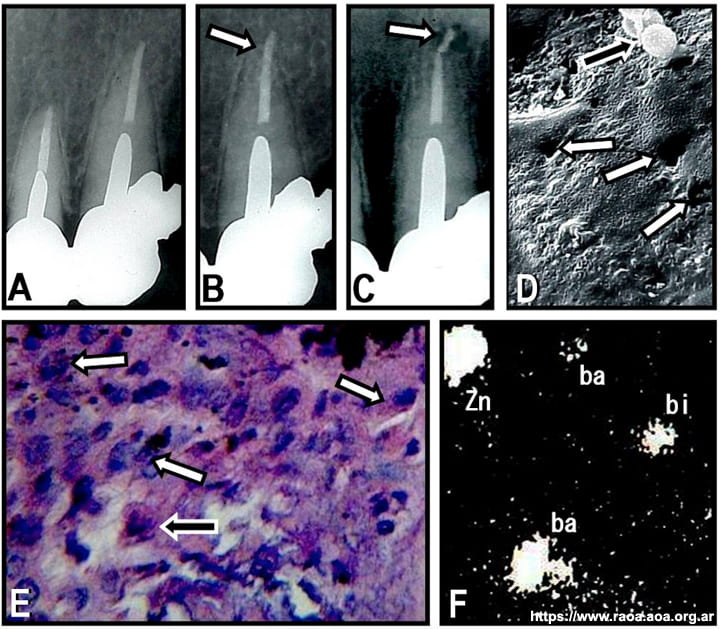
Figura 4 Sobreobturación accidental con cono de gutapercha y sellador en un canino superior izquierdo. A: Radiografía tomada a los 6 meses posoperatorios. Se observa un perno metálico intraconducto y una restauración protética. B: En el control de 18 meses, se puede observar una pequeña zona radiolúcida rodeando al cono (indicada con la flecha). C: Radiografía a los 4 años posoperatorios. La zona radiolúcida presenta mayor tamaño y el paciente manifiesta dolor localizado en la zona periapical. Nótese que el cono de gutapercha se ha separado del resto de la obturación (indicado con la flecha), y presenta pérdida de masa. Se realizó curetaje de la lesión y remoción del fragmento de cono sobreobturado. D: Microfotografía de la superficie del fragmento de gutapercha. Se evidencia la presencia de áreas donde se produjo pérdida de material (indicadas con las flechas blancas) y la presencia de bacterias (indicadas con la flecha negra). (Microscopía electrónica de barrido; magnificación original X300). E: Sección histológica del tejido granulomatoso removido. La imagen es compatible con una reacción a cuerpo extraño. Se observan numerosas partículas que están siendo fagocitadas por macrófagos (indicadas con flechas blancas). La flecha negra está indicando la formación de una célula gigante multinucleada. (Hematoxilina y eosina; magnificación original X1000). F: Microfotografía compuesta del escaneo elemental con microsonda electrónica realizado en diferentes secciones de la lesión, donde se detecta la presencia de zinc (Zn), bario (Ba) y bismuto (Bi), tres de los componentes habituales de los conos de gutapercha y los selladores a base de óxido de cinc-eugenol.
En todo momento, la topografía de la superficie del cuerpo extraño y su comportamiento fisicoquímico influye significativamente en el tipo y extensión de la reacción de los tejidos. 37
1. Absorción de proteínas. Una vez que el material extraño es reconocido como patógeno por los tejidos perirradiculares, las proteínas presentes en el plasma sanguíneo son absorbidas en la superficie del material, se liberan factores de crecimiento, citoquinas y factores quimiotácticos, cuya función es primordial para la atracción y posterior adhesión de macrófagos a la superficie del cuerpo extraño, para la formación de células gigantes multinucleadas y finalmente la formación de un coágulo de fibrina. 37
2. Inflamación. A causa de la interacción entre el cuerpo extraño y la sangre se produce la activación del complemento, 39 reacción que inicia la respuesta del organismo mediante la infiltración de células inflamatorias. 38 Luego de una breve etapa aguda, la inflamación deriva hacia la cronicidad. Los macrófagos son atraídos por la acción de los factores de crecimiento y las proteínas, y se adhieren al fibrinógeno y fibronectina para activar el proceso de fagocitosis. En algunas ocasiones, los macrófagos no pueden fagocitar por si solos partículas extrañas de gran tamaño, por lo que se fusionan entre sí para formar células con mayor capacidad de fagocitosis, llamadas células gigantes de cuerpo extraño o células gigantes multinucleadas, por presentar un número importante de núcleos en su citoplasma (fig. 5). 38
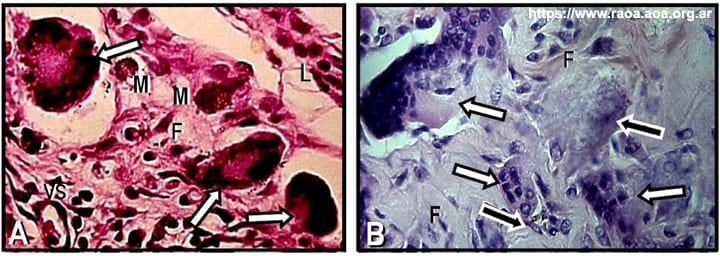
Figura 5 A: Células gigantes multinucleadas (indicadas con las flechas blancas) y macrófagos fagocitando partículas de material extraño (indicados con la M). F: fibroblasto; L: Linfocito; VS: Vaso sanguíneo. (Hematoxilina y eosina; Magnificación original X1000). B: Células gigantes multinucleadas (indicadas con las flechas blancas) rodeando cuerpos extraños (indicados con las flechas negras). (Hematoxilina y eosina; magnificación original X400).
3. Formación de tejido fibroso. En esta etapa, los fibroblastos y las células endoteliales son atraídos hacia la superficie del material extraño, sobre la que se deposita colágeno y otras proteínas para la formación de un tejido fibroso denso y compacto, con el objetivo de aislar al material extraño del medio circundante. Cuando el material resulta difícil de eliminar, la acción aislante del tejido fibroso suele fracasar, resultado que es potenciado por la liberación continua de factores proinflamatorios.
La indicación de tratamiento para los casos de reacción a cuerpo extraño que presentan sintomatología clínica es la cirugía periapical. En ocasiones, se requiere realizar un relleno de la cavidad quirúrgica con algún tipo de substituto óseo que tenga la capacidad de inducir la neoformación de tejido calcificado. 40 Feigin y Shope 41 sugieren que el uso complementario de plasma rico en plaquetas tiene un alto poder regenerativo ya que libera factores de crecimiento, estimula la angiogénesis y mejora el proceso cicatricial.
Cristales de colesterol (CRCo). El colesterol es un lípido de la familia de los esteroides que se encuentra presente con mucha frecuencia en los tejidos perirradiculares. Es precursor de los ácidos biliares, de las hormonas esteroideas y de la pro vitamina D3. 5 Es insoluble en agua y se transporta por vía sanguínea conjuntamente con las lipoproteínas. El exceso de colesterol en sangre juega un rol preponderante como factor etiológico de la ateroesclerosis. 42 Cuando los CRCo actúan como factor etiológico de LPP se los encuentra generalmente en forma de grandes acumulaciones, en granulomas y quistes radiculares. 43 Los cristales se forman a partir del colesterol liberado durante la destrucción y desintegración de los eritrocitos y de las células epiteliales y también a partir de los lípidos plasmáticos circulantes. La acumulación de CRCo estimula la aparición de macrófagos y células gigantes multinucleadas rodeando los cristales en una típica reacción a cuerpo extraño.
En las secciones histológicas, la imagen de los cristales se presenta en forma de espacios vacíos y alargados de gran tamaño que corresponden a los espacios que ocupaban antes de ser sometidos al procesamiento histológico. Esto ocurre porque los CRCo se disuelven por la acción de los reactivos que se utilizan regularmente durante la preparación de las muestras, ya que todos ellos son solventes de grasas. En un trabajo experimental, Nair et al. 44 implantaron CRCo en animales de laboratorio y observaron que los macrófagos y células gigantes eran incapaces de fagocitar los cristales a causa de su gran tamaño, que oscila aproximadamente entre 400 μm de largo y entre 20 y 30 μm de espesor. En ese sentido, se ha sugerido que la exposición de las células macrofágicas a los CRCo, al resultar imposible la fagocitación, produce la liberación de factores proinflamatorios que afectan negativamente al proceso de reparación postratamiento, estimulando de esta forma la reabsorción ósea y manteniendo la persistencia de la lesión. 45
Quistes radiculares. Los quistes radiculares u odontogénicos constituyen un tipo de patología crónica, con una cavidad cerrada y tapizada por un epitelio escamoso estratificado no queratinizado. En raras ocasiones, el epitelio puede ser de tipo cilíndrico ciliado, a causa de una posible migración de células del seno maxilar, de la cavidad nasal o a causa de la metaplasia del mismo epitelio escamoso estratificado. 46
La acumulación de CRCo puede observarse con mucha frecuencia en el caso de quistes radiculares inflamatorios (fig. 6). En el examen microscópico con luz polarizada del fluido extraído de la cavidad quística mediante aspiración, los cristales aparecen en forma de partículas birrefringentes con tono amarillento azulado o verdoso, motivo por el cual se ha sugerido que este tipo de examen puede ser utilizado con fines de diagnóstico. 43 Sin embargo debería tenerse en cuenta que una gran proporción de quistes radiculares pueden no contener CRCo (Zmener et al. 2020; datos no publicados del autor), razón por la cual la presencia de cristales en el fluido quístico no debería ser tomado como dato único para el diagnóstico de la lesión. En un estudio de 105 biopsias de quistes radiculares, Arwill et al. 47 detectaron la presencia de CRCo en solo un 34% de las muestras.
Los cristales también pueden observarse con alguna frecuencia en quistes residuales. 47
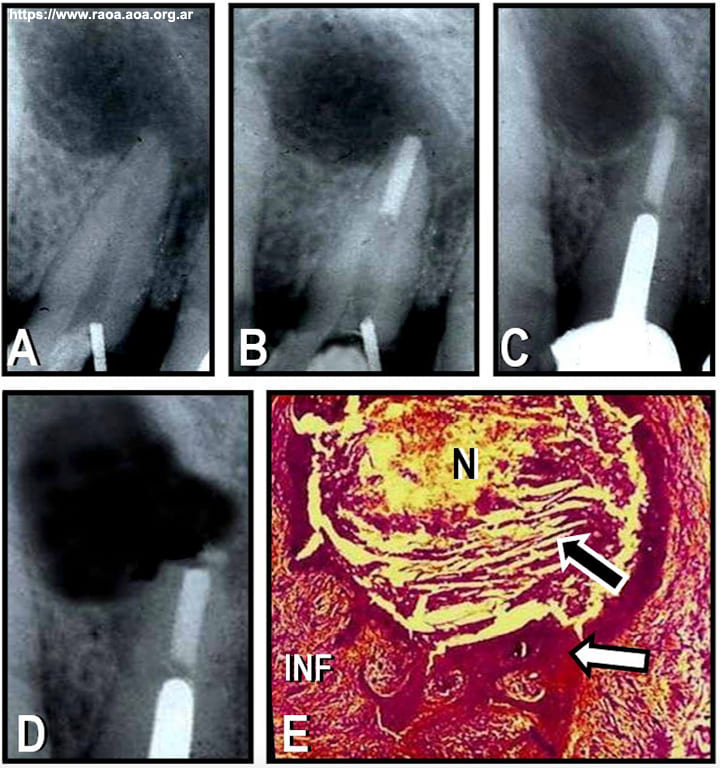
Figura 6 A: Radiografía preoperatoria de un canino superior con necrosis pulpar y lesión compatible con quiste radicular. B: Radiografía posoperatoria inmediata. El conducto fue preparado para recibir un perno intrarradicular. C: Radiografía de control a los tres años posoperatorios, la lesión ha persistido sin sintomatología. D: Radiografía inmediata luego de la cirugía periapical. E: Tras la enucleación quirúrgica, el corte histológico confirma el diagnóstico de quiste radicular. Se evidencia la presencia de cristales de colesterol en la cavidad quística (indicada con la flecha negra), tejido necrótico (indicado con la N), un epitelio engrosado y bien definido (indicado con la flecha blanca) y el tejido inflamatorio circundante (indicado con INF). (Hematoxilina y eosina, magnificación original X45).
Se ha especulado que los traumatismos o cirugías previas pueden causar micro hemorragias, que en un espacio cerrado pueden eventualmente desarrollar CRCo en el interior de la cavidad de la lesión o en sus paredes. 48 La detección de depósitos de hemosiderina en los preparados histológicos tiende a reforzar esta teoría, aunque este aspecto aún se encuentra en discusión.
Cuando se localizan en la pared de la lesión, los CRCo actúan como estímulo para el desarrollo de una reacción a cuerpo extraño. 48 Esto se observa muy frecuentemente en los dientes del sector anterior del maxilar superior. 48 La mayoría de estas lesiones son asintomáticas, por lo que es común detectarlas en exámenes radiográficos de rutina. La lesión puede presentar un gran tamaño, y como consecuencia, puede producir tumefacción, dolor, expansión de la cortical ósea y la presencia de fístula.
En general, el tratamiento endodóntico suele ser suficiente para la resolución de estas patologías, 49 especialmente cuando la lesión guarda continuidad directa con el conducto radicular o en los casos donde la cavidad quística no contiene CRCo, o los contiene en proporciones despreciables. Cuando no hay continuidad, o cuando la cavidad quística contiene gran cantidad de CRCo, la lesión suele persistir en el tiempo y en estas circunstancias el tratamiento endodóntico y eventualmente el retratamiento deben ser complementados mediante la remoción quirúrgica de la lesión.
Lesiones no inflamatorias. Con cierta frecuencia, es posible observar otro tipo de patologías localizadas en los tejidos perirradiculares, como por ejemplo queratoquistes, quistes del conducto nasopalatino y tumores benignos o malignos que no corresponden a la clasificación de lesiones inflamatorias. El tratamiento de estas lesiones siempre es quirúrgico. Cuando el examen radiográfico y/o la tomografía computarizada de haz cónico permiten detectar la presencia de una lesión sospechosa, es importante establecer un diagnóstico de la lesión previo a la cirugía. Es por esto que se ha indicado el empleo de la biopsia por punción como un procedimiento incruento, no invasivo y de gran efectividad para obtener un diagnóstico diferencial que permita determinar cuál es el tratamiento más apropiado para cada caso en particular. 51
Conclusiones
La persistencia de lesiones perirradiculares postratamiento endodóntico es un hallazgo frecuente. En base a los datos analizados en el presente informe, es posible arribar a las siguientes conclusiones:
La persistencia de colonias bacterianas en el sistema de conductos radiculares luego de su preparación, desinfección y obturación, es una de las principales causas de la persistencia de las patologías perirradiculares de origen endodóntico.
La presencia de elementos extraños en los tejidos perirradiculares, tales como infecciones actinomicóticas, restos pulpares infectados, materiales de obturación o restos de alimentos impulsados a través del foramen, cristales de colesterol en granulomas y quistes radiculares e incluso lesiones no inflamatorias, son factores causales de la perpetuación de estas patologías, aun cuando el tratamiento endodóntico original haya sido bien realizado.
En estos casos, el retratamiento por vía ortógrada por sí solo no puede aportar ningún tipo de solución, ya que el problema no se encuentra solamente en el interior del conducto. Por consiguiente, el clínico debería evaluar la conveniencia de realizar un retratamiento y complementar su acción mediante una cirugía periapical, con el objetivo de erradicar la causa que originó la persistencia de la lesión, permitiendo a los tejidos contar con las mejores condiciones para la reparación.















