El prolapso de la válvula mitral descrito por Barlow en 1963 tiene una prevalencia en las distintas cortes de un 3%1. Se define eco-cardio gráficamente por un prolapso de la válvula mitral en sístole mayor a 2 mm sobre el plano del anillo, a predominio de la valva posterior, que puede acompañarse de otras malformaciones estructurales2. Se compone de un amplio espec tro de manifestaciones clínicas, desde estadios asintomáticos hasta el desarrollo de insuficien cia cardíaca, fibrilación auricular, accidente ce rebrovascular, insuficiencia mitral grave, arrit mias ventriculares y la muerte súbita3,4. Esta enfermedad suele afectar a pacientes jóvenes, y dado que hasta estadios avanzados se encuen tran asintomáticos muchos de ellos debutan con muerte súbita o arritmias graves5,6. Además por distintos mecanismos puede devenir en deterio ro grave de la función ventricular.
A continuación, se presenta el caso de una pa ciente de 67 años que ingresó con insuficiencia cardiaca, a la cual se le diagnostica enfermedad de Barlow con deterioro grave de la fracción de eyección del ventrículo izquierdo y que durante la internación en unidad coronaria tuvo 3 episo dios de muerte súbita en contexto de taquicar dia ventricular polimorfa.
Caso clínico
Paciente femenina de 67 años que consultó al servicio de emergencias por palpitaciones. Como antecedentes clí nicos, presentaba prolapso mitral y pérdida de la visión del ojo derecho secundaria a una embolia en la arteria oftál mica. Comenzó 7 días antes con palpitaciones esporádi cas, no asociados a la clase funcional que cedían espontá neamente, los cuales el día de la consulta se mantuvieron de manera permanente por 2 horas. Al interrogatorio diri gido refiere disnea progresiva hasta clase funcional III de 6 meses de evolución. Al ingreso presentaba los siguientes signos vitales: tensión arterial de 110/60 mmHg, frecuencia cardiaca de 140 latidos por minuto, saturación de oxígeno 95% aire ambiente, frecuencia respiratoria de 20 ciclos por minuto, ingurgitación yugular, edemas 3/6 y hepatalgia. En el electrocardiograma de ingreso (Fig. 1A) se observó ritmo de fibrilación auricular a 140 latidos por minuto, eje en 60°, qrs 0,14 con imagen de bloqueo incompleto de rama iz quierda, sin alteraciones del segmento ST-T. Laboratorio: hematocrito de 42, sin leucocitosis, creatinina 0.92, natre mia de 136, kalemia de 4.3, magnesio de 1.9, NT proBnp de 12 000 pg/dL, y troponinas de 1900 ng/dL.
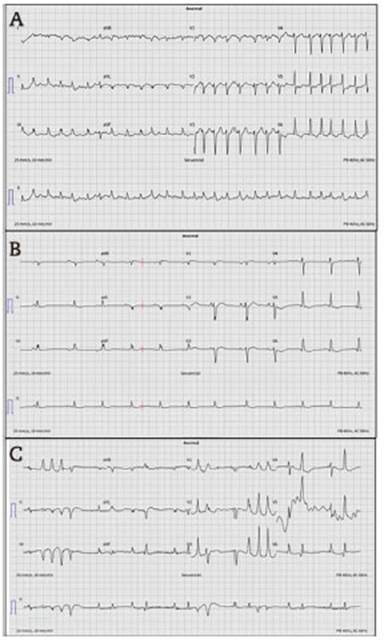
Figura 1 A: Electrocardiograma de ingreso. B: Electro-cardiograma en ritmo sinusal. C: Electrocardiograma posterior al paro. Se observan salvas de taquicardia ventricular no sostenida y morfología de bloqueo de rama derecha, con origen en el músculo papilar posterior
Se interpretó como insuficiencia cardiaca en paciente con fibrilación auricular de alta respuesta ventricular.
Durante la internación se profundizó sobre el diagnós tico etiológico.
Se realizó ecocardiograma donde se observó diámetros del ventrículo izquierdo aumentados (Fig. 2A) con dete rioro grave de la función, dilatación de aurícula izquierda severa (Fig. 2B), válvula mitral redundante con prolapso bivalvar a predominio de p (Fig. 2B, 2C), con reflujo leve e insuficiencia tricuspídea leve con presión sistólica pul monar de 28 mmHg. (Fig. 2A).
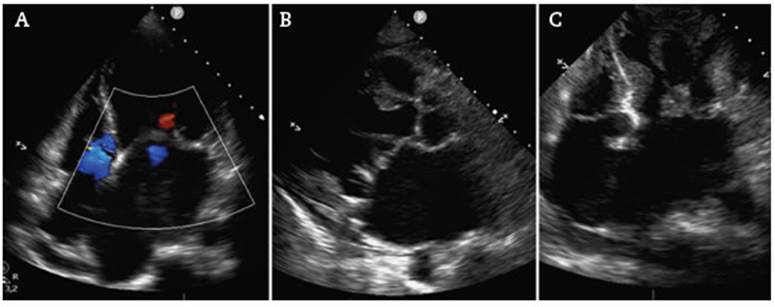
Figura 2 Ecocardiograma transtorácico. A: Vista apical cuatro cámaras con box de doppler color, se evidencia dilatación severa de aurícula y ventrículo izquierdo con degeneración mixomatosa de válvula mitral y prolapso de ambas valvas con insuficiencia mínima asociada en fin de sístole. B y C: Vista de eje largo paraesternal izquierdo y cuatro cámaras apicales. Se observa dilatación de cavidades izquierdas con válvula mitral mixomatosa, con ambas valvas engrosadas, tejido redundante, distensión de aparato subvalvular y coaptación debajo del plano anular mayor a 2 milímetros
Por deterioro grave de la función no conocido y tro poninas positivas se realizó cinecoronariografía, que no evidenció lesiones angiográficamente significativas.
Se plantearon diagnósticos diferenciales: miocarditis y taquicardiomiopatía. Las mismas fueron descartadas, dado que no presentaba características ecocardiográficas de miocarditis y en el seguimiento en ritmo sinusal no había recuperación de la función por la cual tampoco co rresponde con síndrome de taquicardiomiopatía.
Se interpretó como deterioro grave de la función ven tricular en paciente con enfermedad de Barlow.
Se realizó control de frecuencia cardíaca y balance negativo con escasa respuesta. Por tal motivo se decidió realizar ecocardiograma trans-esofágico y cardioversión eléctrica. En el ecocardiograma trans-esofágico se reva loró nuevamente la válvula mitral y la paciente presentó insuficiencia leve con prolapso similar a lo observado en el ecocardiograma transtorácico. Se realizó cardioversión eléctrica de manera exitosa (Fig. 1B).
En los ecocardiogramas, posteriores en ritmo sinusal, persistió con deterioro grave de la función ventricular.
A las 24 horas de la internación intercurrió con episo dio de paro cardiorrespiratorio, secundario a taquicardia ventricular polimorfa (Fig. 1C).
Repitió dos eventos similares a las 48 y 72 horas, todos revirtieron con maniobras de reanimación cardiopulmo nar avanzada. Por tal motivo se decidió la colocación de un cardiodesfibrilador implantable (CDI) en prevención secundaria. La paciente fue dada de alta.
Discusión
El síndrome de Barlow fue descrito por prime ra vez por Jhon Brereton Barlow en 1963. La re firió como una enfermedad congénita en la cual una o ambas valvas de la válvula mitral protru yen hacia el atrio izquierdo durante la sístole y ciertos pacientes presentan un cierre mesosis tólico y un soplo telesistólico2. Actualmente 60 años después de la descripción original conti núa generando muchas incertidumbres. Una parte menor de estos pacientes no desarrollan insuficiencia mitral con criterio de intervención, se encuentran asintomáticos por muchos años, y terminan con una muerte súbita.
Actualmente, los sobrevivientes de esta en fermedad terminan con la colocación de un CDI en prevención secundaria. Hasta el momento no contamos con un tratamiento etiológico, y tampoco existen predictores, que definan cuáles son los pacientes con mayor riesgo de desarro llar muerte súbita. Está descrito que las mujeres jóvenes con prolapso mitral y ondas T negativas en cara inferior podrían tener mayor riesgo de desarrollar taquicardia ventricular7. Se descri ben en la actualidad tres etiologías posibles de la generación de arritmia en este trastorno. La primera es la fibrosis miocárdica ubicada prin cipalmente a nivel de los músculos papilares, la pared libre y la región inferior basal del ventrícu lo izquierdo. La segunda hipótesis sostiene que existe enfermedad de las células de Purkinje, y por último la implantación alta del anillo mitral sería el foco arritmogénico en esta afección. En el primer caso, la resonancia magnética cardiaca nos aporta información dado que quizás pone de manifiesto una región plausible de ablación8.
Si bien no es una causa frecuente de muerte súbita, es una causa olvidada que afecta a pa cientes jóvenes. Otro dato a resaltar es la asocia ción entre esta enfermedad y el deterioro grave de la función ventricular. El mecanismo mayormente descrito, es que el reflujo mitral grave se asocia a dilatación auricular y ventricular. Otro mecanis mo propuesto, es el desarrollo de una miocardio patía arritmogénica, en pacientes que carecen de un reflujo mitral grave con capacidad de generar daño estructural9. Este segundo mecanismo poco frecuente, es quizás el que explique la miocardio patía dilatada de la paciente presentada, dado que no presentó insuficiencia mitral significativa.
En la actualidad no contamos con evidencia fuerte sobre el manejo de las arritmias en esta afección, quizás con el avance de la multi-ima gen podamos seleccionar aquellos pacientes de alto riesgo10,11.
Algunos trabajos proponen el reemplazo mitral precoz el cual evita la fibrosis ventricu lar. Otros sugieren la ablación de zonas de fi brosis, identificadas por resonancia magnética cardiaca12.
A pesar de ser una enfermedad descrita hace décadas, actualmente el manejo suele ser com plejo. En nuestro caso la paciente pudo sobrevi vir a varios episodios de muerte súbita aborta dos, y se encuentra en clase funcional II.
Ante el pronóstico incierto de esta enferme dad, las múltiples formas de manifestarse, y la gravedad de las mismas, el seguimiento cercano de estos pacientes en estadios iniciales es man datorio.














