Durante toda la vida, la alimentación juega un papel esencial en el desarrollo del niño, pero aún más en momentos de crecimiento acelerado. Una nutrición adecuada constituye un proceso complejo, en el cual intervienen no sólo factores económicos sino también culturales, los cuales inciden tanto en los hábitos alimentarios como en los factores sanitarios, entre otros. El acceso a una alimentación “aceptable, suficiente y adecuada”, que depende de los ingresos y del costo de los alimentos, resulta restringida para amplios sectores de la población. En el caso de Argentina, no se encuentra garantizada la equidad alimentaria, es decir, “que todas las personas en especial los más pobres, tengan un acceso a una alimentación culturalmente aceptada, nutricionalmente adecuada, variada y suficiente para desarrollar su vida” (Aguirre, 2005). Dicha inequidad compromete la salud de amplios sectores, especialmente aquellos de recursos más bajos (Bergel Sanchís, Cesani y Oyhenart, 2017).
Las deficiencias de micronutrientes requieren de cierta instrumentación para su diagnóstico y dado que no se detectan por antropometría, es importante el diseño de modelos experimentales in vitro que permitan investigar el efecto de estas deficiencias y aportar información que pueda favorecer el desarrollo de políticas de prevención adecuadas (González, Varea y Malpeli, 2006). Las mismas deberían hacer hincapié en la importancia de la educación nutricional, avocada a la concientización del problema y la generación de una vigilancia social que traspase los marcos de los programas prediseñados (Molina, 2009).
La anemia afecta aproximadamente a un tercio de la población mundial, tanto de los países desarrollados como de aquellos en desarrollo. La mitad de los casos se deben a la deficiencia de hierro (Lopez, Cacoub, Macdougall y Peyrin-Biroulet, 2016). Sus causas son multifactoriales y, frecuentemente, pueden coexistir varias de ellas (Population, Health and Nutrition Information (PHNI), 2003). En nuestro país, numerosos estudios demuestran que la prevalencia de anemia y de deficiencia de hierro son muy elevadas (Apezteguia, Varea, Disalvo, Malpeli y Gonzales, 2008; Comité Nacional de Hematología, Oncología y Medicina Transfusional y Comité Nacional de Nutrición, 2017; Falivene y Fatore, 2016; González et al., 2006; 2007; Malpeli et al., 2006; Sguassero, Guerrero y Romero , 2018).
La anemia por deficiencia de hierro (ADH) es una condición patológica, en la cual no hay suficiente mineral para la síntesis de proteínas y enzimas que lo contienen, tales como hemoglobina, mioglobina y catalasas (Aksu et al., 2010). Dicha patología tiene un mayor impacto cuando ocurre en etapas tempranas de la vida, durante la primera infancia. En el caso de los niños de 0 a 5 años, afecta tanto el desarrollo, a través de la disminución de la atención, dificultades del aprendizaje y disminución en el desempeño cognitivo; como el crecimiento, pudiendo ocasionar un retardo crónico o una disminución de la velocidad del mismo (Algarín, Peirano, Garrido, Pizarro, Lozoff, 2003; Beard, 2001; Carter et al., 2010; Clark, 2008; González et al., 2007; Lozoff et al., 2007; Rivera, Hotz, González-Cossío, Neufeld y García-Guerra, 2003), alterando los aspectos físicos, mentales y sociales de la salud del niño.
La recomendación actual de la Sociedad Argentina de Pediatría (Comité Nacional de Hematología, Oncología y Medicina Transfusional y Comité Nacional de Nutrición, 2017) es la suplementación preventiva diaria con sulfato ferroso a partir de los 2 meses de vida para los nacidos de término alimentados con leche de vaca no fortificada y aquellos con lactancia materna que reciben alimentación complementaria inadecuada con bajo contenido de hierro. A pesar de ello, la adherencia a la suplementación es baja, por lo tanto, la prevalencia de esta patología continúa siendo muy alta en los niños menores de 2 años (Linetzky, Morello, Virgolini, Ferrante, 2011). Como alternativa, en niños y embarazadas, la suplementación semanal ha demostrado ser eficaz en la prevención de la ADH (De Regil, Jefferds, Sylvetsky y Dowswell 2011; Mozaffari Khosravi, Noori-Shadkam, Fatehi y Naghiaee, 2010; Peña-Rosas, De Regil, Malave, Flores Urrutia y Dowswell, 2015; World Health Organization, 2001) pero la evidencia en lactantes es escasa (de Camargo et al., 2008; Yurdakök, Temis, Yalçin y Gümrük, 2004). La dosis semanal permitiría optimizar la absorción a través de los mecanismos de transporte y disminuir así dichos síntomas. Cuenta con otras ventajas, tales como mayor adherencia y cumplimiento, y menores efectos adversos (Eickmann, Brito, Lira y Lima , 2008; Fernández Gaxiola y De Regil, 2019).
Por otro lado, el tratamiento diario preventivo puede llevar a la producción de un cuadro de sobrecarga tisular de hierro. Las alteraciones en la estructura y función celular causadas por la sobrecarga del mismo parecen estar fundamentalmente relacionados con el daño mediado por radicales libres a componentes celulares, tales como proteínas, lípidos y ADN (Jomova y Valko, 2011; Lin, Li, Jia, Ward y Kaplan, 2011; Prá, Franke, Henriques y Fenech, 2012). Este daño puede ser permanente (Aksu et al., 2010) y es aceptado como uno de los principales mecanismos subyacentes a la ocurrencia de ciertas enfermedades crónicas y a daños no deseados por intoxicación (Fraga y Oteiza, 2002; Toxqui et al., 2010). Sin embargo, las células han desarrollado diversos mecanismos para reducir la toxicidad de los iones de hierro, los cuales incluyen la regulación del transporte del hierro a través de las membranas, la producción de enzimas antioxidantes (AO) y el aprovechamiento de los antioxidantes no enzimáticos introducidos por la ingesta. Un antioxidante es, como definición general, cualquier sustancia capaz de prevenir la oxidación. La vitamina E, es el AO no enzimático liposoluble más importante y se lo considera esencial en la defensa celular. En varios estudios, realizados in vivo e in vitro, se ha observado que la vitamina E puede prevenir el daño ocasionado por el hierro (Fraga y Oteiza, 2002; Kajarabille y Latunde-Dada, 2019; Tang et al., 2016).
En trabajos previos, llevados a cabo in vitro por nuestro grupo de investigación (Gambaro, Seoane y Padula et al., 2018 a y b), se pudo observar que el tratamiento semanal tiene tendencia a provocar menor estrés oxidativo y, concomitantemente, menor daño genómico que el tratamiento preventivo diario de la ADH. El objetivo del presente trabajo es evaluar el efecto de la vitamina E sobre ambas modalidades de suplementación preventiva de la anemia ferropénica (diaria y semanal), y comprobar si la capacidad de este antioxidante logra disminuir el daño genotóxico inducido por el sulfato ferroso.
MATERIAL Y MÉTODOS
El presente trabajo se desarrolló in vitro con la utilización de cultivos de linfocitos de sangre periférica humana. Esta metodología se considera eficaz y adecuada para determinar el efecto del hierro sobre el daño genómico. Se optó por no realizar un aislamiento de los linfocitos previo al cultivo, debido a que la presencia de los componentes del plasma y el paquete eritrocitario es necesaria para reproducir con la mayor fidelidad posible las condiciones fisiológicas en las que funciona el sistema y su interacción con los micronutrientes.
Diseño Experimental
Se llevó a cabo un protocolo in vitro, donde se establecieron cuatro controles y cuatro tratamientos combinados con sulfato ferroso (SO4Fe) y vitamina E, según se detalla a continuación.
Se establecieron un control negativo (CN), en el cual las células no recibieron ningún tratamiento adicional, y un control positivo (CP), en el cual las células se trataron con bleomicina (2µg/ml), un reconocido agente inductor de daño genotóxico y citomolecular. Por otro lado, se establecieron dos tratamientos control de las dosis de vitamina E utilizadas: en uno las células se trataron con 8,3 µg/ml (T 8,3) y en el otro con el doble de la dosis, 16,6 µg/ml (T 16,6). El objetivo de estos controles es poder descartar un posible efecto tóxico propio de la vitamina E en estas dosis.
Respecto de los tratamientos combinados, se establecieron cuatro experimentos: el tratamiento con hierro diario con 0,14 mg/ml SO4Fe y 8,3ug/ml de vitamina E (HD 8,3); el tratamiento con hierro diario con 0,14 mg/ml SO4Fe y 16,6ug/ml de vitamina E (HD 16,6); el tratamiento con hierro semanal 0,55 mg/ml SO4Fe y con 8,3ug/ml de vitamina E (HS 8,3) y, por último, el tratamiento con hierro semanal 0,55 mg/ml SO4Fe y con 16,6ug/ml de vitamina E (HS 16,6).
Para simular in vitro los efectos del sulfato ferroso (Ferdrómaco Pediátrico, laboratorios Andrómaco, Buenos Aires, Argentina), se utilizaron las concentraciones publicadas en Gambaro et al. (2018 a). Para la vitamina E (Merck KGaA, Darmstadt, Germany), se establecieron 2 concentraciones, donde la más baja corresponde a la ingesta recomendada por día (4mg/día) y la más alta al doble de la misma calculados para 10 ml de medio de cultivo (vitamina E: 8,3ug/ml y 16,6ug/ml).
Condiciones de cultivo
Luego de la firma del consentimiento informado, se obtuvo una muestra de sangre de donantes sanos, la cual se recogió por punción venosa con jeringa heparinizada y se cultivó en frascos Falcon T-25 (Nunc, Denmark) utilizando como medio base al HAM F12 (Sigma-Aldrich, St. Louis, MO, USA), sin suero fetal bovino y con antibióticos (60UI de Penicilina y 50μg/ml de Estreptomicina) (Bagó Laboratorio, Buenos Aires, Argentina). La estimulación de los linfocitos se logró con 100 µg/ml de Fitohemaglutinina (GibcoThermo Fisher Scientific, Buenos Aires, Argentina). Las muestras se cultivaron a 37º C en 5% de CO2, durante 7 días (Fenech, 2007). Para los protocolos in vitro no se ha establecido un número mínimo de donantes, pero teniendo en cuenta que para los trabajos in vivo se utiliza un mínimo de 5 donantes (MacGregor et al., 1989), en este trabajo se decidió trabajar con un pool génico (teniendo en cuenta grupo y factor sanguíneo) de 10 individuos de sexo femenino de entre 30 y 40 años de edad.
El protocolo cuenta con la aprobación del Comité de Ética de la Universidad Nacional de La Plata (Argentina) y se ha respetado la letra y el espíritu de la Declaración de Helsinki de la Asociación Médica Mundial (Finlandia, 1964) y sus sucesivas enmiendas de 1975, 1983, 1989, 1996 y 2000.
Se realizaron 3 repeticiones de cada ensayo para una estimación precisa de la variación experimental y luego fueron calculados la media y el desvío estándar.
Daño genotóxico
Ensayo de micronúcleos por bloqueo de la citocinesis (CBMN): Actualmente el Ensayo de micronúcleos por bloqueo de la citocinesis (CBMN) se constituye como uno de los métodos más adecuados para evaluar las fluctuaciones de los micronutrientes, ya sea que se encuentren por demás o en menor cantidad de lo recomendado (Fenech, 2010). En el presente ensayo, se analiza la presencia de micronúcleos y otras alteraciones nucleares en células binucleadas (BN). Para ello, se emplea citocalasina B, una sustancia que se extrae del hongo Helminthosporium dematioideum, y que, en pequeñas concentraciones, inhibe la citocinesis y la movilidad celular dando como resultado células que han separado sus núcleos, pero no sus citoplasmas.
Las alteraciones que se analizan con este ensayo son principalmente los micronúcleos, que provienen de un fragmento cromosómico o un cromosoma entero que quedó relegado en anafase durante la división celular (MNi) (Fenech, 2010). También se cuantifican los brotes nucleares (NBuds), que son estructuras similares a vesículas unidas a alguno de los 2 núcleos principales, y los puentes nucleoplásmicos (NPBs), que se reconocen justamente por formar un puente entre los núcleos de una célula BN y son indicadores de rearreglos cromosómicos (Fenech, 2003; Umegaki y Fenech, 2000).
Para poder llevar a cabo este ensayo se debe asegurar que la mayoría de las células contadas derivan de la primera o de la primera y segunda división luego del tratamiento (Fenech, 2002; 2007; 2010). Para esto debe calcularse la proliferación celular de la siguiente forma:
Índice de división nuclear (NDI) = 1 x no. de células mononucleadas + 2 x no. de células binucleadas + 3 x no. de células tri y tetranucleadas / no. total de células contadas (500).
Estimativamente 30 hs. antes de terminar el cultivo se adiciona la citocalasina B (3 ug/ml) (Sigma, St. Louis, MO, USA). Una vez finalizado el mismo se trasvasa el contenido del frasco a un tubo Falcon y se centrifuga por 10 minutos a 1200 rpm. Luego se saca el sobrenadante y se agrega la solución hipotónica fría (ClK 0,075 M). Inmediatamente, se centrifuga nuevamente por 6 minutos a 1200 rpm y se procede a sacar el sobrenadante y agregar el fijador I (cloruro de sodio-metanol-ácido acético 6:5:1). Posteriormente, se realizan dos cambios más con fijador II (metanol-ácido acético 5:1) por 10 minutos a 1200 rpm. Luego de 24 hs. de reposo en heladera, se procede al goteo del material en portaobjetos. Los preparados se tiñen con colorante Giemsa durante 10 minutos, el mismo se prepara con agua y Giemsa al 5% según se especifica en el protocolo. Por último, se procede al análisis de 1000 células por punto experimental de acuerdo a los criterios de Fenech (Fenech, 2007).
Análisis estadístico
Las frecuencias de los biomarcadores descriptos fueron analizadas y comparadas con el programa estadístico Statgraphics® 5.1 software (Manugistics Inc., Rockville, MD). Dado que los resultados respondían a una distribución normal tanto el IDN, como los MNi y los NPBs se analizaron por medio del test de Anova Simple. Para poder visualizar la homogeneidad al interior de los grupos se realizó el test de grupos homogéneos. En el caso de los NBuds que no se correspondían con una distribución paramétrica se utilizó el test de Kruskal-Wallis.
RESULTADOS
En la Tabla 1, se resumen las frecuencias de los cuatro biomarcadores analizados (IDN, MNi, NPBs y NBuds). En el caso del IDN, se observa que los valores de los controles se encuentran ligeramente por encima de los correspondientes a los tratamientos combinados. En el caso de la frecuencia de MNi, se puede observar como los tratamientos con hierro diario muestran valores más altos que aquellos con hierro semanal, y que aquellos con la concentración más elevada de vitamina E poseen menores frecuencias de esta alteración. En el caso de los NPBs y NBuds las frecuencias son bajas en todos los tratamientos, sin embargo, la tendencia se corresponde con los valores de referencia que propone Fenech, 2007.
Tabla 1 Valores promedio y desvío estándar (entre paréntesis) para índice de división nuclear, micronúcleos, puentes nucleoplásmicos y brotes nucleares. Los valores corresponden a la proporción de alteraciones en 1000 células
| Tratamiento | IDN | MNi ‰ | NPBs ‰ | NBuds ‰ |
| CN | 1,136 (0,001) | 1,32 (0,001) | 0,0 (0,0) | 0 |
| CP | 1,06 (0,007) | 4,1 (0,141) | 0,7 (0,14) | 0,3 (0,07) |
| T 8,3 | 1,108 (0,007) | 1,11 (0,007) | 0,0 (0,7) | 0 |
| T 16,6 | 1,114 (0,001) | 1,09 (0,007) | 0,0 (0,0) | 0 |
| HD 8,3 | 1,062 (0,001) | 2,47 (0,007) | 0,2 (0,07) | 0 |
| HD 16,6 | 1,074 (0,001) | 2,41 (0,014) | 0,1 (0,07) | 0 |
| HS 8,3 | 1,074 (0,003) | 2,22 (0,014) | 0,1 (0,07) | 0 |
| HS 16,6 | 1,08 (0,002) | 2,14 (0,014) | 0,0 (0,0) | 0 |
En lo que respecta a la proliferación celular (IDN), se encontraron diferencias estadísticamente significativas entre los grupos (F= 114,11 p=0,0) a través del ensayo de ANOVA Simple. A partir del análisis por contraste de múltiples rangos se observaron cuatro grupos: a. control negativo (CN); b. controles con vitamina E (T 8,3 y T 16,6); c. tratamientos semanales combinados con vitamina E (HS 8,3 y HS 16,6) y tratamiento diario con la dosis más alta de vitamina E (HS 16,6); d. tratamiento diario con la dosis más baja de vitamina E (HD 8,3) y control positivo (CP). De todos los tratamientos combinados, aquel con la suplementación semanal y la dosis más alta de vitamina E (HS 16,6), presentó el mayor IDN (Fig. 1). El control negativo, presentó el IDN más elevado y el control positivo con bleomicina los valores más bajos.

Fig. 1 Índice de División Nuclear. Las barras de error indican el desvío estándar. Control Negativo (CN), Control Positivo (CP), Tratamiento 8,3 (T 8,3) Tratamiento 16, 6 (T 16,6) Hierro Diario (HD 8,3 y HD 16,6) Hierro Semanal (HS 8,3 y HS 16,6). Los grupos que no comparten la misma letra, son significativamente diferentes entre sí (los valores de P se refieren al análisis de ANOVA: p <0,05). De todos los tratamientos combinados, aquel con la suplementación semanal y la dosis más alta de vitamina E (HS 16,6), presentó el mayor IDN.
Los MNi, NPBs y NBuds se analizaron en 1.000 células binucleadas. El test de ANOVA Simple evidenció diferencias estadísticamente significativas (F= 840,04; p= 0,0) sólo para la frecuencia de MNi. Se diferenciaron 4 grupos: a. control negativo (CN) y ambos controles con vitamina E (T 8, 3 y T 16, 6); b. ambos tratamientos semanales (HS 8,3 y HS 16,6); c. ambos tratamientos diarios (HD 8,3 y HD 16, 6); d. control positivo (CP). Se observó un aumento significativo de micronúcleos en los tratamientos diarios respecto de los semanales (Fig. 2) y, además, se pudo observar menor frecuencia de daño cromosómico a mayor concentración de vitamina E, aunque estas observaciones no resultaron estadísticamente significativas. Los tratamientos con hierro diario tuvieron frecuencias mayores de MNi que los semanales.
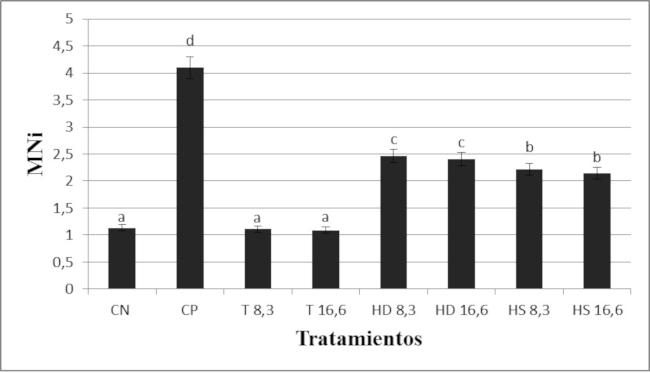
Fig. 2 Frecuencia de Micronúcleos. Las barras de error indican el desvío estándar. Control Negativo (CN), Control Positivo (CP), Tratamiento 8,3 (T 8,3) Tratamiento 16, 6 (T 16,6) Hierro Diario (HD 8,3 y HD 16,6) Hierro Semanal (HS 8,3 y HS 16,6). Los grupos que no comparten la misma letra son significativamente diferentes entre sí (los valores de P se refieren al análisis de ANOVA: p <0,05). Se observó un aumento significativo de micronúcleos en los tratamientos diarios respecto de los semanales y una menor frecuencia de daño cromosómico a mayor concentración de vitamina E.
Cuando se analizaron las frecuencias de NPBs, las diferencias no resultaron estadísticamente significativas entre los tratamientos (F=2,54; p=0,107) (Fig. 3). Dado que las frecuencias de los NBuds no responden a una distribución paramétrica, se utilizó la prueba de Kruskal-Wallis (E=12,63; p=0,082). Dentro de la comparación de a pares, sólo resultaron estadísticamente significativas las diferencias entre el control positivo y los demás tratamientos (Fig. 4).
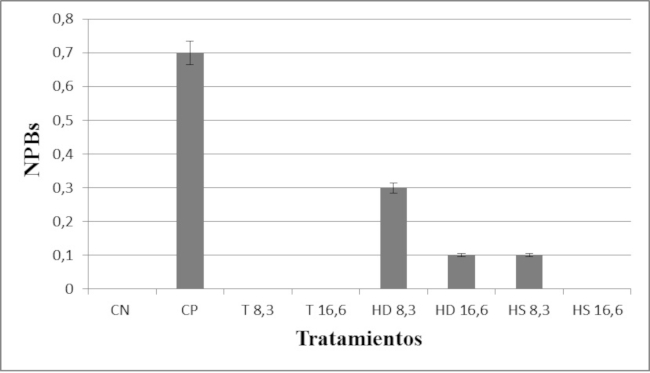
Fig. 3 Frecuencia de Puentes Nucleoplásmicos. Las barras de error indican el desvío estándar. Control Negativo (CN), Control Positivo (CP), Tratamiento 8,3 (T 8,3) Tratamiento 16, 6 (T 16,6) Hierro Diario (HD 8,3 y HD 16,6) Hierro Semanal (HS 8,3 y HS 16,6). Cuando se analizaron las frecuencias de NPBs, las diferencias no resultaron estadísticamente significativas entre los tratamientos.
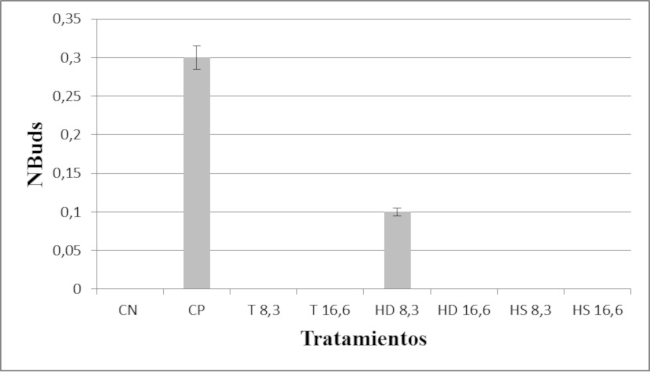
Fig. 4 Frecuencia de Brotes Nucleares. Las barras de error indican el desvío estándar. Control Negativo (CN), Control Positivo (CP), Tratamiento 8,3 (T 8,3) Tratamiento 16, 6 (T 16,6) Hierro Diario (HD 8,3 y HD 16,6) Hierro Semanal (HS 8,3 y HS 16,6). Sólo resultaron estadísticamente significativas las diferencias entre el control positivo y los demás tratamientos.
DISCUSIÓN
Teniendo en cuenta que en trabajos previos de nuestro grupo (Gambaro et al., 2018 a), se pudo observar que el tratamiento semanal con sulfato ferroso ocasiona menos daño en el material genético que el tratamiento diario; y dado que la vitamina E constituye uno de los antioxidantes liposolubles más importante del organismo, se planteó evaluar su efecto en ambos tratamientos. En este sentido, el objetivo del presente trabajo fue evaluar in vitro el efecto de la vitamina E, sobre ambas formas de suplementación con sulfato ferroso (diario y semanal) respecto de la inducción de daño cromosómico.
Para analizar la proliferación celular, se reparó en los resultados del IDN. En este trabajo, se puede observar que el tratamiento semanal presentó un IDN mayor que el tratamiento diario. Respecto al agregado de vitamina E ambas dosis mejoran la proliferación celular y, por ende, atenuarían los efectos citotóxicos del sulfato ferroso, sobre todo en los tratamientos con dosis más altas. Respecto de los controles con ambas dosis de vitamina E, si bien se pudo observar un mayor índice de división nuclear en la dosis más alta, dicho aumento no resultó significativo. Resultados similares fueron reportados por Avula y Fernandes (2000), que observaron que la suplementación con vitamina E en la dieta favorecería la proliferación celular y disminuiría la muerte celular programada al reducir los peróxidos lipídicos en un ensayo con ratones in vivo ( Avula y Fernandes, 2000). Los valores de IDN observados para todos los tratamientos fueron menores que los publicados por Fenech (2007) para linfocitos humanos. Estas diferencias pueden ser adjudicadas a la menor concentración de citocalasina B utilizada (Fenech, 2007) y también al extenso tiempo de cultivo que requiere el protocolo llevado a cabo.
Con respecto a los resultados para los demás biomarcadores, observamos que la frecuencia de MNi para el control negativo y ambos tratamientos control de vitamina E fueron las más bajas entre todos los tratamientos. Por otra parte, la frecuencia de MNi de los tratamientos con sulfato ferroso semanal es significativamente inferior a la observada para los tratamientos diarios. De todos modos, a pesar de observarse estas diferencias, ambas frecuencias se encuentran dentro de los parámetros de normalidad establecidos por Fenech (2007), hecho esperable dado que se trata de dosis correspondientes a suplementación preventiva de la anemia. Sin embargo, en lo que respecta a los resultados aquí obtenidos el tratamiento semanal genera menor efecto genotóxico que el tratamiento diario, lo que podría ser un punto de partida para rever las normas actuales de profilaxis. En la bibliografía analizada, al igual que en el presente trabajo, se observa un aumento del daño genético en relación al aumento de los niveles de sulfato ferroso (Franke, Prá, Silva, Erdtmann y Henriques 2005; Gambaro et al., 2018 a y b; Jomova y Valko, 2011; Lin et al., 2011; Prá et al., 2008; Premkumar y Bowlus, 2003).
En los resultados aquí reportados, se puede observar una clara tendencia hacia un menor daño con las dosis más altas de vitamina E (16,6) aunque dichas diferencias no resultaron estadísticamente significativas. La bibliografía publicada respecto de la combinación entre el sulfato ferroso y la vitamina E, está fundamentalmente basada en los efectos del tratamiento terapéutico de la anemia y resulta contradictoria. Claycombe y Meydani (2001) proponen que la vitamina E, al ser el antioxidante lipídico más potente, podría reducir el daño cromosómico inducido por los radicales libres mediante la inhibición de la formación de los mismos y la activación de las endonucleasas que aumentan la tasa de eliminación del ADN dañado (Claycombe y Meydani, 2001); mientras que Tang y colaboradores (2016), plantean que adicionar vitamina E a la suplementación terapéutica con hierro disminuye los efectos perjudiciales del hierro en la comunidad microbiana en el tracto intestinal y, a su vez, al disminuir la inflamación podría favorecer la absorción del hierro (Tang et al., 2016). Por otra parte, Wawrzyniak y colaboradores (2013) sugieren, a partir de la experimentación en un modelo de ratones, que el α-tocoferol, el ácido ascórbico y el β-caroteno, cuando se administran simultáneamente, tienen principalmente efectos antioxidantes sobre la peroxidación lipídica (Wawrzyniak et al., 2013). Riffle y colaboradores (2018) observaron, en un modelo de ratones, que tanto la vitamina C como la vitamina E favorecen a la eliminación de especies reactivas de oxígeno y ayudan a normalizar el estado oxidativo de la médula espinal alterado por el dolor (Riffel et al., 2018). En discordancia con estos resultados, otros autores no encontraron ningún tipo de efecto protector de la vitamina E contra el daño oxidativo. Record y Jannes (2000), hallaron que la suplementación con vitamina E no tendría efecto protector contra el daño genómico oxidativo en esplenocitos sometidos a estrés oxidativo ex vivo (Record y Jannes, 2000). A su vez, Fenech, Dreosti y Aitken (1997) evidenciaron, durante un estudio de intervención, que el aumento de vitamina E no tuvo un impacto significativo en la tasa de daño genético basal y tampoco hubo correlación positiva entre la frecuencia de daño genético basal y el estado de vitamina E evaluado en linfocitos humanos (Fenech et al., 1997). En lo que respecta específicamente a este trabajo, se podría interpretar que frente a la presencia de un poderoso pro-oxidante como es el sulfato ferroso, mayor cantidad antioxidante de vitamina E resultaría beneficioso para contrarrestar la mayor producción de radicales libres y disminuir así el daño cromosómico.
Los resultados para las frecuencias de puentes y brotes nucleares también se encuentran dentro de lo que Fenech (2007) considera rangos normales de daño genómico. En ambos casos, se puede observar un menor daño genético con el tratamiento semanal en comparación con el tratamiento diario, el cual es aún menor en combinación con la concentración más alta de vitamina E. Sin embargo, como se menciona anteriormente las frecuencias para ambos indicadores son muy bajas impidiendo un análisis más profundo.
CONCLUSIONES
Los resultados del presente trabajo in vitro permiten sugerir que la vitamina E, por sus características antioxidantes, complementaría la respuesta de los antioxidante enzimáticos y ayudaría a disminuir el estrés oxidativo y el consecuente daño genómico ocasionado por el sulfato ferroso. Dicho efecto protector parecería ser mayor al aumentar al doble la dosis de ingesta diaria recomendada para lactantes (16,6). Estos resultados permitirán rever, con una base científica, la forma de suplementación preventiva de la anemia ferropénica. Realizar la suministración conjunta de vitamina E con sulfato ferroso en dosis semanales, podría ser una estrategia plausible para disminuir los efectos adversos que este tratamiento ocasiona. Sin embargo, sería necesario complementar estos hallazgos con estudios donde se analice el estrés oxidativo y daño citomolecular (ensayo cometa) entre otros.












 uBio
uBio 


