Introducción
Los tumores de células de Leydig (TCL) pertenecen a la categoría de tumores endócrinos del intersticio testicular. Si bien en el 90% de los casos resultan clínicamente benignos, un 10% de los casos reportados maligniza en adultos ocasionando tumores resistentes a la radio y a la quimioterapia, lo cual conlleva a que los pacientes posean una sobrevida de solamente dos años 1-3. Además, se ha descrito que ambas terapias aumentan la incidencia de otros tumores a largo plazo 4. Esto implica la necesidad de identificar nuevos blancos terapéuticos para el tratamiento de los TCL, para así poder evitar la resección quirúrgica del testículo y las consecuentes terapias de reemplazo hormonal; lo cual podría llevar, no sólo a la pérdida de las funciones reproductivas del paciente 5, sino también a trastornos psicológicos asociados 6. A su vez, se ha reportado que los TCL comprenden el 4% de los tumores testiculares en niños 1,7, siendo de especial importancia en este grupo etario debido a la aparición de fenotipos como pubertad precoz o ginecomastia 8,9, ambos producto de la alta concentración sérica de esteroides provenientes del tumor (testosterona o estradiol, E2, respectivamente). En los últimos años, la implementación de técnicas más precisas de diagnóstico ha permitido evidenciar que la incidencia de este tipo de tumor es superior al 4%, ascendiendo a un 15% 10,11. A nivel nacional, la Dirección de Estadísticas e Información en Salud del Ministerio de Salud de la Nación (http://www.deis.msal.gov.ar), ha reportado a la fecha un creciente aumento en el número de egresos y defunciones causadas por tumores testiculares, lo cual sugiere la necesidad de prestar mayor atención a este tipo de neoplasias. Lo mismo se observa a nivel mundial 12,13. De forma complementaria, se ha descrito que los TCL no sólo se desarrollan en el testículo, sino también en cordón espermático, ovario y glándula adrenal 14,15. Si bien la etiología de los TCL es aún desconocida, su aparición se ha relacionado con la sobreexpresión de la enzima CYP19 aromatasa y por consiguiente altos niveles de E2, y del factor de crecimiento símil insulina tipo 1 (IGF-1). Ambos factores estarían involucrados en un aumento de la proliferación celular 3,16. Además, se ha reportado muy recientemente una relación causal entre estos tumores y el uso de anabólicos esteroides 17.
La histidina decarboxilasa (HDC) es la única enzima presente en mamíferos capaz de catalizar la conversión de L-Histidina a Histamina (HA) 18. Se ha descrito que HDC está relacionada con la agresividad tumoral, sobre la base de que está sobreexpresada en diversos tipos de tumores malignos, particularmente de mama 19, colangiocarcinoma 20 colorrectal 21,22 y melanoma 23. En nuestro laboratorio, hemos observado sobreexpresión de HDC 24 en TCL pediátricos pertenecientes a pacientes de todos los estados del desarrollo testicular (ver tabla 1). Sumado a estas evidencias, se ha descrito que ratones knock out para el gen de HDC poseen una angiogénesis incompleta 25. Además la línea de células de Leydig tumorales MA-10, que también sobreexpresa HDC, sintetiza y secreta el factor de crecimiento de endotelio vascular (VEGF) 26 y se ha reportado que la HA actúa de forma proangiogénica en córnea 27-29.
Se sabe que el proceso de angiogénesis es uno de los pilares fundamentales para la progresión y malignización de una neoplasia, permitiendo la llegada de nutrientes a todo el volumen tumoral y siendo una vía de salida a la circulación30. Así, por lo expuesto, el objetivo del presente trabajo es profundizar nuestros estudios previos acerca del papel de HDC en la biología de los TCL, evaluando particularmente su rol sobre la modulación de la angiogénesis. Para ello, utilizamos el modelo de células de Leydig tumorales de rata R2C, ya validado para el estudio de Leydigiomas debido a su gran similitud con el fenotipo de los TCL 3,31. Además, realizamos por primera vez estudios de angiogénesis empleando medios condicionados obtenidos a partir del cultivo de células provenientes de 3 TCL pediátricos.
Materiales, pacientes y métodos
Reactivos generales
La [3H]-Timidina (20 Ci/mmol) se compró a New England Nuclear (North Billerica, Massachusetts, Estados Unidos). Los reactivos α-metilhistamine dihidrocloruro (α-MHD) y el dihidrocloruro de Histamina (HA) se adquirieron en Sigma- Aldrich Chemical (Darmstadt, Alemania). El IGF-1 (Factor de crecimiento tipo insulina) fue gentilmente donado por la Dra. Roxana Schillaci (Laboratorio de Mecanismos Moleculares de Carcinogénesis, IBYME-CONICET). El estradiol (E2) fue gentilmente cedido por la Dra. Victoria Lux (Laboratorio de Neuroendocrinología, IBYME-CONICET). hVEGF (Factor de crecimiento de endotelio vascular humano) fue desarrollado por los Dres. Alberto Baldi y Adrián Góngora (Laboratorio de Patología y Farmacología Molecular, IBYME-CONICET). Los reactivos para mantener en cultivo las líneas celulares se obtuvieron de Gibco-BRL (Waltham, Massachusetts, Estados Unidos), y las placas plásticas se compraron en Corning (Corning, Nueva York, Estados Unidos) y BD Falcon (San José, California, Estados Unidos). Los demás reactivos utilizados fueron del mejor grado disponible y comprados a los proveedores usuales.
Material clínico
Se utilizaron muestras de TCL obtenidas a partir de biopsias de tres pacientes pediátricos (PP1, PP2, PP3), las tres con su correspondiente consentimiento informado firmado por los padres de los pacientes antes de las cirugías. El diseño del estudio, los procedimientos de recolección de muestras y el formulario para el consentimiento informado fue aprobado por el Comité de Ética del Hospital de Pediatría Juan P. Garrahan (Buenos Aires, Argentina). La utilización de muestras humanas se realizó de acuerdo a la Declaración de Helsinki (Ratificada en 2013).
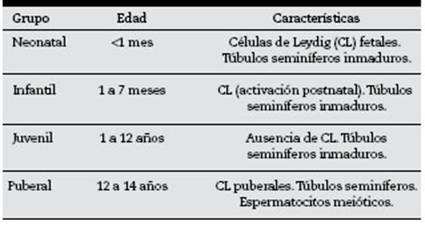
Tabla 1 Clasificación de testículos humanos en grupos etarios, según las características del parénquima testicular
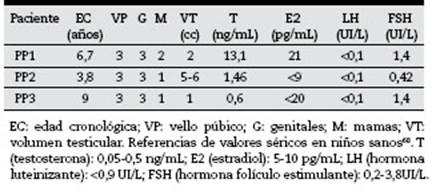
Tabla 2 Información clínica de los pacientes analizados, según estadios del desarrollo descritos por Tanner
Cultivo de células de Leydig tumorales R2C y células HUVEC La línea de células de Leydig tumorales de rata R2C fueron compradas a la ATCC (# 58649146), mientras que las células de endotelio venoso de cordón umbilical humano (HUVEC) fueron gentilmente donadas por el Dr. Alberto Baldi (Laboratorio de Patología y Farmacología Molecular, IBYME-CONICET, Buenos Aires, Argentina). Los experimentos con ambas líneas fueron realizados por triplicado, con al menos tres diferentes pasajes. Las células R2C se cultivaron en medio rico en nutrientes Ham’s/F12, conteniendo 1,2 g/L de bicarbonato de sodio, Glutamina 2 mM, Penicilina 100 U/mL y Estreptomicina 100 µg/mL, suplementado con suero de caballo al 12,5% y suero fetal bovino al 2,5% (medio de crecimiento), a 37ºC en una atmósfera de 5% de CO2. Las células HUVEC se mantuvieron en cultivo según el protocolo antes descrito 32.
Cultivo primario de células provenientes de tumor de células de Leydig
Una muestra de cada TCL (Paciente pediátrico: PP1, PP2 y PP3) fue disectada como se ha descrito previamente 33,34. Las células fueron sembradas en placas de 12 pocillos en presencia de DMEM/Ham F12 suplementado con vitamina C (5 mg/mL), vitamina E (0,2 µg/mL) y suero fetal bovino al 10% durante 48 h. A continuación, las células fueron lavadas e incubadas durante 6 días en DMEM/F12 libre de suero, renovándolo cada 48 horas. El medio condicionado (MC) por estas células fue colectado y reservado para el tratamiento de las HUVEC a -20ºC (fig. 1).
Ensayo de proliferación en células HUVEC
Los MC de las R2C para el tratamiento de las HUVEC se obtuvieron de la siguiente manera: se sembraron R2C en placas de 6 pocillos el día 0 a una densidad de 5 x 105 células/ pocillo, en un volumen total de 3 mL de medio completo. Se mantuvieron en atmósfera húmeda conteniendo 5% de CO2. El día 3, las células se lavaron dos veces con 1 mL de medio libre de suero. Se realizaron incubaciones en un volumen final de 0,8 mL por pocillo a 37ºC con medio Ham’s/F12 completo, solo o suplementado con α-MHD 10 µM, IGF-1 100 ng/mL, E2 10 µM e Histamina (HA) 10 µM. A las 48 h, los medios fueron colectados y preservados a -20ºC para el posterior tratamiento de las HUVEC junto con los medios provenientes de los cultivos primarios de los TCL. El efecto de esos medios sobre la proliferación de las HUVEC fue evaluado como se ha descrito previamente 32.
Ensayo de angiogénesis en membrana corioalantoidea de embrión de codorniz (Ensayo CAM) Los experimentos se llevaron a cabo en embriones de codorniz (Coturnix coturnix japonica) crecidos en placa de 6 pocillos según lo descrito 35. Discos de 5 mm de diámetro de papel de filtro embebidos en los tratamientos fueron dispuestos sobre la membrana corioalantoidea de los embriones el día 7, a 37ºC durante 48 h. Cada experimento de diez embriones por grupo experimental se repitió dos veces. Finalmente se fijaron, procesaron y analizaron las membranas, contabilizando el número de bifurcaciones en los vasos por unidad de área, según lo descrito 36.
Resultados
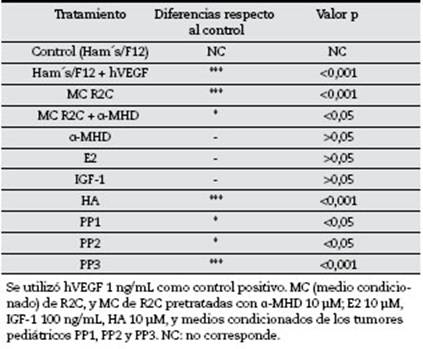
Efecto de medios condicionados por tumores pediátricos de células de Leydig sobre la proliferación del endotelio vascular in vitro En primer lugar, se estudió la presencia de factores angiogénicos en MC por células provenientes de TLC pediátricos (PP1, PP2 y PP3), evaluando la capacidad de dichos MC de inducir la proliferación de células HUVEC en cultivo. Como se indica en la tabla 3, los MC estimularon la proliferación de las HUVEC de forma significativa (PP1 y PP2: p <0,05, PP3: p <0,001).
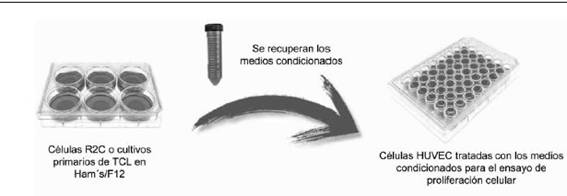
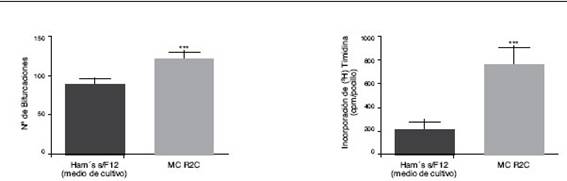
Figura 1 Esquema de obtención de los medios condicionados por las células de Leydig R2C o por los cultivos primarios de los TCL pediátricos. Luego de 48 h de incubación se recuperaron los medios y con ellos se trataron las células HUVEC en presencia de [3H]-Timidina para evaluar proliferación celular.
Efecto de medios condicionados por células de Leydig R2C sobre la proliferación del endotelio vascular in vitro e in vivo Tal como se esperaba en función de lo observado para los MC por TCL pediátricos, los MC provenientes de las células de Leydig de rata R2C estimularon la formación de nueva vasculatura in vitro (fig. 2) en membranas corioalantoideas de embriones de codorniz, y aumentaron la proliferación de las células HUVEC in vitro (fig. 3, p <0,001).
Identificación de los factores angiogénicos sintetizados y secretados por las células de Leydig tumorales
Para caracterizar el/los factor/es angiogénicos sintetizados por los TCL, se realizaron tratamientos directos sobre las HUVEC con factores conocidos por estar involucrados en la progresión de TCL: E2 (10 µM), IGF-1 (100 ng/mL) e HA (10 µM). De estos últimos, el único factor que indujo un aumento significativo de la proliferación del endotelio vascular fue la HA (p <0,001). Más aún, pretratando las células R2C con α-MHD 10 µM, inhibidor de la actividad de la enzima HDC, se observó que los sobrenadantes recuperados no eran capaces de estimular la proliferación de las HUVEC de forma significativa (tabla 3).
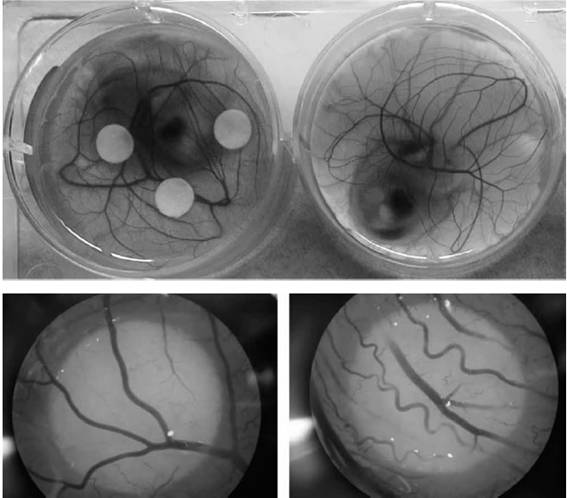
Figura 2 Arriba. Figura representativa de dos embriones de codorniz dispuestos en una placa de 6 pocillos para la incubación con los tratamientos mencionados. Abajo. Imagen representativa de un disco con pocos vasos, perteneciente al medio control sin factores angiogénicos (izquierda) y al medio condicionado por las células de Leydig tumorales R2C (derecha).
Discusión
Si bien los TCL son mayormente benignos, cuando malignizan resultan mortales, permitiendo una sobrevida de solamente dos años a causa de la resistencia a terapias convencionales 1,3. Por otro lado, las terapias actuales para los TCL benignos pueden tener consecuencias a nivel físico y/o psicológico, potencialmente irreversibles 37-39. En conjunto, esto último expone la necesidad de encontrar terapias alternativas, eficaces al controlar el desarrollo de estas neoplasias pero con mínimos efectos colaterales para el paciente. Debido a que inhibir el proceso de angiogénesis es una estrategia muy utilizada para el tratamiento de tumores malignos y otros desórdenes 40, el presente trabajo se centró en el estudio de la angiogénesis en los TCL.
En primer término, demostramos que las células de Leydig tumorales provenientes de pacientes pediátricos con TCL son capaces de sintetizar y secretar factores proangiogénicos para regular la generación de nueva vasculatura, con base en que las HUVEC sólo proliferan en presencia de factores proangiogénicos 41. Esto se condice con lo descrito por Samson y colaboradores, quienes demostraron que las células de Leydig son capaces de secretar factores proangiogénicos tanto en situaciones normales como patológicas, desde estadios fetales hasta adultos 42. Si bien en tejidos normales la síntesis de factores proangiogénicos debe ser estimulada por hCG 43, este tipo de tumores lo hace de forma espontánea. En otros tumores testiculares, como aquellos que se originan en la línea germinal, la regulación de la angiogénesis no se limita a la secreción exclusiva desde las células tumorales, sino que existe una contribución por parte de otros tipos celulares asociados al tumor 44. Debido a ello, a futuro nos abocaremos a dilucidar si el microambiente de TCL posee otros elementos que regulen la angiogénesis, además de los evidenciados en este trabajo por parte de las células de Leydig. Las células de Leydig tumorales R2C, originalmente obtenidas a partir de un TCL de rata, sintetizan esteroides en forma constitutiva y presentan el mismo fenotipo que la mayoría de los TCL humanos. Es por ello que constituyen un modelo validado para el estudio de Leydigiomas 3,31. El hecho de que los MC por las R2C sean capaces de estimular la angiogénesis in vitro, evidenciado en este trabajo, revela un nuevo punto en común entre el comportamiento de las R2C y el fenotipo de los TCL pediátricos. Es razonable entonces inferir que lo observado en membranas corioalantoideas de codorniz con los MC provenientes de las R2C esté de algún modo reproduciendo el comportamiento de los TLC pediátricos in vivo.
Se sabe que la HA está íntimamente involucrada en la regulación de la angiogénesis 27-29, ya sea asociada a la transglutaminasa 2 -enzima capaz de unir histamina a residuos de ácido glutámico (histaminilar) del fibrionógeno durante el proceso de neoangiogénesis y reparación de tejidos 45-; o a través de sus 4 subtipos de receptores (HRH1-HRH4) 46, o bien debido a su interacción directa con el ADN 47. Sumado a ello, se ha descrito que la regulación de la concentración de HA local modula la producción de factores proangiogénicos, al menos en colangiocarcinoma 48. Así, teniendo en cuenta estas evidencias y resultados previos de nuestro laboratorio que indicaban que la HA regula la proliferación de células de Leydig tumorales de ratón MA-10 49, en este trabajo se planteó estudiar la posible participación directa de la HA en el efecto proangiogénico de las células de Leydig tumorales R2C. Efectivamente, inhibiendo la síntesis de HA en dichas células, demostramos el rol fundamental de la amina en la inducción de angiogénesis. Sin embargo, sin duda no es la única molécula involucrada, y además se ha reportado que podría ejercer su función mediante la regulación de la expresión de VEGF 50 a través del subtipo de receptor HRH2, modulando la síntesis de AMPc y la vía de transducción de señales mediada por PKA 51. Además, diversos autores han clasificado a la HA como agente proangiogénico 52-54. De forma complementaria, se ha descrito que tejidos endócrinos (tal como es el caso de las células de Leydig del intersticio testicular), sintetizan y secretan un factor de crecimiento de endotelio vascular tejido específico, EG-VEGF, que estaría involucrado en el desarrollo de los TCL 40,42,55.
En las células R2C, se ha reportado que el IGF-1 y el E2 cumplen un rol fundamental regulando su proliferación 3,31. Lo mismo se observó en tumores de células de Leydig 16,56-59. En este trabajo, descartamos que los factores E2 e IGF-1 intervengan en la regulación de la angiogénesis en forma directa, al menos en los tiempos ensayados. En contraposición con nuestros resultados, otros autores han descrito que el E2 regula positivamente la proliferación de las HUVEC, pero el efecto recién se observa al cabo de tres días de tratamiento 60,61. A su vez, se ha descrito que el IGF-1 es capaz de revertir el arresto celular en las HUVEC 62 y que, a mayores concentraciones que las utilizadas en este trabajo, es capaz de aumentar su proliferación 63.
Cabe agregar que las prostaglandinas, también sintetizadas por las R2C, podrían estar involucradas en el proceso de angiogénesis, con base en que se ha reportado que la PGE2 (prostaglandina E2) aumenta la angiogénesis en la córnea de conejo y en membrana corioalantoidea de embriones de pollo de 8 días de gestación 64; y esto se ha ratificado con experimentos en donde la inhibición de COX-2, responsable de la síntesis de PGE2, disminuye la angiogénesis65. Sería importante evaluar, a futuro, el efecto de PGE2 en la angiogénesis in vitro. de TLC.
En trabajos previos, reportamos que la inhibición de HDC disminuye el crecimiento tumoral y la síntesis de esteroides24 y aquí describimos que revierte la estimulación de la angiogénesis in vitro. A su vez, como se indicó previamente, HDC está sobreexpresada en diversos tipos de tumores, tanto benignos como malignos 19-23, y cumple un rol fundamental durante su desarrollo. Por todo esto, proponemos a la inhibición selectiva de HDC - impidiendo así la síntesis de HA - como estrategia terapéutica para retrasar y/o detener el crecimiento de TCL, ya sea con inhibidores solos o en combinación con bloqueantes de la síntesis de EG-VEGF 66.