INTRODUCCIÓN
La vitamina D (VD) es una hormona esteroidea pleiotrópica tradicionalmente vinculada con la salud mineral ósea. Sin embargo, se ha demostrado ampliamente que el calcitriol (1a,25(OH)2-vitaminaD3), la forma activa de la VD, interviene en la regulación de múltiples procesos fisiológicos1-3. En este sentido, varios trabajos han relacionado a la VD con la función reproductiva masculina reportando la presencia del receptor de VD (RVD), y de las enzimas capaces de metabolizarla, en distintos tipos celulares del testículo4, e incluso, se ha expuesto una correlación con la producción de los esteroides sexuales, testosterona y estradiol, en dicha gónada5-7. A la fecha, no se ha estudiado la expresión de RVD a lo largo del desarrollo testicular normal. El RVD es miembro de la familia de receptores nucleares, y se encuentra presente en la mayoría de las células del cuerpo. Mediante su unión al calcitriol, y asociado a co-activadores o co-represores, regula de manera directa o indirecta entre el 3-5% del genoma humano8. Entre los genes regulados por RVD se incluye HRH1, que codifica para el receptor a histamina (HA) subtipo H19.Trabajos previos de nuestro grupo han demostrado que la HA, mediante su interacción con HRH1 y los subtipos de receptores histaminérgicos H2 y H4 (HRH2 y HRH4, respectivamente) modula la esteroidogénesis en células de Leydig, en forma bifásica y concentración-dependiente10. Asimismo, hemos observado una disminución de la enzima que cataliza la síntesis de HA a partir de L-Histidina, Histidina descarboxilasa (HDC), durante la ontogenia de las células de Leydig11.
Estudios epidemiológicos recientes han sugerido fuertemente que la deficiencia de VD no sólo se relaciona con raquitismo y osteomalacia, sino también con mayor riesgo de diabetes y de enfermedades cardiovasculares, infecciosas, autoinmunes y oncológicas12,13. Los tumores de células de Leydig (TCL) son un tipo poco común de tumores endócrinos, de etiología aún desconocida, que se originan en el intersticio testicular. Comprenden del 1-3% de las neoplasias testiculares en adultos y el 4% en niños prepuberales, pero su incidencia se encuentra en aumento. Si bien son normalmente benignos, aproximadamente un 10% de los TCL en pacientes adultos maligniza y no responde a radioterapia y/o quimioterapia14-16.
Lo expuesto resalta la necesidad de conocer más profundamente la biología de los TCL, a fin de identificar nuevos blancos para su tratamiento. Al respecto, en publicaciones previas se ha reportado el potencial uso terapéutico del calcitriol en cáncer de mama, de próstata y colorrectal, en los que los niveles de VD circulantes correlacionan con un mejor pronóstico y una mayor sobrevida 17-20. Sin embargo, poco se conoce aún acerca de su posible aplicación en TCL. En este contexto, resulta fundamental como un primer paso, investigar la expresión de RVD en estos tumores.
En el presente trabajo se planteó analizar la expresión RVD en la ontogenia de testículo de rata, evaluando una posible correlación con los niveles de testosterona (T) circulantes y el contenido endógeno de HA. Asimismo, se estudió la expresión de RVD en testículo humano fetal, neonatal y juvenil, y también en TCL e hiperplasia de células de Leydig. Finalmente, se investigó la potencial regulación de la expresión génica de RVD por calcitriol, HA y testosterona en TCL, empleando el modelo de células de Leydig tumorales de rata R2C, ya validado para el estudio de Leydigiomas debido a la similitud que presentan con el fenotipo de los TCL16-21.
MATERIAL Y MÉTODOS
Reactivos generales
El calcitriol fue generosamente donado por el Dr. Alejandro Curino (Laboratorio de Biología del Cáncer, INIBIBB-CONICET, Bahía Blanca, Argentina). La testosterona, histamina dehidrocloruro, 3,3-diaminobenzidina (DAB), HEPES, carbón activado, fueron comprados a Sigma-Aldrich Chemical Co. (St. Louis, MO, EEUU). El dextrano T-70 y la gelatina para RIA de esteroides fueron de Pharmacia (Amersham-Pharmacia, Reino Unido) y Panreac Química S.A. (Barcelona, España), respectivamente. El medio Ham's/F12, fue comprado a Sigma-Aldrich Chemical Co (St. Louis, MO, EEUU). El suero de caballo, el suero fetal bovino y la solución de tripsina/EDTA (0,25% /1 mM) fueron obtenidas en Gibco Laboratories (Grand Island, NY, EEUU). La penicilina-estreptomicina se compró en Invitrogen (Carlsbad, CA). El material de cultivo utilizado fue de Corning y Falcon. Para la preparación de los medios, se utilizaron unidades filtrantes de acetato de celulosa (0,22 pm) de Corning Incorporated (Corning, NY, US). La [2,3,4,5-3H]- Testosterona (80 Ci/mmoL) fue obtenida de Amersham International (Buckinghamshire, GB). El anticuerpo anti-Testosterona fue una donación del Dr. GD Niswender (Animal Reproduction, Biotechnology Lab, Colorado State University, Fort Collins, EEUU). Los demás reactivos utilizados fueron del mejor grado disponible y obtenidos de los proveedores usuales.
Material Clínico
Todas las muestras de material humano fueron obtenidas a partir de biopsias de pacientes pediátricos, con su correspondiente consentimiento informado firmado por los padres de los pacientes antes de las cirugías. El diseño del estudio, los procedimientos de recolección de muestras y el formulario para el consentimiento informado fue aprobado por el Comité de Ética del Hospital de Pediatría Juan P. Garrahan (Buenos Aires, Argentina). La utilización de muestras humanas se realizó de acuerdo a la Declaración de Helsinki (Ratificada en 2013).
Inmunohistoquímica en cortes de testículo
Se utilizaron muestras de testículo normal fetales, neonatales y prepuberales, hiperplasias de Leydig y tumores de Leydig, cortadas en secciones de 10 pm, las cuales se incubaron con anticuerpo primario monoclonal anti-receptor de vitamina D hecho en ratón (Concentración 1:50, sc-13133, Santa Cruz, CA, USA). Luego se incubaron con anticuerpo secundario anti-ratón hecho en caballo (Vector Laboratories, CA, EE.UU.). La inmunomarca se generó por el método de estreptavidina-biotina y peroxidasa, según indicaciones del fabricante (DAKO Catalyzed Signal Amplification System, HRP, Dako Cytomation, CA, EE.UU.). Se realizaron controles negativos reemplazando el anticuerpo primario por suero de ratón según correspondiera. En este caso no se detectó inmunoreactividad.
Modelo animal
Se utilizaron ratas macho de la cepa Sprague-Dawley de 7, 21, 35, 90 y 240 días, criadas en el bioterio del Instituto de Biología y Medicina Experimental, respetándose en todo momento las reglas de la “Guía para el cuidado y utilización de animales de laboratorio” del Instituto Nacional de Salud de los Estados Unidos (NIH).
Inmunohistoquímica en testículos de rata
Los testículos de ratas se fijaron en Bouin y se incluyeron en parafina. Se utilizaron secciones de 10 pm, las cuales se incubaron con anticuerpo primario policlonal anti-histamina hecho en conejo (concentración 1:100, HIST12-A, Alpha Diagnostics International, TX, EE.UU.) o con anticuerpo primario monoclonal anti-receptor de vitamina D hecho en ratón (Concentración 1:50, sc-13133, Santa Cruz, CA, USA). Luego se incubaron con anticuerpo secundario biotinilado anticonejo hecho en cabra o anticuerpo secundario anti-ratón hecho en caballo (Vector Laboratories, CA, EE.UU.) según corresponda. La inmunomarca se generó por el método de estreptavidina-biotina y peroxidasa, según indicaciones del fabricante (DAKO Catalyzed Signal Amplification System, HRP, Dako Cytomation, CA, EE.UU.). Se realizaron controles negativos reemplazando el anticuerpo primario por suero de conejo o ratón según correspondiera. En ninguno de los dos casos se detectó inmunoreactividad.
Cuantificación de los niveles de esteroides en suero de rata Extracción de Testosterona de suero de rata
Para medir los niveles de testosterona en suero de rata, inmediatamente luego de sacrificar al animal por asfixia en cámara de CO , se tomó una muestra de sangre por punción cardíaca. Después de la formación del coágulo el tubo fue centrifugado a 800 x g por 15 minutos a 4°C y el suero obtenido se separó y se reservó a -20°C. Los esteroides se extrajeron del suero mediante una separación en fase orgánica. Para ello se tomó una alícuota de 200 pl de suero y se la colocó en un tubo de vidrio cónico. Se agregaron 2,5 mL de éter etílico (fase orgánica), se agitó en un vórtex en forma continua por 30 segundos y se dejó decantar por 15 minutos a -70°C. La fase orgánica superior conteniendo los esteroides fue recuperada y con la fase inferior (suero) se repitió una vez más el proceso de extracción. Los dos extractos orgánicos se juntaron en un único tubo y se llevó a evaporación bajo flujo continuo de N2, sobre una plancha caliente. El extracto seco se disolvió en 300 pL de buffer RIA y se reservó a -20°C hasta la posterior determinación de testosterona.
Dosaje de esteroides por Radioinunoensayo (RIA)
Para cuantificar los niveles de esteroides en el suero de ratas, se empleó la técnica de radioinmunoensayo (RIA). La cuantificación de testosterona se realizó por duplicado. Se utilizaron anticuerpos específicos previamente titulados para determinar la dilución óptima a usar, correspondiente al 40% de unión de la hormona tritiada de referencia (aproximadamente 10000 cpm). Brevemente, alícuotas de 100 pl del medio de incubación (o de la dilución adecuada) fueron transferidas a tubos de plástico, donde se agregaron 200 pL de buffer RIA (Na2HPO4 40 mM; NaH2PO4 30 mM; NaCl 150 mM; azida sódica 0,01% y gelatina 0,1%; pH 7,0), 100 pL de hormona tritiada y 100 pL de la dilución óptima del anticuerpo. Las muestras fueron incubadas durante 16 h a 4°C. Finalizada la incubación, la hormona libre se separó de la unida al anticuerpo mediante el agregado de 0,2 mL de una suspensión de carbón (Norit A; 0,5% P/V)-dextrano (dextrano 70; 0.05% P/V) en buffer RIA, y posterior centrifugación a 1400 x g durante 10 min. Los sobrenadantes fueron transferidos a viales de conteo, a los que se les agregó 1,5 mL de líquido de centelleo (Opti/Phase Hi Safe 3, ETC, Buenos Aires, Argentina). La radioactividad de los mismos se determinó utilizando un contador de centelleo líquido Perkin-Elmer Tri Carb 2800TR (65% de eficiencia). El rango de utilidad del ensayo fue de 25 a 1600 pg/tubo para progesterona, y de 12,5 a 800 pg/tubo para testosterona (volumen final/tubo: 500 pL). Los coeficientes de variación intra e interensayo en ambos casos fueron menores al 12%.
Cultivo de células de Leydig tumorales R2C
La línea de células de Leydig tumorales de rata R2C fue comprada a la ATCC (# 58649146). Se cultivó en medio rico en nutrientes Ham's/F12, conteniendo 1,2 g/L de bicarbonato de sodio, Glutamina 2 mM, Penicilina 100 U/mL y Estreptomicina 100 pg/mL, suplementado con suero de caballo al 12,5% y suero fetal bovino al 2,5% (medio de crecimiento), a 37°C en una atmósfera de 5% de Co2.
Cuantificación de niveles de mensajero por RT-qPCR
Se trataron células de Leydig tumorales R2C con testosterona (10 pM, disuelta en PBS), calcitriol (1 nM, disuelta en alcohol isopropílico), histamina (1 pM y 1 nM, disuelta en PBS), PBS (control vehículo de T y HA) o alcohol isopropílico (control vehículo del calcitriol) isopropilico, durante 5 h y se determinó mediante RT-qPCR la expresión de RVD. Brevemente, se extrajo RNA total de las células R2C usando TRIzol Reagent (Thermo Fischer Scientific) de acuerdo al protocolo del vendedor. Se realizó la transcripción reversa del RNA usando primers aleatorios y la enzima MMLV (Promega, Madison, WI, EEUU). La PCR en tiempo real se realizó utilizando SYBR Green PCR Master Mix (Roche, Basilea, Suiza) en el equipo Step One Real Time PCR (Applied Biosystems, Foster City, CA, EEUU) usando primers específicos para RVD (5'-TGA CCC CAC CTA CGC TGA CT-3'; 5'-CCT TGG AGA ATA GCT CCC TGT ACT-3, previamente utilizado22). Los parámetros configurados fueron 95°C durante 10 minutos, seguido de 40 ciclos a 95 °C durante 15 segundos, 60 segundos a 60°C. Como gen de referencia para relativizar se utilizó GAPDH (5'- GGG TGT GAA CCA CGA GAA AT -3'; 5'- ACT GTG GTC ATG AGC CCT TC -3', previamente utilizado23).
Análisis estadístico
Los datos fueron analizados usando el programa Graph Pad Prism 6 (Graph Pad Software Inc., CA, EEUU) y contrastados mediante un ANOVA de una vía, seguidos del test de Tukey para comparaciones múltiples. Para comprar la media de dos grupos se utilizó el test T de Student. En todos los casos un p< 0,05 fue considerado estadísticamente significativo para tres ensayos independientes.
RESULTADOS
Expresión del receptor de vitamina D en la ontogenia del testículo de rata.
A los 7 días de edad, se detectó expresión de RVD en los túbulos seminíferos, así como también en las células peritubulares. Particularmente, se observó una marca conspicua en los nidos de células de Leydig fetales (Fig. 1 a). A los 21 días de edad, la inmunomarca en el túbulo seminífero disminuyó, en las células peritubulares se mantuvo, mientras que el intersticio no se detectó (Fig. 1 b). A los 35 días de edad se observó un aumento de la marca en el intersticio, y, particularmente, una clara expresión de RVD en las células de Leydig. Las células peritubulares y el túbulo seminífero mantuvieron la misma expresión que en la edad previa (Fig. 1 c). A los 90 días de edad la rata ya ha alcanzado la pubertad y produce espermatozoides, los cuales se pueden visualizar claramente en la luz del túbulo. A esta edad, se observó un aumento en la expresión de RVD en el intersticio, con marcación abundante en las células de Leydig. Por otro lado, se observó una disminución en la inmunomarca de las células peritubulares y un aumento en el túbulo seminífero. Por último, a los 240 días de edad las células de Leydig mantuvieron una alta expresión de RVD. En las células peritubulares no se vio alterada su expresión y se vio un aumento moderado en el túbulo seminífero (Fig. 1 c).
Contenido endógeno de histamina en células de Leydig en la ontogenia del testículo de rata.
En los testículos de ratas de 7 días se detectó una intensa inmunomarca de HA en nidos de células de Leydig fetales (Fig. 2 a). En los cortes de 21 días de edad se observaron células de Leydig marcadas, pero en menor proporción (Fig. 2 b). A los 35 días de edad se detectó una marca más sutil y difusa en el citoplasma de células de Leydig (Fig. 2 c). A los 90 días de edad la inmunomarca de HA disminuyó en el intersticio, y, particularmente en las células de Leydig no se observó marca en su citoplasma (Fig. 2 d). Este patrón también se obtuvo en los cortes de 240 días de edad (Fig. 2 e).
Concentración de testosterona en suero de rata a distintas edades.
Se observó que conforme aumenta la edad aumenta la concentración de testosterona en suero de ratas macho (Fig. 3).
Expresión del receptor de vitamina D en células de Leydig en testículo humano de distintos grupos etarios y condiciones patológicas.
En las condiciones normales, se observó que en cortes de testículos fetales la expresión de RVD en las células de Leydig fetales resultó positiva, y muy intensa, y menor que en la observada en cortes de neonatales. En el caso del testículo prepuberal se observó un intersticio mayormente negativo (Tabla I).
En cuando a las condiciones patológicas evaluadas, en las hiperplasias de células de Leydig se detectó marca positiva para RVD, pero menor que la observada en el tumor de células de Leydig. Este último, a su vez, poseía una sobreexpresión de RVD, aún mayor que la observada en las células de Leydig fetales (Tabla I).
Modulación in vitro de la expresión génica de RVD en células de Leydig tumorales de rata, R2C.
Con el fin de evaluar la modulación de la expresión génica de RVD, se trataron células de Leydig tumorales de rata (R2C) con posibles estimuladores de la misma, y se analizaron los niveles de expresión relativa. En presencia del estímulo de calcitriol (1 nM) se obtuvo un aumento de 180 veces respecto al control (p< 0,05). En igual medida, se vio un aumento estimulado por testosterona (10 pM) (p< 0,01), mientras que la histamina (1nM) logró producir un aumento significativo de la expresión de RVD (p< 0,05), pero de menor magnitud que testosterona y calcitriol (Fig. 4).
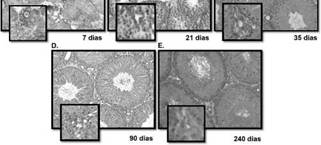
Figura 1: Inmunohistoquímica del receptor de Vitamina D (RVD) en cortes de testículo de rata de distintas edades (expresada en días). Ampliación del intersticio testicular (abajo a la izquierda).
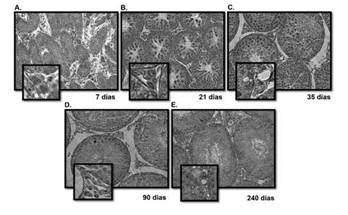
Figura 2: Inmunohistoquímica de Histamina en cortes de testículo de rata de distintas edades (expresada en días). Ampliación del intersticio (abajo a la izquierda).

Figura 3: Concentración de testosterona (pg/mL) en suero de ratas de distintas edades, expresada en días.

Figura 4: Expresión génica relativa del receptor de vitamina D (RVD) en células de Leydig tumorales murinas R2C expuestas a testosterona (10 pM), calcitriol (1 nM) e histamina (1 pM y 1 nM). En todos los casos la expresión génica fue relativizada a la expresión de GAPDH.
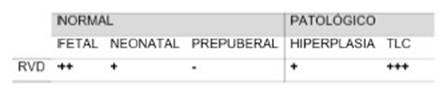
Tabla I Inmunomarcación del receptor de vitamina D (RVD) en células de Leydig en cortes de testículo de humano normales de distintos grupos etarios (fetal, neonatal y prepuberal) y en dos condiciones patológicas (hiperplasia de células de Leydig y tumor de células de Leydig [TLC]).- ausencia de inmunomarcación, + marcación moderada, ++ marcación media, y +++ marcación abundante.
DISCUSIÓN
Previamente se ha relacionado a la VD con la función reproductiva masculina, particularmente con la fertilidad 24’25 y la producción de esteroides sexuales 26’27. En el presente trabajo, se evaluó la expresión del receptor de vitamina D (RVD) en las células de Leydig durante la ontogenia testicular, como un primer paso hacia la comprensión del papel de la VD a lo largo del desarrollo testicular normal.
En mamíferos, las células de Leydig (CL) existen en dos poblaciones, las fetales y las adultas, y se encuentran presentes en distintos momentos del desarrollo testicular 28. Estos tipos celulares difieren en su morfología y propiedades bioquímicas, pero poseen una función en común, la producción de andrógenos. Las células de Leydig fetales (CLF) se desarrollan in utero, y son las responsables de la producción de testosterona gestacional 29, que tiene el rol clave de la diferenciación del sistema urogenital masculino30. En el testículo de rata se pueden identificar grandes nidos de CLF hasta los 21 días de edad 31. Las células de Leydig adultas (CLA) surgen en la pubertad, y provienen de un linaje distinto al de las fetales 32. En este trabajo, en los cortes de rata de 7 y 21 días de edad, fue posible reconocer a las CLF por su ubicación intersticial, su agrupación en nidos y su morfología esférica. Estas células mostraron altos contenidos de histamina endógena (HA) y una elevada expresión de RVD. Esto último se vio replicado en los cortes de testículo fetal y neonatal de humano. Previamente nuestro grupo demostró que las CL de ratas de 7 y 21 días de edad presentan elevados niveles de expresión de la enzima histidina descarboxilasa (HDC), que cataliza la producción de HA11, lo cual explicaría el alto contenido endógeno de HA observado. Asimismo, nuestro grupo reportó que la HA en concentraciones de orden micromolar resulta inhibitoria para la esteroidogénesis en CL, en tanto que concentraciones del orden nanomolar potencian efectos estimulatorios sobre dicho proceso10’33. Teniendo en cuenta estas evidencias, es posible que la HA sea un componente regulador de la producción del pico de andrógenos, secretado por las CLF, responsable de la diferenciación sexual30. Por su parte, RVD podría modular la susceptibilidad de las CL a las acciones de la HA, dado que, unido a ligando, RVD modula la expresión génica de los receptores de HA tipo 1 (HRH1) 9 y tipo 4 (HRH4) 34. Asimismo, RVD podría exacerbar la producción de HA endógena, ya que se ha visto que aumenta la expresión génica de HDC 34. Independientemente, RVD unido a ligando es capaz de inducir la producción de testosterona por parte de las CL35, así como también de modular la expresión de aromatasa y la producción de estrógenos26,27.
Al analizar los cortes de testículo de 35, 90 y 240 días de edad no se encontraron CLF remanentes, y las inmunomarcas observadas se encontraron en CL inmaduras (en el caso de 35 días de edad) o en CLA (en el caso de 90 y 240 días de edad) 36. En dichos tipos celulares no se encontró HA. Nuevamente, estos resultados concuerdan con lo observado para la expresión de HDC, que disminuye en el testículo conforme avanza la edad11. En el caso de RVD, se vio que en CLA su expresión aumentaba con la edad, lo cual fue concordante con el aumento de testosterona sérica (T). Al respecto, si bien se ha correlacionado previamente a la VD y la T, sin poder determinar claramente qué hormona precede a la otra 37, se ha visto que los suplementos de VD aumentan los niveles de T 38, 41. En el testículo prepuberal humano no se detectó expresión de RVD. Esto puede deberse a que en dicho corte no se observaron CLA, sino solo CL inmaduras o incluso progenitoras. Es posible que RVD cumpla un rol como modulador de la esteroidogénesis luego de la pubertad, asociado a CLA, pero no a CL de estadios menos diferenciados.
En trabajos previos se ha reportado que la VD es un importante modulador de la diferenciación celular y la proliferación de células normales y tumorales, y que es capaz de regular la proliferación, apoptosis y adhesión celular en distintos tipos de células tumorales, modificando la capacidad de angiogénesis, invasión y metástasis 42, 45. Por ello, en este trabajo se analizó la presencia de RVD en hiperplasia de CL y tumores de CL (TCL). Particularmente en el caso de las hiperplasias, se observó que presentaban inmunomarca de RVD. Las hiperplasias de CL se originan a partir de una desregulación de la relación entre LH (hormona luteinizante) y T. A su vez, se ha visto que los ratones knockout para RVD desarrollan más hiperplasias de CL46. Esto plantea a posibilidad de que la VD regule la relación entre LH y T, y en condiciones de hipovitaminosis, este balance se pierda dando lugar a la hiperplasia. Sin duda, estudios más profundos permitirán corroborar esta hipótesis.
En base a las publicaciones que muestran una correlación entre la hipovitaminosis D, y la incidencia y supervivencia en cáncer 18, 47, 53, se ha propuesto al calcitriol, compuesto activo de VD, como tratamiento oncológico (a modo preventivo y en combinación con otras terapias) 54, 56. En concordancia, si bien en el presente trabajo no fue posible saber si el origen del TCL tenía relación con los niveles séricos de VD, se detectó alta expresión de RVD. Por otro lado, resultados previos empleando la línea de células de Leydig tumorales de rata R2C - el modelo más ampliamente utilizado para el estudio de Leydigiomas -mostraron que el tratamiento con calcitriol disminuye la expresión de aromatasa34, que se encuentra aumentada en TCL23, y al mismo tiempo aumenta los niveles del receptor HRH1, que media la respuesta antiproliferativa de HA34 (en contraposición a la respuesta proliferativa que se produciría por la unión de la HA al receptor HRH2)10. A su vez, en este trabajo se observó que tanto la T como la HA fomentan la expresión de RVD en R2C. Estos hallazgos permitirían explicar la sobreexpresión de RVD observada en el TCL estudiado, ya que los TCL sintetizan esteroides en forma constitutiva y poseen elevados niveles de HDC 57. Se ha postulado que RVD en ausencia de ligando, aumenta la proliferación celular, y que este efecto se disipa en presencia de ligando 58. Así, la sobreexpresión de RVD en condiciones de hipovitaminosis resultaría contraproducente. Esta observación cobra mayor importancia si se considera que la prevalencia de la deficiencia de la vitamina D (VD) es más alta de lo que tradicionalmente se ha supuesto, inclusive en regiones tropicales donde hay mejor exposición solar. Esta deficiencia se está convirtiendo en una situación epidémica en aumento, aún no bien reconocida, con serias implicancias en la salud de la población 13,48,59.
En conjunto, nuestros hallazgos sugieren que la VD está involucrada en múltiples vías en las CL, como lo son la esteroidogénesis y la regulación del sistema histaminérgico, en condiciones normales y patológicas. Resulta entonces prometedor considerar a la VD como un posible tratamiento adicional en TLC, lo cual amerita la realización de estudios más exhaustivos al respecto.














