INTRODUCCIÓN
El enfoque de los pacientes con carcinoma diferenciado de tiroides (CDT) presentó un cambio radical en los últimos años, con una tendencia mundial hacia el tratamiento y seguimiento individualizado de acuerdo al riesgo de recurrencia (RR) de la enfermedad (1,2). La estratificación por RR fue propuesta casi concomitantemente por la American Thyroid Association (ATA) y por la Sociedad Latinoamericana de Tiroides (SLAT), entre otras sociedades en el mundo (1-5). Estos sistemas de clasificación, originalmente diseñados para establecer la probabilidad de respuesta estructural incompleta, fueron adicionalmente validados para ser predictivos de múltiples otros resultados clínicos importantes en el seguimiento del paciente con CDT: la frecuencia de respuesta inicial excelente, de recurrencia luego de haber alcanzado esta respuesta, y la de ser considerado sin evidencia de enfermedad a largo plazo (2, 510). Por otra parte, varios investigadores demostraron que la clasificación estática del riesgo de recurrencia inicial podría mejorarse aplicando el denominado riesgo dinámico, que resulta de adicionar al RR estático inicial, los hallazgos que aparecen en el seguimiento del paciente (6,7,11). Este riesgo dinámico adiciona: i) los niveles de tiroglobulina (Tg) hallados luego de la cirugía (12) al momento de la ablación con radioyodo, ii) los medidos en la respuesta inicial al tratamiento bajo terapia hormonal de reemplazo y, iii) los hallazgos ecográficos, entre otras variables, las que podrían modificar la probabilidad inicial de presentar una respuesta estructural incompleta en el seguimiento (2).
Históricamente, en Latinoamérica, la administración de RAI fue rutinaria en todos los pacientes independientemente del RR, y recién en el año 2009, con la publicación de las guías regionales, comenzó a implementarse un menor uso de radioyodo en pacientes con microcarcinomas unifocales (3). Los pacientes de bajo riesgo de recurrencia que han recibido RAI tienen una frecuencia de respuesta estructural incompleta que oscila entre el 3 al 7%. De hecho, todos los pacientes incluidos en nuestra base de datos hasta el año 2011 habían recibido RAI. Actualmente, el 15% de los pacientes de nuestra base de datos no recibió RAI luego de la TT, lo que demuestra el cambio ocurrido luego de la implementación de estas guías internacionales y nacionales (1-3,5).
La ablación con radioyodo no demostró reducir la mortalidad ni prolongar la sobrevida libre de enfermedad en esta población, aunque probablemente podría facilitar el seguimiento. Por otro lado, es cuestionable la necesidad de efectuar ablación con el objetivo de facilitar la detección temprana de recurrencia, ya que ésta será fácilmente evidenciable por la tendencia de tiroglobulina y su anticuerpo, y por la ecografía de la región cervical (2).
La evaluación de la respuesta inicial al tratamiento (usualmente entre los 6-18 meses) es una herramienta utilizada para redefinir conductas terapéuticas y de seguimiento a largo plazo, las cuales fueron ampliamente descriptas y validadas para pacientes tratados con tiroidectomía total (TT) y ablación con radioyodo (RAI) (6-10). En el año 2014, Momesso y Tuttle (13) propusieron por primera vez las definiciones de respuestas al tratamiento para pacientes tratados con lobectomía y/o tiroidectomía total sin RAI. Sin embargo, son escasos los estudios que validan las respuestas en pacientes no ablacionados, entre ellos la reciente publicación de validación en nuestra población no ablacionada con RAI (14,15,16).
Los objetivos de esta investigación fueron: i) comparar pacientes ablacionados de bajo riesgo y riesgo intermedio de recurrencia inicial y de alto riesgo dinámico en el seguimiento con aquellos no ablacionados de bajo riesgo dinámico, ii) comparar la población de ablacionados de bajo riesgo inicial con aquellos no ablacionados de bajo riesgo dinámico.
PACIENTES Y MÉTODOS
Se incluyeron pacientes mayores de 18 años, con carcinoma papilar de tiroides, de bajo riesgo y riesgo intermedio de recurrencia según ATA (2), con un período de seguimiento mínimo de 12 meses. Adicionalmente, cada paciente debía contar con al menos dos determinaciones de Tg y anticuerpos antitiroglobulina (aTg).
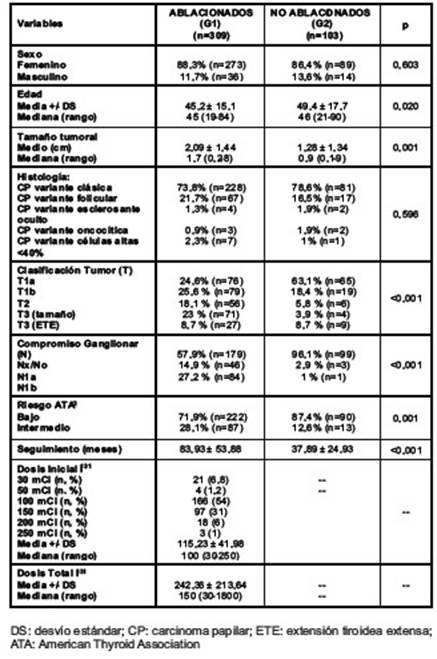
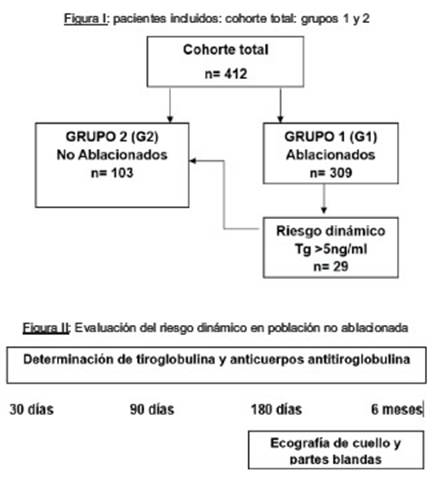
Fueron incluidos 412 pacientes, 309 ablacionados (Grupo 1: G1), y 103 no ablacionados (Grupo 2: G2). El 22% (n=29) pacientes del G2 con niveles de Tg bajo terapia hormonal > 5 ng/ml en el riesgo dinámico fueron ablacionados (Figura I). El G1 incluyó a nuestra cohorte histórica de pacientes de bajo riesgo y riesgo intermedio de recurrencia que hasta el año 2011 habían recibido RAI inmediatamente luego de la cirugía, la mayoría de estos pacientes fueron ablacionados con dosis > 100 mCi (Tabla I). El G1 incluyó además aquellos de alto riesgo dinámico en el seguimiento (9,4% de la población total del G1). Desde ese momento hasta la actualidad, la decisión de ablación se basó en el riesgo dinámico (6).
Evaluación del riesgo dinámico en pacientes no ablacionados (G2)
La evaluación luego del tratamiento inicial se realizó con la medición de Tg y aTg aproximadamente a los 30, 90 y 180 días postquirúrgicos, y posteriormente, de manera semestral. A partir del sexto mes de seguimiento, se adicionó ecografía de partes blandas de cuello con un transductor lineal de 11 MHz, la cual se repitió semestralmente (Figura II).
Riesgo dinámico
Luego de definir la respuesta inicial al tratamiento, los pacientes se re-clasificaron de acuerdo a la estratificación por riesgo dinámico en bajo riesgo dinámico o baja probabilidad de recurrencia y alto riesgo dinámico o elevada probabilidad de recurrencia (6).
Bajo riesgo dinámico: se aplicaron los siguientes criterios para definir esta variable:
a) Respuesta inicial excelente b) Niveles de Tg bajo terapia hormonal < 5 ng/mL c) Niveles estables o decrecientes de Tg en el tiempo o niveles estables o decrecientes de aTg, medidos con la misma metodología,
Alto riesgo dinámico: se aplicaron los siguientes criterios para definir esta variable:
a) Respuesta estructural incompleta inicial, b) Niveles de Tg > 5 ng/mL bajo terapia hormonal, c) Niveles de Tg crecientes bajo terapia hormonal o tras estimulación durante el seguimiento, d) Niveles crecientes de aTg medidos por la misma metodología.
Medición de Tg y aTg
Los valores de Tg se midieron con método quimioluminiscente (ICMA Immulite 2000) con una sensibilidad analítica (SA) de 0,2 ng/ml y una sensibilidad funcional (SF) de 0,3 ng/ml, y por método electroquimioluminiscente (ICMA) Elecsys 1010 (Roche) con una SA de 0,04 ng/ml y SF de 0,1 ng/ml. Los ensayos para medición de aTg fueron el método electroquimioluminiscente Elecsys Anti-Tg (RSR Ltd., Pentwyn, Cardiff, UK), y el método quimioluminiscente Immulite 2000 Anti-TG Ab (Siemens). Para ambos ensayos, los valores >20 UI/mL se consideraron positivos.
Estadificación inicial
Para la clasificación de RR se utilizaron los lineamientos de la American Thyroid Association (2), la cual define como i) bajo riesgo: pacientes con tumores intratiroideos, N0 clínico ó N1 < 5 con micrometástasis (<0.2 cm), ausencia de metástasis locales y a distancia, sin histología agresiva y resección macroscópica completa; ii) riesgo intermedio: pacientes con tumores con invasión microscópica de tejidos blandos peritiroideos, histología agresiva, invasión vascular (<4 focos), N1 clínico o > 5 ganglios comprometidos < 3 cm.
El riesgo de mortalidad fue establecido con el Sistema de Estadificación de la American Joint Committee on Cancer /International Union against Cancer (AJCC/UICC) 8va ed, (Estadios TNM I, II, III, IV) (17).
Respuesta inicial y al final del seguimiento en grupo de pacientes ablacionados (G1): se evaluó la respuesta luego del tratamiento quirúrgico y la ablación con radioyodo. Se consideraron los valores de Tg bajo terapia hormonal, de Tg estimulada luego de la suspensión hormonal o la administración de TSH recombinante (rhTSH), los hallazgos de la ecografía de cuello, del rastreo corporal diagnóstico o de las imágenes seccionales (Tomografía Axial Computada, FDG-PET/TC y/o Resonancia Magnética Nuclear) si se hubieran realizado. Se definieron según los lineamientos de la ATA (2).
Respuesta Inicial al Seguimiento: Excelente (RE): Tg bajo terapia hormonal (TH) y estimulados <1 ng/ml y anticuerpos antitiroglobulina (aTg) negativos, Rastreo corporal total diagnóstico con 2-5 mCi 131I demostrando captación ausente o <0,1 % en el lecho tiroideo, ecografía de cuello y partes blandas sin evidencia de alteraciones; Indeterminada (RI): niveles de Tg indetectables bajo TH y estimulados entre 1-10 ng/ml sin evidencia clara de enfermedad estructural, aTg estables o en descenso medidos por la misma metodología y / o alteraciones inespecíficas por imágenes; Bioquímica incompleta (RBI): Tg bajo TH >1 ng/ml y/o estimulada, tras suspensión hormonal o rhTSH, mayores a 10 ng/ml, o niveles aTg crecientes medidos por la misma metodología, sin hallazgos patológicos o inespecíficos en la ecografía de partes blandas de cuello; Estructural incompleta (REI): evidencia de enfermedad loco-regional o metástasis a distancia.
Respuesta al final del seguimiento: Sin evidencia de enfermedad (SEE): cuando se reunían las mismas características de respuesta excelente inicial, luego de 36 meses de seguimiento. Las definiciones de Respuesta indeterminada, bioquímica incompleta y estructural incompleta fueron las mismas que las utilizadas para la respuesta inicial al tratamiento.
Respuesta inicial y al final del seguimiento en grupo no ablacionados (G2): para la evaluación de las respuestas al tratamiento se usaron las definiciones previamente publicadas y validadas (13, 14, 15). Se definieron las respuestas como: Excelente (RE): Tg bajo terapia hormonal (TH) <0,2 ng/ml o estimulada <2 ng/ml con anticuerpos antitiroglobulina (aTg) negativos; Indeterminada (RI): Tg bajo TH entre 0,2 ng/ml y 5 ng/ml, Tg estimulada entre 2 y 10 ng/ml, o pacientes con niveles de aTg estables o en descenso, con hallazgos inespecíficos por imágenes; Bioquímica incompleta (RBI): Tg bajo TH >5 ng/ml o estimulada >10 ng/ml, o niveles de Tg o aTg en ascenso con niveles similares de TSH, e imágenes negativas; Estructural incompleta (REI): evidencia de enfermedad loco-regional o metástasis a distancia.
RESULTADOS
Las características basales de los pacientes ablacionados (G1) y no ablacionados (G2) pueden observarse en la Tabla I. En ambas poblaciones predominó el sexo femenino. La media de tamaño tumoral fue de 2,09 ± 1,44 cm en ablacionados, y 1,28 ± 0,53 cm en no ablacionados (p=0,001). Hubo compromiso ganglionar (N1a/b) en el 42,1% del G1, y en el 3,9% del G2 (p=<0,001). Histológicamente predominó el carcinoma papilar (CP) variante clásica en ambas poblaciones, seguido por el CP variante folicular. En la cohorte no ablacionada el 87,4% y el 12,6%, y en la población ablacionada el 71,9 y el 28,1% fueron clasificados como bajo e intermedio RR, basados en la American Thyroid Association. El seguimiento en meses fue de 83,93 ± 53,88 en G1, y 37,89 ± 24,93 en G2 (p=<0,001).
Evaluación comparativa de pacientes ablacionados (pacientes de bajo riesgo y riesgo intermedio estático y alto riesgo dinámico) y no ablacionados de bajo riesgo dinámico
Respuesta inicial
Los pacientes del G1 presentaron una respuesta inicial excelente en el 44,6% de los casos, y el 16,5% presentó una respuesta inicial estructural incompleta. Por otro lado, el 27,8% de los pacientes presentaron inicialmente una respuesta indeterminada, y el 11% respuesta bioquímica incompleta. Los pacientes pertenecientes al G2 presentaron una respuesta inicial excelente en el 55,3%, e indeterminada en el 44,7% de los casos. En este grupo ningún paciente presentó respuesta bioquímica ni estructural incompleta (Figura III).
Respuesta al final del seguimiento
Los pacientes ablacionados (G1) evolucionaron con una respuesta excelente en el 62,1% de los casos, comparados con el 72,8% en el grupo de pacientes no ablacionados (G2) (p=0,058). Por otro lado, los pacientes del G1 presentaron una respuesta estructural incompleta en el 11,3% comparado al 0,9% en el G2 (p=<0,001).
Con respecto a las respuestas indeterminada y bioquímica incompleta, estas fueron del 20% y 6,5% en el G1, y del 24,3% y 1,9% en el G2, respectivamente (Figura IV).
Evaluación comparativa de pacientes ablacionados de bajo riesgo de recurrencia inicial y no ablacionados de bajo riesgo dinámico
Los pacientes ablacionados de bajo riesgo de recurrencia inicial presentaron una frecuencia de respuesta estructural incompleta del 3%, y los no ablacionados de bajo riesgo dinámico del 0,9% (p=0,366) (Figura V).
DISCUSIÓN
Las validaciones de las respuestas al tratamiento en pacientes tratados con TT y RAI demostraron que un paciente de bajo riesgo puede presentar una frecuencia de respuesta excelente al final del seguimiento entre 78-91% y estructural incompleta entre el 3-9%; y un paciente de riesgo intermedio entre 52-63% y 21-34%, respectivamente (6-9,11).
Nuestra hipótesis respecto a la elevada frecuencia de respuesta estructural incompleta observada en este estudio en pacientes
tratados con radioyodo comparados con los no ablacionados se relacionaría con la inclusión en el grupo de pacientes ablacionados de pacientes de alta probabilidad de recurrencia definidos con el riesgo dinámico. Por otro lado, la baja frecuencia de respuesta estructural incompleta en pacientes no ablacionados comparados con aquellos de bajo riesgo y riesgo intermedio tratados con radioyodo se relacionaría a la adecuada selección de aquellos que no se beneficiarían con la ablación con radioyodo.
La aplicación del riesgo dinámico de recurrencia en nuestro estudio constituyó una herramienta útil para predecir con mayor certeza la probabilidad de respuesta excelente al final del seguimiento, comparado con los sistemas estáticos de clasificación de RR iniciales. En la mayoría de los pacientes no ablacionados incluidos en este estudio, los niveles de Tg evolucionaron espontáneamente a niveles indetectables, lo que demuestra el beneficio de la evaluación dinámica para decidir la RAI.
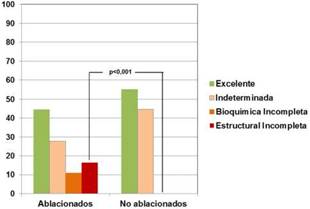
Figura III: Evaluación comparativa de la respuesta inicial al seguimiento en pacientes ablacionados de bajo riesgo y riesgo intermedio de recurrencia inicial y no ablacionados de bajo riesgo dinámico
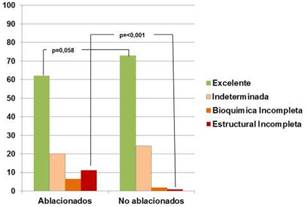
Figura IV: Evaluación comparativa de la respuesta al Anal del seguimiento en pacientes ablacionados de bajo riesgo y riesgo intermedio de recurrencia inicial y no ablacionados de bajo riesgo dinámico
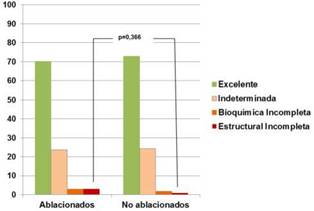
Figura V: Evaluación comparativa de pacientes ablacionados de bajo riesgo inicial y no ablacionados de bajo riesgo dinámico
CONCLUSIONES
Los pacientes ablacionados de bajo riesgo dinámico presentan una mayor frecuencia de respuesta excelente cuando se los compara con los pacientes ablacionados de bajo riesgo y riesgo intermedio de recurrencia estático. Esto demuestra que el riesgo dinámico es una herramienta efectiva en pacientes con CDT tratados con tiroidectomía total sin ablación con radioyodo. La decisión de la ablación con radioyodo debiera realizarse en pacientes con estos RR utilizando el riesgo dinámico ya que esta situación no amerita una conducta postquirúrgica inmediata ni urgente. Cuando estos pacientes son apropiadamente seleccionados tienen un pronóstico excelente con una baja frecuencia de respuesta estructural incompleta en el seguimiento. Esta frecuencia de respuesta estructural incompleta es inclusive menor a la observada en pacientes de bajo riesgo estático ablacionados.
Declaración de conflicto de intereses
Fabián Pitoia es consultor de los laboratorios Bayer, Genzyme-Sanofi y Raffo. El resto de los autores no presenta conflictos de interés.
Aspectos éticos referidos al paciente
Para esta publicación se contó con el consentimiento informado de los pacientes.