Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680
Medicina (B. Aires) vol.75 no.5 Ciudad Autónoma de Buenos Aires oct. 2015
CASUÍSTICA
Tratamiento exitoso con fondaparinux en trombocitopenia inducida por heparina y trombosis
Carina E. Seculini Patiño1, María Florencia Pascualini2, Aldo H. Tabares3, 4
1Servicio de Clínica Médica,
2Servicio de Dermatología,
3Servicio de Medicina Vascular y Trombosis, Hospital Privado Centro Médico de Córdoba,
4Instituto Universitario de Ciencias Biomédicas de Córdoba (IUCBC), Córdoba, Argentina
Dirección postal: Dra. Carina E. Seculini Patiño, Servicio de Clínica Médica, Hospital Privado Centro Médico de Córdoba, Av. Naciones Unidas 346, 5016 Córdoba, Argentina
e-mail: cari_seculini@hotmail.com
Recibido: 30-III-2015
Aceptado: 22-VI-2015
Resumen
La trombocitopenia inducida por heparina (TIH) es una reacción adversa inmunológica caracterizada por trombocitopenia y la asociación paradojal de trombosis arterial o venosa. Es causada por la formación de anticuerpos IgG contra el complejo multimolecular de heparina-factor plaquetario 4 (FP4). Fondaparinux es un inhibidor selectivo del factor Xa que tiene escasa afinidad por el FP4 y posee un menor potencial para inducir una respuesta inmunológica, haciendo del mismo un agente potencialmente útil en el tratamiento de la TIH. Se presenta el caso de una mujer de 73 años con TIH asociada a fenómenos trombóticos arteriales y venosos, que recibió exitosamente fondaparinux, con normalización del recuento plaquetario y sin progresión trombótica.
Palabras clave: Trombocitopenia inducida por heparina; Fondaparinux; Trombosis; Anticuerpos anti factor plaquetario 4.
Abstract
Successful treatment with fondaparinux in heparin-induced thrombocytopenia and thrombosis.
Heparin induced thrombocytopenia (HIT) is an immune-mediated adverse reaction characterized by thrombocytopenia and paradoxical arterial or venous thrombosis, due to the formation IgG antibodies directed to a multimolecular complex of heparin-platelet factor 4 (PF4). Fondaparinux is a selective factor Xa inhibitor with little affinity for PF4 and thus less likely to induce an immune response, making fondaparinux a potentially useful drug for the treatment of HIT. Herein we report the case of a 73 years old woman with HIT associated with arterial and venous thrombosis that was successfully treated with fondaparinux, with normalization of the platelet countand without progression of thrombosis.
Key words: Heparin induced thrombocytopenia; Fondaparinux; Thrombosis; Anti PF4 antibodies.
Las heparinas son los anticoagulantes parenterales más utilizados en la actualidad. La complicación más temida es la hemorragia; sin embargo, la trombocitopenia inducida por heparina (TIH) es una reacción adversa poco frecuente pero grave del tratamiento con cualquier tipo de heparina.
La TIH es una condición clínica caracterizada por trombocitopenia moderada y la asociación paradojal de trombosis arterial o venosa. Es causada por una reacción inmunológica con la formación de anticuerpos IgG contra el complejo multimolecular de heparina-FP4 con capacidad de activar las plaquetas y el endotelio vascular1.
Su reconocimiento permite la discontinuación inmediata de la heparina y la instauración de tratamiento anticoagulante alternativo para evitar la progresión y formación de nuevos trombos y sus complicaciones, como la amputación de un miembro y en ocasiones la muerte2-4.
En EE.UU. los medicamentos aprobados para el tratamiento de la TIH son los inhibidores directos de la trombina5, pero los mismos no están disponibles en Argentina.
El fondaparinux es un pentasacárido sintético inhibidor selectivo del factor X de administración parenteral. Tiene escasa afinidad por el FP4, y dado su bajo peso molecular posee un menor potencial para inducir una respuesta inmunológica.
Presentamos el caso clínico de una mujer de 73 años con TIH asociada a fenómenos trombóticos, que recibió exitosamente fondaparinux, con normalización del recuento plaquetario y sin progresión trombótica.
Caso clínico
Mujer de 73 años con hipertensión arterial en tratamiento con enalapril 10 mg día y poliquistosis renal, sometida a un reemplazo total de cadera derecha secundario a artrosis; recibió profilaxis para trombosis venosa profunda con heparina sódica 5000 U cada 12 horas durante los 5 días de internación. Fue dada de alta con heparina cálcica subcutánea 5000 U cada 12 horas.
A los 38 días posterior al alta y recibiendo la profilaxis, fue internada por presentar trombosis venosa profunda en ambos miembros inferiores comprometiendo la cava inferior por debajo de venas renales y trombosis de vena subclavia izquierda. La paciente recibió tratamiento con HNF intravenosa, a las 48 horas se objetivó caída del recuento plaquetario a 30000 mm3 asociado a trombosis arterial con isquemia de antepié y dígitos del pie derecho, mano izquierda y tercer dedo del pie izquierdo con pulso pedio, tibiales posteriores y radiales presentes (Figs. 1 y 2).
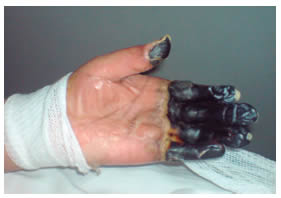
Fig 1. Lesión necrótica por trombosis e isquemia en pulpejo del primer dedo, segundo, tercer cuarto y quinto dedo de la mano izquierda
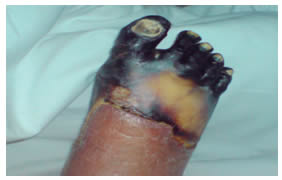
Fig. 2. Lesión necrótica por trombosis e isquemia de antepié y dígitos del pie derecho.
Se realizaron estudios de trombofilia y anticuerpos antifosfolípidos que fueron negativos, y se documentó la presencia de títulos elevados de anticuerpos poliespecíficos contra heparina-FP4 por ELISA.
Se decidió suspender la HNF e iniciar tratamiento con fondaparinux sódico (ARIXTRA®Glaxo-SmithKline) 7.5 mg/día hasta la normalización plaquetaria, continuándose en conjunto con acenocumarol por vía oral hasta lograr el rango terapéutico. Las plaquetas retornaron a sus niveles basales de 350 000/mm3 al cuarto día de suspendida la heparina. Durante la terapia con fondaparinux no se observó progresión de la trombosis, eventos hemorrágicos ni otra manifestación adversa.
El tratamiento de las lesiones necróticas fue quirúrgico, mediante la amputación transmetacarpiana del segundo, tercer, cuarto, quinto y pulpejo del primer dedo de la mano izquierda y del tarso-metatarso del pie derecho.
Discusión
Presentamos un caso que ilustra las manifestaciones clínicas más graves de TIH como la trombosis venosa y el compromiso arterial. Esta paciente fue expuesta a HNF en dosis profilácticas por 38 días, y recibiendo profilaxis presentó una trombosis venosa extensa de los miembros inferiores con compromiso de la vena cava inferior y la vena subclavia izquierda, asociados a una disminución en la cuenta plaquetaria2, 6. La exposición prolongada a HNF en el postoperatorio de cirugía ortopédica y su posterior re-exposición para el tratamiento de la trombosis venosa agravaron los síntomas con compromiso arterial y subsiguiente necrosis digital. La asociación de trombocitopenia moderada, trombosis arterial, venosa, y la ausencia de otras causas de trombocitopenia en un paciente expuesto a la heparina, constituyen criterios de una alta probabilidad clínica de TIH basados en el score de 4T7. En estas circunstancias es imperativo la suspensión de la heparina y el uso de anticoagulantes alternativos como el argatroban, danaparoid, y cuando estos no están disponibles, el fondaparinux5.
La TIH es una reacción adversa poco frecuente pero potencialmente grave del tratamiento con heparina. La incidencia es variable del 0.5-5.0% según el tipo de heparina utilizada. Es hasta diez veces más frecuente en los pacientes tratados con HNF intravenosa que los tratados con HBPM6.
En la fisiopatología está involucrada la formación de anticuerpos contra el complejo heparina-FP4 que se unen al receptor Fcγ-IIa de las plaquetas activándolas; también se produce activación del endotelio vascular, los monocitos y la cascada de la coagulación, induciendo un aumento en la generación de trombina1. Estas alteraciones explicarían la trombocitopenia y los eventos trombóticos observados en la TIH.
La trombocitopenia es moderada con una caída del 50% del recuento plaquetario y ocurre 5-10 días post-exposición a la heparina, aunque en algunos pacientes con exposición previa las reacciones pueden ocurrir en minutos a horas2.
Las complicaciones tromboembólicas pueden ser arteriales, venosas o ambas2-4. El diagnóstico se basa en datos clínicos e inmunológicos: el descenso plaquetario en relación temporal al uso de heparina, las lesiones en piel en el sitio de inyección o una reacción sistémica luego de la administración endovenosa, asociados a serología positiva con la demostración de anticuerpos contra el complejo heparina- FP48.
Para facilitar el diagnóstico, es común utilizar un score clínico conocido como "sistema de puntuación 4 T" el cual permite determinar la probabilidad pretest de esta entidad, y por lo tanto decidir la continuidad o no de la heparina utilizada8.
El tratamiento de la TIH se basa en la suspensión de la HNF o HBPM y el inicio de anticoagulantes alternativos. Hay dos clases: los inhibidores directos de la trombina como el argatrobán y la lepirudina, y los heparinoides como el danaparoide. En la fase aguda no se recomienda el uso de dicumarínicos, ya que los mismos pueden inducir gangrena de los miembros5.
Actualmente los únicos anticoagulantes aprobados por la Food and Drug Administration (de EE.UU.) para el tratamiento de la TIH son los inhibidores directos de la trombina, ya que carecen de sensibilidad cruzada con las heparinas y, por tanto, se han convertido en la terapia estándar de pacientes con TIH en ese país5.
Los inhibidores directos de la trombina son costosos, requieren una infusión por vía intravenosa continua y pueden ser monitorizados con un aPTT que no se encuentran disponibles en Argentina, por lo que se necesitan otros fármacos para el tratamiento de la TIH9.El fondaparinux es un pentasacárido sintético con actividad antitrombótica por inhibición selectiva del factor Xa mediado por la antitrombina III. A diferencia de la HNF y HBPM, tiene escasa afinidad por FP4, y por ende, una menor probabilidad de inducir una respuesta inmunológica como la observada en TIH, por lo que puede ser considerado una alternativa válida para el tratamiento de pacientes con TIH. Las pautas publicadas en el 2012 por "American College of Chest Physician", reconocen al fondaparinux como tratamiento alternativo para pacientes con TIH5.
El fondaparinux está aprobado para la profilaxis de trombosis venosa profunda en pacientes operados de cirugía abdominal, fractura de cadera, reemplazo de rodilla, y para tratamiento del tromboembolismo pulmonar agudo10. Su biodisponibilidad por vía subcutánea es del 100% con vida media de 17 horas que permite administrarlo una vez al día, no requiere monitorización frecuente ni ajuste de dosis y es menos costoso que los inhibidores de la trombina parenterales. Dado que la eliminación es predominantemente renal está contraindicado en pacientes con insuficiencia renal severa11.
La experiencia del fondaparinux en el tratamiento de TIH es escasa, se fundamenta principalmente en reportes de casos o estudios retrospectivos con pocos pacientes y seguimiento a corto plazo. Un estudio retrospectivo reciente con un importante número de pacientes con sospecha de TIH mostró que el fondaparinux tiene una efectividad y seguridad similar al argatroban y danaparoide12.
Hay casos comunicados de TIH asociada al uso de fondaparinux, la misma es improbable ya que "in vitro" los anticuerpos no muestran reactividad cruzada y muy probablemente no tengan importancia clínica. Aunque controvertido, se ha sugerido la posibilidad de TIH "espontanea", es decir aquella que ocurre en ausencia de exposición a la heparina y presenta hallazgos serológicos similares13. Recientemente se ha documentado la formación de complejos de FP4 con ácidos nucleicos y los mismos pueden inducir anticuerpos similares a los observados en los pacientes con TIH secundarios a la exposición a heparina14.
En nuestro medio carecemos de danaparoide y de inhibidores directos de la trombina, por lo cual el fondaparinux podría ser una alternativa para el tratamiento y la profilaxis de episodios trombóticos en pacientes con TIH confirmada.
La introducción de los inhibidores orales de la trombina, como el dabigatrán, y los inhibidores del factor Xa, como el rivaroxaban y apixaban, abren nuevas avenidas para el tratamiento de la TIH14. Estudios in vitro confirman la ausencia de reactividad cruzada con los anticuerpos anti heparina-PF4; en informes de casos han mostrado efectividad y se planean estudios para documentar su eficacia y seguridad15.
Serían necesarios estudios prospectivos y controlados que evalúen la eficacia y seguridad del fondaparinux en TIH, antes de que esta recomendación sea de uso rutinario.
Conflicto de intereses: Ninguno para declarar
1. Warkentin TE, Hayward CP, Boshkov LK, et al. Sera from patients with heparin-induced thrombocytopenia generate platelet-derived microparticles with procoagulant activity: an explanation for the thrombotic complications of heparin-induced thrombocytopenia. Blood 1994;84: 3691-9. [ Links ]
2. Warkentin TE. Heparin-induced thrombocytopenia: a clinicopathologic syndrome. Thromb Haemost 1999; 82: 439-47. [ Links ]
3. Greinacher A, Volpel H, Janssens U, et al. Recombinant hirudin (lepirudin) provides safe and effective anticoagulation in patients with heparin-induced thrombocytopenia: a prospective study. Circulation 1999; 99: 73-80. [ Links ]
4. Lewis BE, Wallis DE, Leya F, Hursting MJ, Kelton JG. Argatroban anticoagulation in patients with heparin-induced thrombocytopenia. Arch Intern Med 2003; 163: 1849-56. [ Links ]
5. Linkins LA, Dans AL, Moores LK, et al. Treatment and prevention of heparin-induced thrombocytopenia: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141: 495S-530S. [ Links ]
6. Jang IK, Hursting MJ. When heparins promote thrombosis: review of heparin-induced thrombocytopenia. Circulation 2005; 111: 2671-83. [ Links ]
7. Lo GK, Juhl D, Warkentin TE, Sigouin CS, Eichler P, Greinacher A. Evaluation of pretest clinical score (4 T´s) for diagnosis of heparin-induced thrombocytopenia in two clinical settings. J Thromb Haemost 2006; 4: 759-65. [ Links ]
8. Martinuzzo ME, Cerrato GS, Iglesias Varela ML, Adamczuk YP, Pombo G, Forastiero RR. Levels of antiplatelet factor 4-heparin antibodies and 4T score for heparin induced thrombocytopenia. Medicina (B Aires) 2012; 72: 19-22. [ Links ]
9. Warkentin TH, Greinacher A (Editors).Fundamental and Clinical Cardiology Series: Heparin-Induced Thrombocytopenia. Fifth Edition, Boca Raton, Fl: CRC Press, 2012. [ Links ]
10. Papadopoulos S, Flynn JD, Lewis DA. Fondaparinux as a treatment option for heparin-induced thrombocytopenia. Pharmacotherapy 2007; 27: 921-26. [ Links ]
11. Donat F, Duret JP, Santoni A, et al. The pharmacokinetics of fondaparinux sodium in healthy volunteers. Clin Pharmacokinet 2002; 41: 1-9. [ Links ]
12. Kang M, Alahmadi M, Sawh S, Kovacs MJ, Lazo-Langner A. Fondaparinux for the treatment of suspected heparin-induced thrombocytopenia: a propensity score-matched study. Blood 2015: 125; 924-9. [ Links ]
13. Warkentin TE, Basciano PA, Knopman J, Bernstein RA. Spontaneous heparin-induced thrombocytopenia syndrome: 2 new cases and a proposal for de defining this disorder. Blood 2014; 123: 3651-4. [ Links ]
14. Jaax ME, Krauel K, Marschall T, et al. Complex formation with nucleic acids and aptamers alters the antigenic properties of platelet factor 4. Blood 2013; 122: 272-81. [ Links ]
15. Linkins LA, Warkentin TE, Pai M, et al. Design of the rivaroxaban for heparin-induced thrombocytopenia study. J Thromb Thrombolysis 2014; 38: 485-92. [ Links ]













