La apnea obstructiva del sueño (AOS) constituye un trastorno respiratorio crónico de gran relevancia en la población general. Es una enfermedad cuya prevalencia en adultos se estima en 22% en hombres y 17% en mujeres, de acuerdo a la revisión del 2015 realizada por Franklin y col.1. En un estudio efectuado en Sao Paulo, Brasil, se halló que un tercio de la población general padecía AOS2.
La evaluación objetiva mediante polisomnografía (PSG) vigilada por personal técnico especializado (nivel I de la clasificación de la Academia Americana de Medicina del Sueño), es actualmente el estándar de referencia para el diagnóstico de la AOS3-4. Sin embargo, se han desarrollado dispositivos portátiles para registrar parámetros de sueño sin supervisión técnica en tiempo real (clasificados como estudios de nivel II) describiéndose en ellos una buena calidad de las señales neurológicas y respiratorias, con adecuada correlación con parámetros fisiológicos cuando se compararon en el laboratorio de sueño vs. registros obtenidos en el domicilio del paciente5,6.
La eficiencia del sueño relaciona el tiempo total de sueño con el tiempo pasado en la cama. Varias publicaciones hacen referencia a que la calidad de sueño sería menor en el laboratorio de sueño comparada con resultados de PSG nivel II en el domicilio5,7,8, mostrando menor eficiencia del sueño, menor porcentaje de etapa de sueño REM (del inglés; rapid eye movements) y aumento de microdespertares (arousals), no hallándose diferencias en cuanto a la estimación del índice de apneas e hipopneas por hora de sueño (IAH).
Sin embargo, es escaso el conocimiento actual sobre la eficiencia de sueño y calidad de la polisomnografía (PSG) realizada en la planta de internación de un hospital general, donde la prevalencia de AOS podría ser notoriamente mayor que en la población general7-8.
Algunas unidades de sueño con gran demanda, tienen listas de espera, por lo que ofrecen estudios de PSG con vigilancia técnica parcial o bien, sin vigilancia en tiempo real en pacientes hospitalizados, en etapa estable, o luego de la mejoría de la enfermedad que generó la admisión.
La clasificación de los niveles de PSG de la Academia Americana de Medicina del Sueño (AASM) discrimina el uso de dispositivos nivel I y nivel II (domiciliarios) en los cuales se requiere personal técnico para su correcta colocación y control del paciente, aunque no precisan una vigilancia del trazado en tiempo real.
Los criterios de calidad de los estudios de sueño realizados en el contexto específico de la planta de internación no han sido suficientemente estudiados. Por ello nos propusimos describir y comparar la calidad de los registros de PSG y la eficiencia de sueño (E ), en la PSG con vigilancia parcial realizada en pacientes ambulatorios que concurren a realizarse el estudio con dispositivos portátiles en el ámbito del laboratorio de sueño y PSG no vigilada con los mismos equipos y montajes en pacientes hospitalizados.
Materiales y métodos
Se trata de un estudio retrospectivo, descriptivo y comparativo, basado en una muestra consecutiva de registros de PSG nivel II, de una base de datos de recolección sistemática. El objetivo del estudio fue describir y comparar la eficiencia y calidad de sueño mediante PSG realizada en la planta de internación de pacientes hospitalizados y en el laboratorio de sueño.
El protocolo fue aprobado por el Comité de Ética y Revisión Institucional del Hospital Británico de Buenos Aires (protocolo #996) de acuerdo a los principios éticos de la declaración de Helsinki y sus modificaciones sucesivas.
Se incluyeron registros de PSG consecutivos de pacientes adultos entre julio de 2014 y enero del 2018 derivados por especialistas (clínicos, neurólogos, cardiólogos y neumonólogos) por sospecha clínica de AOS, debido a alguno de los síntomas cardinales: ronquido, somnolencia excesiva o apneas observadas por terceros.
Los pacientes ambulatorios concurrieron a la Unidad de Sueño a un estudio nocturno entre las 22.30 a las 06:30 horas. Se utilizó una habitación acondicionada fuera de la planta ordinaria de internación. Se instruyó a los pacientes ambulatorios a no modificar sus hábitos de alimentación o medicación antes de la prueba de sueño.
Los hospitalizados fueron seleccionados por sospecha de AOS para una PSG sin vigilancia técnica continua en la planta de internación con una agenda similar. Los investigadores del estudio no modificaron el régimen de medicación o tratamiento de los internados antes de la realización de la PSG.
Se registraron; edad, sexo, índice de masa corporal (IMC; en kg/m2) y motivo de internación.
Los menores de 18 años y aquellos que utilizaban oxigenoterapia, CPAP (siglas en inglés de presión positiva continúa en la vía aérea), o ventilación no invasiva, fueron excluidos del estudio.
El equipamiento, procedimiento de instalación y montajes fueron los mismos en ambos grupos. Utilizamos dispositivos portátiles ALICE PDX (Philips-Respironics, USA). El montaje incluyó al menos dos canales de electroencefalografía (EEG; C4, 02); dos canales de electrooculograma, tres canales de electromiografía (submentoniano, tibiales anteriores en ambas extremidades); electrocardiograma (un canal); flujo aéreo por termistancia y cánula nasal; esfuerzo respiratorio de tórax y abdomen usando sensores RIP (pletismografía por inductancia respiratoria); ronquido; posición corporal; oximetría de pulso y frecuencia cardíaca.
Todos los registros se analizaron manualmente mediante software específico (G3 Philips-Respironics, USA). Médicos expertos en Medicina del Sueño realizaron la puntuación de los registros usando criterios estandarizados cumpliendo las normativas AASM3-4.
Definimos tiempo total de sueño (TST) al resultante del total de tiempos calificados en cualquier etapa de sueño y eficiencia (E ) al cociente entre el tiempo total de sueño sobre el tiempo total en cama. La latencia se definió como el tiempo entre “luces apagadas” y la primera etapa de sueño por criterios neurofisiológicos.
Se estableció que un evento respiratorio era una apnea cuando el flujo aéreo nasal se redujo en más de un 90% y una hipopnea si se redujo entre un 30% y un 90%, asocia- da a una caída en la saturación de > 3% o asociado a un microdespertar cortical. En ambos casos durante un tiempo superior a 10 segundos. El índice de apneas e hipoapneas (IAH) se definió como el número de eventos respiratorios (apneas o hipopneas) (ev/h) por hora de sueño. y éste fue de valor patológico cuando alcanzó > 5 ev/h, estableciéndose las siguientes categorías de gravedad: leve (IAH entre 5.1 y 14.9 ev/h), moderado (IAH entre 15 y 29.9 ev/h) y grave (IAH ≥ 30 ev/h). Todos los datos se calcularon en función del TST luego de la calificación manual.
No se incluyeron registros de titulación de CPAP o bajo ventilación no invasiva. Los registros de PSG con montaje para epilepsia o realizados en pacientes con sospecha de trastornos del sueño no respiratorios no fueron incluidos en este análisis. (Fig. 1).
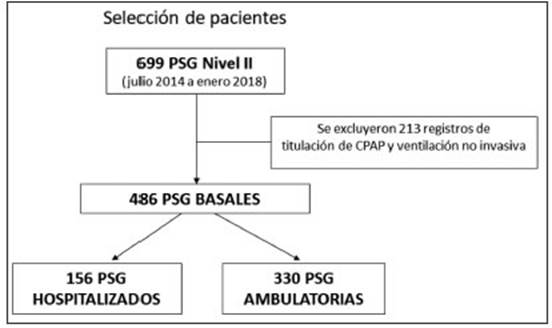
Fig. 1 Diagrama de flujo de selección de pacientes PSG: polisomnografía; CPAP: presión positiva continua en las vías aéreas
Las variables continuas fueron consignadas como media y desvío estándar (±) o mediana y rango intercuartilo. Para evaluar diferencias entre grupos se utilizaron test de Student (t-test) o Mann Whitney, dependiendo de su distribución. Las variables dicotómicas fueron consignadas como número y porcentaje. Las diferencias entre variables categóricas fueron evaluadas mediante Chi cuadrado. Todos los análisis fueron a dos colas y se consideró estadísticamente significativo un valor de p < 0.05.
Se incluyeron 486 registros en igual número de pacientes; 156 en la habitación de la planta de internación (PI) y 330 PSG en pacientes ambulatorios (PA) que concurrieron de manera programada al laboratorio de sueño.
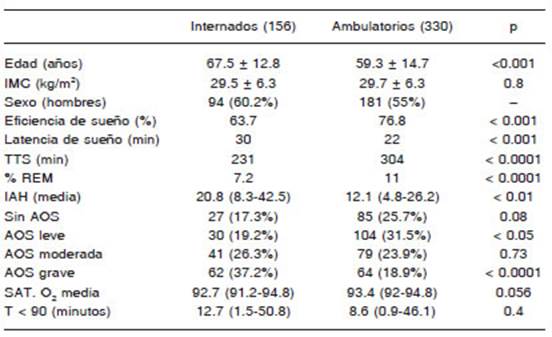
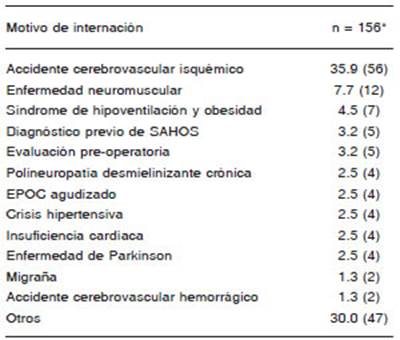
La comparación entre PI vs. PA mostró: 94 fueron hombres (60.2%) vs. 181 (55%); edad: 67.5 ± 12.8 vs. 59.3 ± 14.7, p < 0.001; índice de masa corporal: 29.5 ± 6.3 vs. 29.7 ± 6.3, p 0.8 (Tabla 1). En la Tabla 2 se muestran los motivos de internación más frecuentes.

Fig. 2 Tiempo total de sueño y eficiencia de sueño (en porcentaje) en pacientes ambulatorios (laboratorio de sueño) y durante la internación TTS: tiempo total de sueño
La latencia de sueño en minutos fue: 30 vs. 22, p < 0.001, tiempo total de sueño (TTS min); 231 vs. 304, p < 0.0001 (Fig. 3A) y el porcentaje de sueño REM fue de 7.1% vs. 11%, p < 0.0001, respectivamente (Fig. 3B).
Más aún, en ambos grupos una escasa proporción de horas), la E (%) fue menor en el grupo PI (mediana y pacientes tuvo una E normal (> 80% de TTS), siendo percentilo 25-75); 73.3 (60.8-82.1) vs. 78.5 (67.1-86.2), mayor en PA; 41.5 vs. 22.5 p < 0.001 (Fig. 4).
Finalmente, en aquellos con TTS > 180 min (tres horas), la Eff (%) fue menor en el grupo PI (mediana y percentilo 25-75); 73.3 (60.8-82.1) vs. 78.5 (67.1-86.2), p < 0.01.
Discusión
Nuestro estudio expone diferencias en la calidad de sueño en la PSG nivel II en el laboratorio de sueño en relación a la PSG realizada en la planta de hospitalización.
La PSG con vigilancia técnica en el laboratorio de sueño según normativas estandarizadas es la prueba de referencia para el diagnóstico de AOS. La PSG nivel II no se recomienda como una práctica estándar, según recomendaciones internacionales (AASM), aunque la información que provee es similar y su costo es inferior4-8.
La situación de cada institución puede determinar adaptación de la estrategia de diagnóstico en la AOS. Nuestro centro tiene 2-3 meses de demora para PSG y frecuentemente el especialista en medicina respiratoria es convocado para definir un caso de AOS probable en un paciente que cursa una internación por otra causa.
Bruyneel y col., en un estudio prospectivo, aleatorizado, ciego y cruzado, compararon PSG en el laboratorio de sueño vs. PSG en el domicilio sin vigilancia técnica, hallando una elevada eficiencia diagnóstica con alto grado de acuerdo en los indicadores respiratorios, por lo que proponen a la PSG domiciliaria como una alternativa rentable y eficaz en el proceso diagnóstico de la AOS7.
Sin embargo, factores extrínsecos (vinculados al ambiente) e intrínsecos (vinculados fundamentalmente a las afecciones de cada paciente y a sus alteraciones en el ritmo circadiano) interrelacionados entre sí, pueden ser responsables de la fragmentación del sueño de los hospitalizados e influir en los resultados de los estudios de PSG.
Además, características propias de cada paciente como hábitos de sueño y calidad del sueño previas a la internación, respuesta inflamatoria, dolor y ansiedad, así como la pérdida de los ciclos de luz-oscuridad y del ritmo circadiano, podrían afectar la calidad de sueño durante la hospitalización10. Adicionalmente, el ruido ambiental, las intervenciones de enfermería o la presencia de familiares o cuidadores podrían perturbar el sueño en condiciones de internación.
Las anomalías de la arquitectura del sueño son comunes, aunque poco reconocidas, en hospitalizados. Las que han sido más frecuentemente descriptas son la reducción del tiempo total de sueño, etapas REM y N3 (sueño delta o de onda lenta) y aumento en el porcentaje de la etapa N1 (sueño superficial no consolidado)11, consistentes con nuestros hallazgos.
En nuestra experiencia, los hospitalizados muestran un TTS reducido con latencias de sueño prolongadas. Este hallazgo alcanza diferencias notables cuando son comparados con pacientes ambulatorios que fueron sometidos a una PSG técnicamente similar dentro del mismo hospital (en el ámbito del laboratorio de sueño) y podría reflejar alteraciones circadianas dependientes de la situación clínica9.
Los laboratorios de sueño tienen que cumplir regulaciones respecto del nivel de luminosidad y ruido4,10 y aunque nosotros no hemos tomado mediciones en este sentido, hipotetizamos que el lugar y el momento en el que se realiza la evaluación polisomnográfica podrían influir en la calidad del estudio.
La AASM sugiere prudencia con las decisiones que se toman basados en estudios domiciliarios no vigilados, debido a que pueden subestimar los indicadores respiratorios y advierten que un resultado negativo no descarta la AOS3-4,12. En este contexto, la PSG evalúa múltiples variables del sueño y arrojaría mayor exactitud en el cálculo de los indicadores respiratorios si se compara con los métodos de diagnóstico simplificados, ya que permite interpretar los arousals corticales.
En nuestra experiencia, pese a que la PSG en PI obtuvo muestra de sueño escasa y con eficiencia reducida, permitió diagnosticar y clasificar a los pacientes con IAH elevado en grado patológico en el 80% de los casos, siendo el disturbio respiratorio grave en el 37% de manera concordante a otras series publicadas13-17.
La realización de una PSG, su análisis e interpretación y las conductas que se basan en sus hallazgos presentan dificultades en internados. Incluso la correlación con los hallazgos clínicos es difícil ya que los cuestionarios de sueño no han sido validados en este contexto, la somnolencia puede tener un origen multifactorial y la AOS es prevalente e incluso puede ser oligo o asintomática, como lo han sugerido Venkateshiah y Collop9.
En este estudio, la población analizada tuvo una significativa preponderancia de los diagnósticos relacionados a enfermedad cerebral isquémica, desmielinizante o degenerativa que podría influir sensiblemente en los indicadores de calidad de sueño. Este dato es de interés, ya que en ciertas poblaciones la identificación y el tratamiento precoz de la AOS podrían mejorar el pronóstico (accidente cerebrovascular agudo e insuficiencia cardíaca, por ejemplo)11. En este contexto, nuestros hallazgos adquieren jerarquía debido a la identificación de apneas obstructivas del sueño graves en el 37.2% en este grupo de pacientes. Pese a la eficiencia de sueño reducida, la PSG en hospitalizados permite identificar poblaciones de riesgo elevado que accederían al tratamiento precozmente.
El diseño retrospectivo de nuestro trabajo no nos permite evaluar la eficacia diagnóstica de la PSG ni hacer recomendaciones para su aplicación, sin embargo, los dispositivos usados en ambos grupos y la técnica de lectura e interpretación fueron similares en una población con elevada prevalencia de AOS.
Finalmente, no fueron incluidas la totalidad de las variables que pueden actuar como probables causas de interrupción del sueño durante la noche de adquisición del trazado en los hospitalizados. Nuestros hallazgos ponen en evidencia la prudencia necesaria al analizar indicadores obtenidos de estudios hospitalarios en pacientes que cursan enfermedades agudas, ya que no conocemos el momento óptimo para el registro de PSG.
La decisión de estudiar a cualquier hospitalizado debe fundamentarse en una evaluación completa y una correcta interpretación del cuadro clínico. Asimismo, se deben tomar precauciones para evitar interrupciones innecesarias del sueño. No parece criterioso realizar estudios en pacientes críticamente inestables o en situaciones en las que la información no sería útil a la hora de indicar la terapia específica para las AOS18.
Las condiciones clínicas pueden cambiar a medida que la enfermedad de base evoluciona o se resuelve, y podría ser necesario repetir un nuevo registro de PSG como procedimiento ambulatorio diferido (por ejemplo, después de un accidente cerebrovascular o resolución de la falla cardíaca) para redefinir el tratamiento definitivo. Las indicaciones y estándares de práctica específicamente para hospitalizados son aún una deuda pendiente.
Finalmente, en hospitalizados la calidad y la eficiencia de sueño fueron menores y una escasa proporción de pacientes duerme cuatro horas durante un registro basal de polisomnografía no vigilada.