PUNTOS CLAVE
• No hay estudios centroamericanos que evalúen la pre valencia de la infección por Tripanosoma cruzi en car diópatas, usando dos pruebas serológicas de principio diferente, tal como recomienda la OMS.
• Los datos de esta investigación sugieren que la principal estructura miocárdica involucrada es el nodo AV, con afectación por lo menos 8 veces más frecuente que la publicada en estudios sudamericanos.
• Teniendo en cuenta los costos en salud pública ocasio nados por las cardiopatías chagásicas, el alto costo de los marcapasos en países de bajos recursos, y la relación costo-efectividad de los programas de control del vector, estos deben financiarse y sostenerse en el tiempo.
La enfermedad de Chagas se distribuye casi exclusi vamente en los países en desarrollo de América Latina1,2. Como consecuencia de la creciente movilidad global, tam bién está siendo introducida en otras regiones3. En EE.UU. se han demostrado la presencia de insectos triatominos, que son los vectores, y la enfermedad fue documentada por primera vez en Texas en 1955 en inmigrantes procedentes de zonas endémicas, sin detección de casos autóctonos4. En un estudio realizado en 1985-1991 en Baltimore y Hous ton, 6 de 11 430 pacientes sometidos a cirugía cardíaca resultaron con serología positiva para Chagas. Los 6 eran extranjeros “hispanos”5. Se ha estimado que en Texas hay aproximadamente 250 000 personas infectadas6. Esta cifra está obviamente relacionada con la inmigración masiva desde México y América Central7. La infección chagásica también ha sido descrita en Europa8.
En 1909, el investigador brasileño Carlos Chagas describió una enfermedad causada por un protozoario, transmitida por insectos hematófagos pertenecientes a la subfamilia de triatominos tales como Rhodnius prolixus y Triatomina dimidiata 9. Siendo Centroamérica una región con economías básicamente agrícolas, clima cálido y con diciones precarias de vivienda, ofrece el hábitat propicio para la reproducción del vector. Recientes investigaciones han establecido que T. dimidiata es el principal vector en El Salvador10.
En 1913, un médico recién graduado, Juan Segovia, describió el parásito por primera vez en El Salvador en un extendido de sangre de un paciente febril con diagnóstico presuntivo de malaria. La identificación de Trypanosoma cruzi de este caso fue hecha en colaboración con Carlos Chagas11. En 1935, Cecilio Romaña describió la infla mación unilateral periorbital indolora propia de la etapa aguda de la enfermedad, signo que lleva su nombre12. Rosenbaum y Álvarez, en su estudio clásico de 1955, describieron los hallazgos electrocardiográficos más frecuentes en la miocardiopatía chagásica13. Posterior mente, Rosenbaum, en una amplia revisión, presentó los conceptos clínicos, fisiopatológicos y epidemiológicos de la infección14. En 1956, un grupo de cardiólogos y parasitó logos salvadoreños publicó en una revista local la primera serie de 14 casos con detección del parásito en sangre periférica15,16. En 1975, Rafael Cedillos, parasitólogo e investigador de la Facultad local, en colaboración con la Estación Centroamericana de los CDC de EE.UU. situada en San Salvador, observó una prevalencia de infección inesperadamente alta, a juzgar por los resultados de las pruebas serológicas de personas asintomáticas residen tes en zonas rurales, con valores que oscilaban entre 17 y 46%17. Se hizo evidente que la transmisión puede ocurrir también por mecanismos no vectoriales como transfusiones, trasplantes de órganos, verticalmente de madre a hijo y al ingerir alimentos contaminados18,19. En consecuencia, se desarrollaron estrategias para prevenir estas formas de transmisión. Desde 1996, es obligatorio investigar la infección en donantes de sangre, órganos y tejidos en la mayoría de los países de América Latina, incluido El Salvador20-22.
Con el propósito de conocer la frecuencia de infección chagásica en pacientes con enfermedades miocárdicas de El Salvador, se realizó una investigación observacional retrospectiva en nuestro hospital, que es un centro de referencia de nivel nacional.
Materiales y métodos
En Centroamérica, es usual solicitar pruebas de Chagas a pa cientes hospitalizados según su condición social, lugar de re sidencia, o cuando hay historia de picadura del insecto vector, que es conocido por la mayoría de las personas. Sin embargo, siendo el istmo una zona 100% tropical y subdesarrollada, las condiciones habitacionales, clase social y otros datos demo gráficos, normalmente terminan siendo irrelevantes, por lo que la muestra se considera homogénea para infección chagásica en prácticamente todos los factores de riesgo.
El 70% de la población de El Salvador es atendido por la red del Ministerio de Salud, financiada totalmente por el gobierno. Esta red se encarga del segmento económicamen te más desfavorecido: campesinos, obreros no calificados, artesanos, micro comerciantes e individuos desempleados. El Hospital Rosales forma parte de esta red del Ministerio de Salud y provee atención en las especialidades de Medicina y Cirugía. Solo atiende adultos mayores de 18 años (y oca sionalmente pacientes entre 12-18), provenientes de áreas rurales y urbanas. La muestra aquí estudiada proviene de esta población.
En el presente estudio se revisaron semanalmente los registros de la sección de Chagas en el Laboratorio Clínico, desde el primer día hábil de enero de 2013 hasta el último día hábil de diciembre de 2015 (36 meses consecutivos) a fin de identificar pacientes con serología positiva, que eventualmente resultaron hospitalizados en la Unidad Cardiológica.
En ese periodo se habían efectuado 1472 pruebas, en los pacientes atendidos en todas las especialidades que ofrece la institución. No se incluyeron donantes, que son anotados en la base de datos de la Red Nacional de Bancos de Sangre. Los individuos con cardiopatías estudiados fueron reclutados estando hospitalizados.
Debido a la naturaleza de la especialidad, además del exa men físico y pruebas básicas de laboratorio, a todo paciente ingresado a la Unidad Cardiológica se le practica al menos, un electrocardiograma (ECG) y un ecocardiograma (ECO) con Doppler, para optimizar la sensibilidad diagnóstica13,23.
Las enfermedades fueron definidas de la siguiente mane ra: El diagnóstico de cardiomiopatía chagásica se estableció valiéndose de ECO y ECG con o sin Holter más la prueba serológica. Ocasionalmente, cuando se consideró pertinente excluir otras enfermedades, se ordenó una resonancia magné tica (RM). No realizamos cateterismo, ni biopsia endocárdica.
La cardiopatía isquémica se diagnosticó con la presencia de criterios de infarto agudo o no agudo (clínicos, laboratorio y electrocardiográficos), al momento del estudio. Tampoco se realizó cateterismo debido a restricciones financieras.
El diagnóstico de insuficiencia cardíaca se determinó por los resultados del ECO para conocer la fracción de eyección y por estar asociada a causas diferentes de isquemia.
En la institución asignamos diagnóstico de arritmia a los casos cuya principal causa cardiológica de ingreso es la pre sencia electrocardiográfica de cualquier ritmo que no sea ritmo sinusal normal con normal conducción AV. Generalmente son personas con fibrilación auricular reciente o crónica presentan do alguna complicación que requiera manejo intrahospitalario.
El diagnóstico de bloqueo AV nodal se efectuó según definiciones estándar y al igual que la decisión de implantar marcapasos permanentes, fue basada en guías vigentes al momento del estudio24.
El proceso de diagnóstico serológico siguió las estrate gias estándar de la OMS25, ejecutando una prueba de ELISA recombinante (Wiener Lab, Argentina) que, cuando era po sitiva, se confirmaba con hemoaglutinación indirecta (HAI, Wiener Lab, Argentina). Dos pruebas positivas aseguraban el diagnóstico.
Por tratarse de un estudio observacional retrospectivo que consistió en revisión de registros de laboratorio y expedientes, no se comprometió la privacidad de las personas.
Resultados
De las 1472 pruebas realizadas a pacientes individua les, sin incluir donantes de sangre, durante el período de estudio, 557 (37.8%) resultaron seropositivas y 915 seronegativas (62.2%). De los 557 casos seropositivos, 97 (17.4%) presentaban diversas cardiopatías. Las restantes 460 (82.6%) pruebas serológicas positivas correspondieron a pacientes no cardiópatas atendidos por otras especialidades.
De los 915 pacientes que resultaron seronegativos para Chagas, 191 (20.9%) presentaron cardiopatías diver sas. De este modo, el total de casos asistidos por cardio patías ascendió a 288 (191+97) y la infección chagásica estaba presente en el 33.7% (97/288) de ellos (Fig. 1).
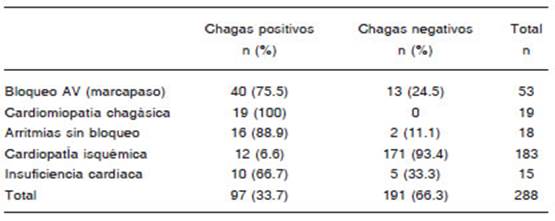
Las frecuencias de distintas entidades cardiológicas en pacientes seropositivos y seronegativos se describen en la Tabla 1. Entre los 97 con cardiopatía chagásica, 40 (41.2%) cumplieron criterios para colocación de marca paso permanente, mientras que solo 13 de 191 (6.8%) enfermos con cardiopatías no chagásicas cumplieron esos criterios (Tabla 2).
Discusión
Un Comité de Expertos de la OMS estimó en 2006 las tasas de infección en los países de la región de las Amé ricas26. Los porcentajes variaron entre 6.8% en Bolivia y 0.5% en Costa Rica, con una prevalencia media de 1.5% para toda la región y 2.0% para América Central. Aunque El Salvador presentó la tasa más alta (3.4%) del istmo, este valor constituye un notable descenso en la prevalencia con respecto a las observadas por Cedillos en 197517. Para 2010 se estimaba que aún existían 806 600 personas infectadas en un istmo de 39.6 millones de habitantes11.
En 2011, investigadores internacionales y locales ana lizaron una muestra de 885 187 pruebas en 31 bancos de sangre en El Salvador, detectando una reducción en la prevalencia a 1.7%27. Cabe destacar que descensos similares también han ocurrido en el resto de América Latina1,21,28,29. A pesar de esto, se ha documentado la exportación del protozoario fuera de la región7,8,30,31.
En virtud de la marcada presencia de infección por T. cruzi en Centroamérica, no sorprende que la enferme dad de Chagas haya resultado responsable de un tercio (97/288) de las cardiopatías de nuestro estudio (Tabla 1). En cambio, entre los diagnósticos asociados, es llamativo que 4 de cada 10 pacientes con cardiopatía chagásica tuvieran criterios para recibir marcapasos permanentes por bloqueo auriculoventricular (AV) (Tablas 1 y 2). Esta proporción es mayor que la informada en otras investiga ciones y solo comparable al de una serie muy antigua de casos documentada en California, EE.UU., donde 9 de 25 (36%) enfermos requirieron implantación de marcapasos por bloqueo AV32. En contraste, un estudio realizado en Bolivia encontró que solo 8 de 327 (2.4%) individuos positivos tuvo bloqueo AV con criterios suficientes para implantación del dispositivo33. De modo similar, en una cohorte brasileña de 424 pacientes con cardiopatía cha gásica, se encontró 9% con bloqueo AV34. También en una gran muestra de 7590 ECGs de pacientes en Minas Gerais, con enfermedad de Chagas auto-reportada, hubo 406 con bloqueo AV para una prevalencia de 5.3%. Cabe señalar que, en esa casuística detectaron 36 pacientes con bloqueo de segundo o tercer grado, sugiriendo que la presencia de bloqueo avanzado se correlaciona fuer temente con la enfermedad (OR 13.3 IC 11.5-15.4)35.
Aun tomando en cuenta que el número de infectados es relativamente pequeño, llama la atención que la fre cuencia de bloqueo nodal AV asociado a infección por T. cruzi, con indicación de marcapasos (de alto costo), resultó entre 8 y 16 veces mayor que la documentada en países de América del Sur. Esto hallazgos indican y refuerzan la recomendación de financiar y sostener en el tiempo estrategias de salud ambiental preventiva, por razones de salud pública y costo efectividad36.