El rabdomiosarcoma se define como una neoplasia maligna con diferenciación fenotípica a músculo estriado esquelético. Originalmente Weber y Virchow1 describie ron la entidad en 1854, sin embargo, recién en 1946 fue formalmente definido y caracterizado por Stout en una revisión de 121 casos2.
El rabdomiosarcoma es el sarcoma de partes blandas más frecuente en niños y localiza generalmente en cabeza y cuello y extremidades. El pronóstico depende del control de la enfermedad primaria, su diseminación y del grupo molecular al cual pertenezcan3. En adultos la frecuencia es mucho menor y generalmente asienta en extremidades.
En cuanto a la localización pulmonar primaria cabe destacar que es extremadamente infrecuente y el mayor número de publicaciones mencionan su existencia en pacientes en la primera década de la vida, siendo el origen pulmonar excepcional en adultos.
Desde el punto de vista histológico se reconocen 4 subtipos: alveolar, embrionario, pleomórfico y esclero sante. El alveolar se caracteriza por una proliferación de células redondas de aspecto primitivo, miogenina, desmi na y MYOD1 positivas. El embrionario está representado por células redondas y fusiformes, con rabdomioblastos diferenciados, desmina y miogenina/MYOD1 positivas. El pleomórfico muestra células con abundante citoplasma eosinófilo, desmina y miogenina positivas. Finalmente, el esclerosante se halla constituido por elementos fusiformes con un fondo esclerosante que son desmina, miogenina y MYOD1 positivas4-6.
Datos obtenidos del Surveillance, Epidemiology and End Results(SEER) Program, comparando hallazgos clínicos y seguimiento en niños y adultos revelaron que estos últimos tenían un pronóstico más adverso (26.6% con 5 años de supervivencia vs. 60.5% en niños)3.
Caso clínico
Se trata de un varón de 48 años, sin antecedentes de je rarquía, derivado de un centro de baja complejidad para estudio y tratamiento de tumor pulmonar. La radiografía de tórax mostró una lesión única radiopaca en campo pulmonar derecho, en relación al hilio. La tomografía computarizada evidenció compromiso de los segmentos posteriores del lóbulo inferior derecho. El estudio clínico e imagenológico descartó el compromiso de otros órganos por lo que se optó por realizar una lobectomía inferior derecha con vaciamiento ganglionar. El diagnóstico intraoperatorio de la pieza quirúrgica fue de neoplasia maligna poco diferenciada.
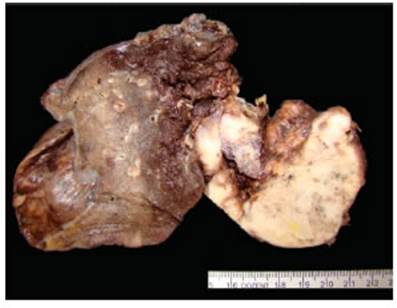
La pieza quirúrgica mostró una lesión tumoral sólida de bordes irregulares, consistencia duro-firme y tonalidad blan quecina, de 7 cm de diámetro mayor, que comprometía el hilio lobar y pleura visceral (Fig. 1). Se recepcionaron además cin co ganglios linfáticos hiliares sin alteraciones macroscópicas.
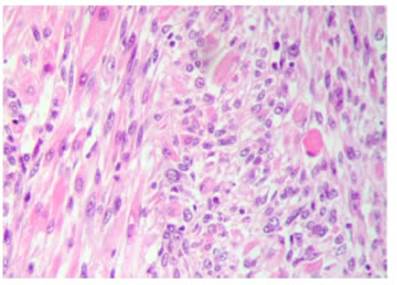
El estudio microscópico reveló una lesión neoplásica ma ligna, constituida por células mesenquimáticas primitivas que en sectores adquirían abundante citoplasma acidófilo, núcleos excéntricos y ocasionales estriaciones citoplasmáticas. El conteo mitótico fue de 10-15/10 campos de gran aumento, y se observaron focos de necrosis. Los ganglios linfáticos no presentaron compromiso tumoral (Fig. 2).
Entre los diagnósticos diferenciales planteados cabe men cionar: carcinoma de células grandes con hallazgos rabdoides, carcinosarcoma y fundamentalmentalmente sarcomas metas tásicos originados en partes blandas.
Con la finalidad de definir la estirpe se realizaron estudios de inmunohistoquímica cuyos resultados fueron: desmina, actina muscular específica, miogenina, vimentina y S100 positivos, citoqueratinas, CD34, actina muscular lisa y TTF 1negativos. La imagen histológica sumada al perfil inmunohis toquímico permitió arribar al diagnóstico de rabdomiosarcoma embrionario. Ante la necesidad de definir el origen primario o metastásico de la lesión pulmonar se estudió al paciente mediante diversas técnicas de imágenes. Teniendo en cuenta que las mismas no revelaron lesiones tumorales en otros órganos se consideró a la neoplasia como un rabdomio sarcoma primitivo pulmonar estadio (AJCC) pT2b pn0 pMx; estadificación del IRSG: Estadio Clínico 3+ Grupo Clínico Ib: Grupo Clínico de Bajo Riesgo.
El paciente inició tratamiento quimioterápico (carboplatino + etopósido). Tres meses luego de la cirugía se identificó una masa tumoral en lóbulo superior derecho. Se realizó neumonectomía derecha. La pieza quirúrgica presentó un nódulo de 5 cm de diámetro en relación al hilio, con hallaz gos histomorfológicos e inmunohistoquímicos similares a los previamente descriptos.
El paciente continuó con los ciclos quimioterápicos, y en un control evolutivo a los 11 meses de la cirugía original se detectó una lesión tumoral en la glándula suprarrenal derecha. El estudio citohistológico demostró la presencia de elementos atípicos con un perfil inmunohistoquímico similar al obtenido en el tumor pulmonar por lo que interpretó la lesión como secundarismo adrenal del rabdomiosarcoma. El paciente prosiguió con quimioterapia, durante la cual desarrolló in fecciones intercurrentes, y falleció 20 meses después de la primera cirugía.
Responsabilidades éticas: no se revelan datos personales. Se cumplimentan los requerimientos del Comité de Ética.
Consentimiento informado: los pacientes que ingresan al Hospital firman un consentimiento para que los informes de patología y datos clínicos puedan ser utilizados para fines académicos sin que consten los datos de filiación.
Discusión
El rabdomiosarcoma primitivo de pulmón es una neopla sia extremadamente infrecuente que requiere de un ex haustivo estudio anatomopatológico ya que es primordial descartar otros tumores poco diferenciados que podrían presentar una morfología similar. La inmunohistoquímica es relevante ya que juega un papel fundamental para definir estirpe7,8.
El asiento de rabdomiosarcomas en sitios no habitua les es objeto de estudio y se proponen diferentes teorías. Existen varias hipótesis que intentan dar una interpreta ción adecuada en cuanto al origen de estas neoplasias las cuales incluyen: a- asiento en células mesenquimáticas primitivas presentes en la pared bronquial e intersticio pulmonar que han sufrido diferenciación mioblástica, b- transformación metaplásica de células pluripotenciales no mioblásticas, c- presencia de músculo estriado abe rrante, d- restos embrionarios. Existen autores a favor de una u otra teoría teniendo en cuenta su experiencia y datos de investigación, sin embargo, no existe hasta el momento una que haya sido totalmente aceptada y se postula que la histogénesis del rabdomiosarcoma pulmonar puede ser heterogénea y depende de diversas condiciones9.
En los casos publicados de pacientes adultos la neo plasia asentó en pulmones sin enfermedad previa, no se observó componente teratomatoso, enfermedades congénitas ni presencia de músculo estriado. Se halló en la bibliografía un únicocaso de rabdomiosarcoma primitivo pulmonar en paciente adulto asociado a neu rofibromatosis10.
En la gran mayoría de los casos reportados en pa cientes pediátricos se describe la asociación con diversas patologías pulmonares pre-existentes tales como: enfer medad adenomatoidea, quistes pulmonares congénitos y quistes broncogénicos11.
En base a esto existen autores que intentan clasificar la neoplasia en dos grupos diferentes: aquellos que asientan en pulmones sin patología previa, (habitualmente pacientes adultos) y los que se originan en pulmones previamente enfermos9.
Si bien no se tuvo acceso al estudio por biología molecular, cabe mencionar que en algunos rabdomio sarcomas embrionarios se ha detectado pérdida de la heterocigocidad en el locus 11p15, sitio de los genes del factor de crecimiento IGF-2 y H19, gen de un ARN no codificante de cadena larga que interviene en la limitación de la proliferación celular.
En relación a la estadificación clínica de los pacientes, esta se realiza a partir de los esquemas propuestos por Intergroup Rhabdomyosarcoma Study Group y Children’s Oncology Group Stratification for Rhabdomyosarcoma, grupos cooperativos de estudios clínicos que recopilan en conjunto más de 30 años de investigación multicéntrica12. La clasificación considera diferentes parámetros como tipo histológico, sitio y tamaño tumoral, extensión local y metástasis ganglionares y a distancia. Esta estadificación permite encuadrar a los pacientes en alguno de los tres grupos de riesgo clínico (bajo, intermedio o alto) para adaptar los tratamientos en concordancia.
El abordaje terapéutico es multimodal y consiste en resección quirúrgica amplia y eventual radioterapia de la neoplasia primaria, así como quimioterapia sistémica. En los últimos años se ha evidenciado mayor supervivencia en pacientes pediátricos, sin embargo, en adultos el pronóstico en general es ominoso, con tasas de supervi vencia a los 5 años que no superan el 40%.