Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. vol.84 no.4 Ciudad Autónoma de Buenos Aires ago. 2016
CARTAS CIENTÍFICAS
Incidencia y factores que influyen en la isquemia medular durante el tratamiento endovascular de la aorta torácica
La colocación de endoprótesis en la aorta torácica es un procedimiento que se realiza en un número cada vez mayor de pacientes. Trabajos recientes evidencian que la cobertura extensa de la aorta torácica está relacionada con la incidencia de complicaciones neurológicas. (1) Si bien reportes en la literatura internacional reflejan generalmente una incidencia menor de isquemia medular (IM) durante la colocación de endoprótesis que durante la cirugía convencional, la IM persiste como una de las complicaciones más devastadoras y temidas. (2, 3) Muchos factores se han identificado como favorecedores de aparición de IM; caben mencionar el antecedente de tratamiento previo de la aorta abdominal, la hipotensión arterial durante el implante, la cobertura de la arteria subclavia izquierda y la extensión de aorta cubierta. (4) El objetivo de esta presentación fue analizar la incidencia de IM e identificar los factores de riesgo asociados con su aparición en aquellos pacientes en los que se cubrió completamente la aorta torácica.
Entre abril de 1999 y diciembre de 2014 se trataron 176 pacientes por vía endovascular en la aorta torácica; a 62 pacientes (48 hombres y 14 mujeres) con una edad media de 59,95 años se les colocó una endoprótesis en la aorta torácica desde el arco aórtico hasta el tronco celíaco, debido a aneurisma verdadero (n = 13), disección aórtica (n = 42), hematoma intramural (n = 4), seudoaneurisma postraumático (n = 2) y úlcera aórtica (n = 1). En la Tabla 1 se muestran las características clínicas y demográficas de los pacientes.
Previo a la intervención, a todos los pacientes se les realizó una angiotomografía. La arteria subclavia izquierda fue ocluida intencionalmente sin revascularización en 22 casos (35,48%) debido a que el cuello aórtico proximal era de menos de 15 mm de longitud. (5) En 3 pacientes se cubrió intencionalmente el tronco celíaco debido a un cuello aórtico distal corto. En 5 pacientes se realizó protección medular mediante drenaje de líquido cefalorraquídeo. Todos estos pacientes tenían antecedentes de cirugía abdominal previa.
Todos los procedimientos se realizaron bajo anestesia general y monitorización invasiva de la presión arterial, manteniendo una presión arterial media superior a 90 mm Hg.
Se definió éxito técnico del implante a la liberación correcta de las endoprótesis, sin conversión a cirugía convencional y sin evidencias de endoleaks inmediatos tipos I y III. (6) Las variables continuas se presentan como mediana e intervalo intercuartil (25-75), mientras que las categóricas se expresan como porcentajes junto con su valor absoluto. La diferencia en la sobrevida a 1, 3 y 6 años se evaluó por el método de Kaplan-Meier. El análisis estadístico se realizó con el programa STA-TA 13.
El éxito técnico del implante fue del 96,7% registrándose dos endoleaks tipo I (3,23%) al finalizar el procedimiento y mortalidad perioperatoria en 3 pacientes (4,84%). No hubo conversión a cirugía convencional y las causas de muerte fueron rotura aórtica en un paciente y falla multiorgánica en los otros dos. El largo medio de cobertura aórtica fue de 288 mm (rango 200 a 360 mm). Ninguno de los pacientes en los que se cubrió intencionalmente la arteria subclavia izquierda (35,48%) y el tronco celíaco (4,84%) desarrolló isquemia de miembro superior izquierdo o mesentérica, respectivamente.
La incidencia de IM se observó en 3 pacientes (4,83%), inmediata en uno y alejada en dos. La presentación de la IM en un paciente fue con paraparesia a 24 horas del tratamiento estando en unidad coronaria. El segundo paciente desarrolló un cuadro de eyaculación retrógrada y parestesias de ambos miembros inferiores a los 3 años del procedimiento y el tercero desarrolló paraplejía permanente a los 4 años de la intervención. La sobrevida a 1, 3 y 6 años fue del 76%, 69,91% y 64,32%, respectivamente (Figura 1).
La IM es una complicación grave durante la colocación de endoprótesis en patología de la aorta torácica, con una frecuencia que en la literatura internacional se reporta en rangos del 0% al 12%. (3-5) En nuestro trabajo, la incidencia de IM fue del 4,83% (3 pacientes). El paciente que presentó paraparesia a las 24 horas
Tabla 1. Características de los pacientes
| Edad, años | 59,95 (22-87) |
| Hipertensión arterial, % (n) | 98,44 (61) |
| Tabaquismo activo, % (n) | 35,94 (21) |
| Diabetes, % (n) | 20,31 (13) |
| Obesidad, % (n) | 43,55 (27) |
| Enfermedad coronaria, % (n) | 23,44 (15) |
| Enfermedad pulmonar obstructiva crónica, | % (n) 43,75 (26) |
| Insuficiencia renal crónica, % (n) | 16,13 (10) |
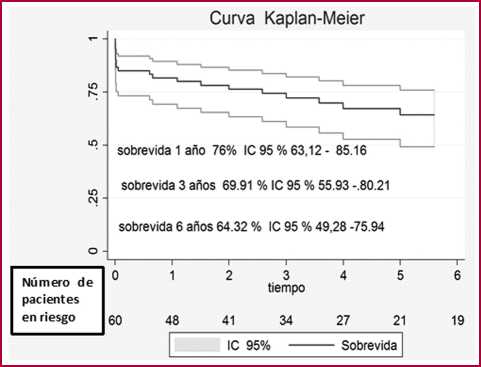
Fig. 1. Curvas de sobrevida de Kaplan-Meier a 1, 3 y 6 años.
del tratamiento estando en unidad coronaria había sido tratado por un aneurisma torácico y años antes había recibido un bypass aorto-bifemoral. Se le realizó un drenaje de líquido cefalorraquídeo mediante un catéter raquídeo colocado durante la intervención hasta alcanzar los 10 mm Hg. El paciente fue dado de alta a las 72 horas, asintomático.
El segundo paciente tratado por una disección crónica y que había sido intervenido precedentemente por vía endovascular de la aorta abdominal desarrolló un cuadro súbito de parestesias de ambos miembros inferiores y eyaculación retrógrada a los 3 años de la intervención, que se corrigió con estabilización de la presión arterial. El tercer paciente, tratado también por una disección aórtica crónica, desarrolló paraplejía a los 4 años del procedimiento, debido probablemente a embolia ateromatosa en una aorta con múltiples placas fibrolipídicas calcificadas, permaneciendo parapléjico durante el seguimiento.
La aparición de IM luego de la colocación de endo-prótesis en la aorta torácica ocurre más frecuentemente cuando las arterias que suplen la médula espinal son sacrificadas (arteria de Adamkiewicz, intercostales y lumbares), como también luego de un período de hipotensión grave o de embolias provenientes de lesiones ateromatosas de la aorta. (5) Nuestros resultados demuestran que, a pesar de cubrir la totalidad de la aorta torácica y en consecuencia ocluyendo la totalidad de las arterias intercostales, no existe una correlación lineal de esto con la aparición de IM. Esto puede ser explicado por el modelo de vascularización de la médula espinal propuesto por Griepp, (6) el cual demuestra que la irrigación de la médula espinal es dependiente de múltiples arterias colaterales que suplen a la arteria espinal anterior, en lugar de una única arteria dominante de Adamkiewcz que anteriormente se consideraba esencial para mantener la perfusión de la médula espinal. (6) También hay que mencionar que la IM es un fenómeno que no solo puede presentarse durante el tratamiento endovascular o inmediatamente luego de él, sino que también puede aparecer en el período alejado, como ocurrió en dos de nuestros pacientes. (6) Las únicas dos medidas que aplicamos sistemáticamente para prevenir la IM fueron mantener una presión arterial media elevada (> 90 mm Hg) y estable durante la intervención y evitar la pérdida hemática.
En nuestra serie realizamos protección medular en aquellos casos en los cuales se cubrió toda la aorta torácica y la aorta abdominal había sido intervenida previamente. Si bien existe riesgo de hematoma compresivo de la médula espinal por la punción del canal raquídeo, consideramos que esta técnica debe utilizarse como medida profiláctica solamente en este escenario. Podemos concluir que el tratamiento endovascular de la aorta torácica descendente mediante colocación de endoprótesis no debe considerarse un factor causante de IM. De nuestros 62 pacientes intervenidos por vía endovascular con cobertura total de la aorta, solamente 3 pacientes (4,48%) presentaron IM, dos temporarias y una permanente. En relación con el establecimiento de un factor predictivo, consideramos que el único es la reparación previa de la aorta en el sector abdominal. En este escenario, todos los pacientes deberían ser intervenidos con protección medular, manteniendo una presión arterial media estable > 90 mm Hg durante toda la intervención y en las primeras 48 horas posteriores al procedimiento.
Hernán Bertoni1, Germán Gírela2, Juan I. Pardo3,Eduardo Magariños1
1 Servicio de Cardioangiología Intervencionista, Instituto Fleni, Buenos Aires 2 Servicio de Cirugía Cardíaca, Instituto Cardiovascular
del Sur, Río Negro 3 Servicio de Cirugía Vascular, Sanatorio La Torre,
Buenos Aires
BIBLIOGRAFÍA
1. Gravereaux EC, Faries PL, Burks JA, Latessa V Spielvogel D, Hollier LH, et al. Risk of spinal cord ischemia after endograft repair of thoracic aortic aneurysms. J Vasc Surg 2001;34:997-1003. http:// doi.org/fTdzcb
2. Bavaria JE, Appoo JJ, Makaroun MS, Verter J, Yu ZF, Mitchell RS. Endovascular stent grafting versus open surgical repair of descend-ing thoracic aortic aneurysms in low-risk patients: a multicenter comparative trial. J Thorac Cardiovasc Surg 2007;133:369-77. http:// doi.org/dg2zx5
3. Greenberg R, Resh T, Nyman U, Lindh M, Brunkwall J, Brunkwall P et al. Endovascular repair of descending thoracic aortic aneurysms: An early experience with intermediate-term follow-up. J Vasc Surg 2000;31:147-e156. http://doi.org/c785hh
4. Carroccio A, Marin ML, Ellozy S, Hollier LH. Pathophysiology of paraplegia following endovascular thoracic aortic aneurysm repair. J Card Surg 2001;11:359-e366.
5. Bertoni H, Azzari F, Girela G, Salvo G, De la Vega A, Romero G y cols. Oclusión intencional de la arteria subclavia izquierda durante el tratamiento endovascular de la aorta torácica descendente. Rev Argent Cardiol 2011;79:21-6.
6. White RA, Donayre CE, Walot I, Lippmann M, Woody J, Lee J, et al. Endovascular exclusion of descending thoracic aortic aneurysms and chronic dissections: Initial clinical results with the AneuRx device. J Vasc Surg 2001;33:927-34. http://doi.org/dt4fcf
Rev Argent Cardiol 2016;84:372-373. http://dx.doi.org/10.7775/rac.es.v84. i4.7715
Hallazgo angiográfico inesperado: remanente de guía de angioplastia
La fractura de la guía de angioplastia es una complicación infrecuente durante la revascularización percu-tánea. Hasta 2015 existían solo 67 casos publicados en todo el mundo, (1) con descripción de múltiples estrategias para abordar este problema. Sin embargo, debe considerarse que muchos de estos episodios podrían no ser comunicados ni publicados. La gran mayoría de los autores optan por el retiro del material, ya sea de forma percutánea o quirúrgica, mientras que solo una minoría decide un manejo conservador. Presentamos un caso en el que 4 años atrás se había optado por una estrategia conservadora a pesar de tratarse de un fragmento de considerable tamaño.
Se trata de una mujer de 65 años, hipertensa, diabética, dislipidémica, obesa mórbida y con antecedentes familiares de cardiopatía isquémica precoz. Se ha trasladado recientemente a nuestra área sanitaria y no disponemos de informes previos, pero refiere que hace 4 años se le implantaron seis stents por un infarto. Llama la atención que está con tratamiento antiagregante de forma crónica con prasugrel en monoterapia junto con el resto de tratamiento para cardiopatía isquémica crónica.
Acude a urgencias por clínica que sugiere infección respiratoria de varios días de evolución; en ese contexto presenta un episodio de dolor torácico de características anginosas, acompañado de discreto descenso del segmento ST inferolateral, que cede rápidamente con nitratos intravenosos. Se solicita evaluación a la guardia de Cardiología y en la anamnesis dirigida la paciente refiere molestias similares con grandes esfuerzos que ocasionalmente han requerido utilización de nitroglicerina sublingual para remitir, pero niega episodios previos en reposo desde la revascularización realizada 4 años atrás.
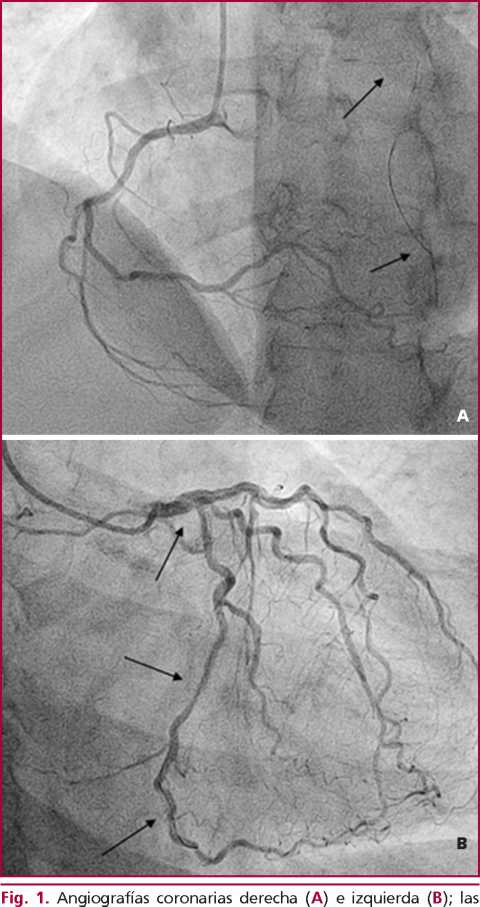
En la analítica posterior se objetiva ligera elevación de marcadores de daño miocárdico y, aunque todo orienta hacia un infarto sin elevación del segmento ST tipo II, por aumento de demandas, dados los antecedentes que refiere la paciente se decide su ingreso en Cardiología. El ecocardiograma muestra un ventrículo izquierdo no dilatado, con función sistólica conservada y ausencia de valvulopatías significativas. El cuadro infeccioso aparenta ser una viriasis de vías respiratorias altas no complicada, sin infiltrados en la radiografía de tórax ni más alteraciones relevantes en la analítica. Se realiza una coronariografía en la que se objetiva la presencia de un remanente de guía de angioplastia desde el tronco común de la coronaria izquierda (TCI) hasta la arteria circunfleja distal, que aparentemente está enjaulada por el stent del TCI y no compromete el flujo (Figura 1 A y B). Todos los stents están permeables, presenta irregularidades no significativas en el resto de los vasos epicárdicos, con alguna estenosis no revascularizable en vasos de escaso calibre. Se plantea la realización de una tomografía de coherencia óptica intracoronaria, pero finalmente se decide no profundizar en estudios con imagen intravascular por el innecesario riesgo que conllevarían. Superado el cuadro infeccioso, la paciente no vuelve a presentar clínica de angina.
Ante la escasa evidencia existente en la literatura sobre el manejo de estos casos, y en vista de la estabilidad de la paciente durante los 4 años que habían transcurrido desde la fractura de la guía, optamos por mantener empíricamente la antiagregación con prasugrel de forma indefinida, tal y como lo venía realizando. Nos planteamos serias dudas sobre flechas muestran el remanente de guía.
si añadir o no anticoagulación sistémica al tratamiento, ya que la mayoría de los autores apoyan su utilización. (2) De nuevo, al contar con la ventaja de ya haber comprobado la buena evolución sin tratamiento anticoagulante, consideramos que añadiría un riesgo hemorrágico excesivo sin margen para aportar grandes beneficios.
La rotura de la guía de angioplastia es un evento muy poco habitual durante el intervencionismo coronario percutáneo, con una incidencia estimada del 0,1-0,2% de las angioplastias. (3) El exceso de rotación axial, las fuerzas de tracción, sobre todo si la punta ha quedado atrapada, o una marcada flexión son los mecanismos más conocidos que pueden generar la rotura de la guía. (4) La unión entre los 3 cm más flexibles de la punta y el resto de la guía es el lugar donde generalmente se produce la fractura. (5) Se ha encontrado una asociación de las roturas de las guías
con el uso de determinado instrumental intracoronario, como tromboaspiradores o aterótomos rotacionales. (6)
El manejo de estas situaciones es extremadamente complejo y existe poca evidencia en la que apoyarse. Los remanentes de guías abandonados dentro del árbol coronario pueden generar complicaciones graves, como perforación del vaso, fenómenos embólicos, trombosis in situ y la oclusión del vaso. (2) Por este motivo se recomienda intentar el retiro del material, en lo posible de manera percutánea, reservando la cirugía para cuando la estrategia intervencionista falla.
Se encuentran descriptos múltiples mecanismos para intentar el retiro de la guía de forma percutánea. Si la parte más proximal del fragmento queda en la aorta se suelen utilizar lazos con resultados bastante satisfactorios. Cuando todo el remanente se encuentra dentro de la arteria coronaria, existen dos estrategias principales; una de ellas consiste en hacer cuña con un balón o un microcatéter e intentar arrastrar el fragmento, mientras que la otra técnica se basa en envolver el remanente de la guía fracturada girando a su alrededor otras dos guías para poder retirarlo. (1) Cuando estas estrategias fallan, algunos autores optan por implantar stents cubriendo el fragmento, dejándolo atrapado entre la malla del stent y el endo-telio, buscando así minimizar los riesgos antes mencionados. Si durante el procedimiento de recuperación de la guía se produce isquemia, ya sea acompañada de inestabilidad hemodinámica o no, se recomienda detener la estrategia intervencionista y optar por cirugía. La cirugía se convierte en obligatoria si se evidencia extravasación de contraste que haga suponer una laceración del vaso. (1)
Se ha referido en la literatura que pequeños componentes en zonas distales pueden ser manejados de forma conservadora con un seguimiento estrecho y bajo tratamiento anticoagulante y antiagregante. (2) Además de haber podido evaluar el seguimiento a los 4 años de una estrategia conservadora, la principal particularidad de nuestro caso radica en que se trata de un fragmento de considerable tamaño, con un trayecto que va desde el tronco común de la coronaria izquierda hasta la arteria circunfleja distal. El fragmento está fracturado a nivel del stent del TCI, lo que imposibilitó en su momento el retiro percutáneo con los métodos antes descriptos y cabe pensar que se optó por una estrategia conservadora para evitar una cirugía cardíaca que supondría un riesgo alto en una paciente con sus comorbilidades. Una vez más, nos basamos en la buena evolución que había presentado la paciente durante los últimos 4 años para descartar cualquier cambio en una estrategia que, contra todo pronóstico, parece estar dando buenos resultados.
Javier López Pais, Carlos G. Martínez Peredo, Juan Gorriz Magaña, Joaquín Alonso Martín
Hospital Universitario de Getafe. Servicio de Cardiología.
Madrid, España e-mail: javierlopezpais@gmail.com
BIBLIOGRAFÍA
1. Abdulrahman M, AI-Moghairi, Hussein S. AI-Amri. Management of retained intervention guide-wire: a literature review. Curr Cardiol Rev 2013;9:260-6. http://doi.org/bdww
2. Khonsari S, Livermore J, Mahrer P Magnusson P Fracture and dislodgment of floppy guidewire during percutaneous transluminal coronary angioplasty. Am J Cardiol 1986;58:855-6. http://doi.org/ d4bv8t
3. Hartzler GO, Rutherford BD, McConahay DR. Retained percu-taneous transluminal coronary angioplasty equipment components and their management. Am J Cardiol 1987;60:1260-4. http://doi. org/cvpq6r
4. Lotan C, Hasin Y, Stone D, Meyers S, Applebaum A, Gotsman MS. Guide wire entrapment during PTCA: a potentially dangerous complication. Cathet Cardiovascular Diagn 1987;13:309-12. http:// doi.org/fsrk44
5. Vrolix M, Vanhaecke J, Piessens J, De Geest H. An unusual case of guide wire fracture during percutaneous transluminal coronary angioplasty. Cathet Cardiovasc Diagn 1988;15:99-102. http://doi. org/dg78f9
6. López-Mínguez JR, Dávila E, Doblado M, Merchán A, González R, Alonso F. Rotura y atrapamiento intracoronario de una guía de angioplastia con el extractor de trombos X-Sizer en una angioplastia de rescate. Rev Esp Cardiol 2004;57:180-3. http://doi.org/bdwx
Rev Argent Cardiol 2016;84:373-375. http://dx.doi.org/10.7775/rac.es.v84. Í4.7955
Leiomiosarcoma primario cardíaco en una paciente embarazada
Presentamos el caso de una mujer de 19 años, que ingresó al Hospital Juárez de México con 34 semanas de embarazo con taquicardia, disnea y hemoptisis. En el servicio de urgencias se efectuó el diagnóstico de insuficiencia cardíaca y edema pulmonar agudo. La paciente no tenía ningún antecedente de enfermedad cardíaca. Las radiografías de tórax demostraron la congestión pulmonar propia del edema pulmonar agudo y el ecocardiograma bidimensional mostró la presencia de una tumoración dentro de la aurícula izquierda de 40 X 47 mm, pegada a la desembocadura de la vena pulmonar superior izquierda, sin evidenciar alteración alguna del resto de las estructuras cardíacas, como puede observarse en la Figura 1. Fue intervenida quirúrgicamente, pudiéndose extirpar completamente la tumoración y la totalidad de su base de implantación. La paciente y su hijo no tuvieron complicación alguna durante la cirugía, ni por someterse a circulación extracorpórea. El estudio histológico reveló un leiomiosarcoma pleomórfico, con alto grado de malignidad; los estudios histopatológicos se realizaron con actina específica de músculo, CD 34, desmina, mioglobina, vimentina y PS 100, lo que confirmó el leiomiosarcoma (Figura 2 A). La paciente rechazó el tratamiento con quimioterapia durante su embarazo; su hijo nació 5 semanas después sin ninguna anomalía al nacimiento, mediante cesárea. La paciente rechaza nuevamente tratamiento con
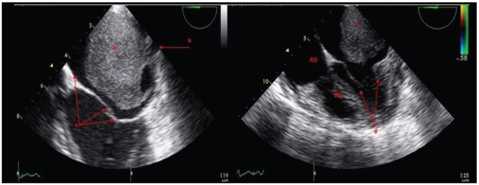
Fig. 1. Ecocardiograma transtorácico bidimensional en 2 y 4 cámaras, que muestra tumoración intraauricular izquierda (a), desembocadura de la vena pulmonar superior izquierda (b), contorno auricular (c) y válvula mitral libre (d). Véase la imagen color en la web. AD: Aurícula derecha. VD: Ventrículo derecho.
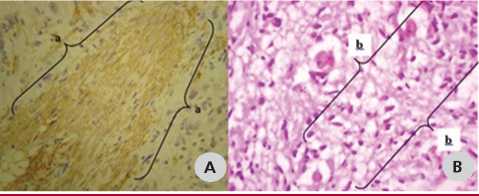
Fig. 2. A. Estudio histopatológico con actina específica de músculo; patrón fusocelular; diagnóstico de leiomiosarcoma cardíaco. B. Corte histológico con tinción de hematoxilina y eosina. 40x. Hipercelularidad de astrocitos. Astrocitoma de bajo grado.
quimioterapia y es reingresada un año después al presentar un tumor primario del sistema nervioso central, por el que fue intervenida quirúrgicamente. Se determinó que se trataba de un astrocitoma de bajo grado (Figura 2 B) sin relación con el tumor cardíaco, por lo que ambos se consideraron entonces tumores primarios.
Para el tratamiento del tumor del sistema nervioso central recibió manejo con quimioterapia y resección quirúrgica; sin embargo, la paciente fallece por complicaciones inherentes al procedimiento neu-roquirúrgico.
Las neoplasias cardíacas primarias son una enfermedad poco frecuente, con una prevalencia del 0,001% al 0,026% en series de autopsia; las más comunes son las metástasis o la invasión directa del corazón, cuyo origen procede de mama o de pulmón. (1)
Entre los tumores malignos primarios, los angio-sarcomas son más frecuentes, seguidos por el rab-domiosarcoma, el fibrosarcoma y el mesotelioma. El leiomiosarcoma se produce en menos del 1% de los casos malignos y es un tumor de origen mesenquimá-tico, que surge del tejido de células musculares lisas. En el corazón se localiza principalmente en la aurícula izquierda y las venas pulmonares. (2)
Comúnmente causan disnea, derrame pericárdico, dolor de pecho, arritmias auriculares, embolia periférica o insuficiencia cardíaca y, con menos frecuencia, pérdida de peso además de fiebre. Es un tumor altamente metastásico y con recurrencia amplia en el mismo sitio una vez que se realiza su resección. (3)
Por lo tanto, el pronóstico es malo, con una supervivencia media de 6 meses después del diagnóstico.
Muy a menudo, la caracterización de los sarcomas es difícil, pero el uso de marcadores inmunohisto-químicos permite la identificación más precisa y su posible diferenciación, ya que algunas áreas habitualmente tienen una alta celularidad. Los núcleos de las células del tumor se alargan de manera característica, con un grado variable de pleomorfismo; las figuras mitóticas se encontraron con una frecuencia amplia y la tinción inmunohistoquímica con el marcador de proliferación Ki-67 y las tinciones como alfa-actina de músculo liso y desmina son características, como en este caso. (2)
En el tratamiento de todo tumor cardíaco, la opción quirúrgica por sí sola no suele proporcionar la erradicación completa o efectiva, debido a que la neoplasia a menudo implica una gran área de miocardio, lo que frecuentemente lleva a una resección quirúrgica incompleta o a la diseminación sistémica. La supervivencia varía de una serie de casos a otra, con un promedio de entre 17 y 28 meses con extirpación quirúrgica completa y de 6 meses en los que no se puede realizar la resección completa. (4)
El papel de la quimioterapia adyuvante es todavía controversial; algunos estudios han encontrado que la quimioterapia posoperatoria convencional no parece modificar la evolución clínica, pero otros mostraron que la terapia combinada quirúrgica y adyuvante es efectiva. (1)
En conclusión, consideramos importante este caso porque al brindar el tratamiento quirúrgico oportuno se logró la erradicación completa del tumor maligno, logrando por cierto tiempo la supervivencia de la madre y su hijo; sin embargo, la generación de un nuevo tumor primario a nivel cerebral ocasionó la defunción de la paciente. Según la base de datos, es el primer caso en América Latina de un leiomiosarcoma cardíaco en una paciente embarazada.
Carlos N. Soberanis Torruco, Eder N. Flores López, Luis F. Arias Velarde, Carlos Ugarte Briones, Luis F. Covarrubias Gil, Tania Guerrero Marin
Hospital Juárez de México - Servicio de Cardiología.
Ciudad de México, México Dr. Eder Natanael Flores López Hospital Juárez de México Av. Instituto Politécnico Nacional Número 5160 Colonia Magdalena de las Salinas México DF, CP: 07760 Tel. 58257924 e-mail: dr.eder.natanael@msn.com
BIBLIOGRAFÍA
1. Pacini D, Careddu L, Pantaleo A, Parolari A, Leone O, Daprati A, Gargiulo GD, Di Bartolomeo R. Primary malignant tumors of the heart: Outcomes of the surgical treatment. Asian Cardiovasc Thorac Ann 2015;23:645-51. http://doi.org/bjm8
2. Winther C, Timmermans-Wielenga V, Daugaard S, Mortensen SA,
Sander K, Andersen CB. Primary cardiac tumors: a clinicopathologic evaluation of four cases. Cardiovasc Pathol 2011;20:63-7. http://doi. org/fczfp4
3. Wang JG, Cui L, Jiang T, Li YJ, Wei ZM. Primary cardiac leiomyo-sarcoma: an analysis of clinical characteristics and outcome patterns. Asian Cardiovasc Thorac Ann 2015;23:623-30. http://doi.org/bjm9
4. Neragi-Miandoab S, Kim J, Vlahakes GJ. Malignant tumours of the heart: a review of tumour type, diagnosis and therapy. Clin Oncol (R Coll Radiol) 2007;19:748-56. http://doi.org/fv93rc
Rev Argent Cardiol 2016;84:375-377. http://dx.doi.org/10.7775/rac.es.v84. Í4.8939














