Introducción
Los HAPs, son contaminantes orgánicos persistentes (COPs), que se originan en la combustión incompleta de la materia orgánica causada por acontecimientos naturales (e.g. actividades volcánicas, incendios forestales) o actividades antrópicas (e.g. combustión de combustibles fósiles, incineración de desechos sólidos y derrame de petróleo), afectando la salud humana y el medio ambiente (Spagnuolo et al., 2016; Jajoo, 2017). La mayoría de los HAPs son volátiles y se adhieren a partículas en la atmósfera, transportándose y depositándose a grandes distancias, lo que genera problemas a escala mundial (Vives et al, 2001). En el ambiente, el antraceno puede encontrarse en concentraciones que varían desde 0,011 pM, en suelos que no se consideran contaminados, hasta 561 pM en suelos altamente alterados como el del alquitrán de hulla (Nadal et al., 2004; García-Sánchez et al., 2018).
Las plantas juegan un papel importante en el ciclo y destino de los HAPs, debido a que tienen la capacidad de absorberlos del ambiente, translocarlos, transformarlos y bioacumularlos (Tao et al., 2004; Gao et al., 2013). Los HAPs afectan tanto la fisiología como la morfología de plantas vasculares produciendo necrosis, clorosis y disminución de la biomasa, entre otros (Liu et al., 2009; Oguntimehin et al., 2010). Sin embargo, es escaso el conocimiento sobre el efecto de estos contaminantes en la fisiología de las plantas avasculares.
Las briofitas (sensu lato) son un grupo de plantas que incluye tres phyla: Anthocerotophyta (antocerotes), Marchantiophyta (hepáticas) y Bryophyta (musgos, sensu estricto), y están representadas por 14.000 a 15.000 especies a nivel mundial (Chandra et al., 2017). Dado que el gametofito carece de un sistema radicular y vascular, reacciona de manera rápida y directa a los cambios ambientales, por lo que la tolerancia a condiciones adversas es necesaria para la aclimatación de dichos organismos a diferentes ambientes (Bates, 1992). Con respecto a la contaminación por HAPs, se ha documentado que algunas especies pueden incorporarlos en forma gaseosa y en partículas sólidas, acumulándose principalmente en la pared celular (Keyte et al., 2009; Spagnuolo et al, 2016).
Algunas especies de hepáticas (phylum Marchantiophyta) son capaces de colonizar sitios con alto impacto antrópico (Alam & Sharma, 2012). Una de ellas es Lunularia cruciata (Linn.) Dumort., (familia Lunulariaceae, orden Lunulariales), una especie considerada bioindicadora de metales pesados (Carginale et al., 2004). Resulta fundamental estudiar el efecto de los contaminantes en los sistemas biológicos para establecer bioindicadores de toxicidad fiables (Huang et al., 1997). Dado que L. cruciata es tolerante a los ambientes disturbados por actividades antrópicas, es un organismo ideal para el estudio in vitro de toxicidad por HAPs. El objetivo de este trabajo fue estudiar los cambios morfológicos y fisiológicos de L. cruciata expuesta al antraceno, para evaluar su posible rol como organismo indicador de este contaminante. Además, se estudió si esta especie podría cumplir algún rol como organismo secuestrador del contaminante mediante su bioacumulación.
Materiales y Métodos
Material de estudio
Los ejemplares de L. cruciata se obtuvieron en Argentina, Prov. Rio Negro, San Carlos de Bariloche (41° 08’ 32,0” S, 71° 18’ 36,7” O). Las plantas fueron identificadas según caracteres morfológicos siguiendo la bibliografía de Hassel de Menéndez (1959).
Cultivos in vitro
Para los cultivos in vitro se colectaron gemas de los conceptáculos y se esterilizaron siguiendo el protocolo de Silvani et al. (2012). Luego se sembraron en placas de Petri de vidrio (90 mm de diámetro) con medio de cultivo mínimo (Bécard & Fortin, 1988), a pH 6,2-6,3. Se mantuvieron en cámara de cultivo con un fotoperiodo de 16/8 h de luz y oscuridad (42 pmol s-1 m-2). Las condiciones de temperatura y humedad fueron 22,1°C y 48,1 % respectivamente.
Germinación de gemas
El antraceno se agregó al medio de cultivo según la metodología de Aranda et al. (2013). Se preparó una solución stock de antraceno en acetona, que se dosificó a los medios de cultivo para obtener las concentraciones 100 y 280 pM/l (dos tratamientos) más un tratamiento control que consistió en medio de cultivo mínimo sin antraceno con igual dosis de acetona. Se sembraron 100 gemas estériles por tratamiento, en un mínimo de cuatro réplicas (Spinedi et al., 2019). A los tres días se cuantificó el porcentaje total de germinación para cada tratamiento, utilizándose la emergencia de rizoides como indicador de germinación (Valió & Schwabe, 1969).
Desarrollo de las plantas
Las gemas germinadas se pasaron a placas de Petri con medio de cultivo en las mismas concentraciones antes descritas (seis réplicas por tratamiento) y los experimentos se repitieron tres veces. Transcurridos 60 días se registró la morfología y el crecimiento mediante superficie del talo y biomasa total (Spinedi et al., 2019). Para la medición de la superficie, la planta se fragmentó y se escaneó con un escáner (HP Scanjet G2410). Las imágenes se analizaron con el programa imageJ (https://imagej.nih.gov/ij). Para la medición de la biomasa se secaron las plantas en estufa a 70 °C durante 48 horas, registrándose el peso en una balanza analítica (OHAUS AP250D).
Bioacumulación de antraceno
La presencia de antraceno en el interior de las plantas se analizó mediante microscopia de fluorescencia siguiendo los protocolos descritos por Spinedi et al. (2019). En un microscopio de fluorescencia Olympus Bx51 (Olympus Optical Co., Tokio, Japón), se irradiaron las plantas con longitudes de onda de 330 y 375 nm, midiéndose la emisión a 420 nm. Las imágenes obtenidas se analizaron con el programa ImageJ (https://imagej. net/Fiji) obteniéndose la intensidad de fluorescencia (en unidades arbitrarias UA) en 20 paredes celulares por tratamiento. La concentración de antraceno en las plantas se analizó por cromatografía líquida de alta resolución (HPLC, Agilent 1100) siguiendo los protocolos descritos por Aranda et al. (2013). Las separaciones de los analitos se llevaron a cabo en una columna de fase reversa Sinergy Fusión RP 80A C18 (4 pm, 3,9 x 150 mm), usando acetonitrilo y un buffer de fosfatos como fases móviles y se midió en una longitud de onda entre 210 a 280 nm con un detector de diodos de array. Los resultados se expresaron en pmoles mg-1 y se calculó el porcentaje de absorción de antraceno en los diferentes tratamientos.
Contenido de clorofila
El contenido de clorofila a y b se analizó según el protocolo de Sims & Gamon (2002). Se registró el peso fresco de tres talos por tratamiento y se homogenizaron con 1 ml de acetona/Tris buffer (80:20 V: V, pH 7,8). Se llevó a volumen final de 3 ml y se centrifugó (2500 rpm, 10 minutos). Se midieron las longitudes de onda: 537, 647 y 663 nm, con un espectrofotómetro (UV-1800, Shimadzu UV). Los contenidos de clorofila a y b se calcularon en valores relativos con respecto al total de clorofila, lo cual nos brinda información sobre la variación porcentual de cada pigmento. Además, se calculó la relación entre los contenidos de clorofilas a y b.
Análisis de datos
Los datos se analizaron con el programa STATISTICA. Para comparar los tratamientos se aplicaron las pruebas estadísticas de comparaciones múltiples ANOVA de una vía y se contrastaron con el test de Tukey y de Diferencia Significativa Mínima (DSM) de Fisher (p < 0,05). Las imágenes tomadas con el microscopio de fluorescencia se analizaron con el programa Fiji (ImageJ).
Resultados
Germinación de gemas
Con respecto al porcentaje de germinación de las gemas de L. cruciata no se encontraron diferencias significativas entre las distintas concentraciones de antraceno y el control (p > 0,05) (Fig.1). Por otra parte, el comportamiento entre el porcentaje de germinación y el posterior desarrollo de las plantas (Fig. 2) fue diferente entre las distintas concentraciones de antraceno.
Desarrollo de las plantas
Se observó que las plantas expuestas al antraceno presentaron morfología de apariencia “arrosetada”. Por otra parte, en ausencia del contaminante el crecimiento fue dicotómico y aplanado sobre el sustrato (Fig. 2A). Con respecto al crecimiento, se encontró una disminución de la superficie total del talo en los tratamientos con antraceno con respecto a las plantas control, siendo las diferencias significativas (p < 0,05) (Fig. 2B). Además, la biomasa de las plantas disminuyó progresivamente al incrementarse la concentración de antraceno, siendo las diferencias significativas entre los distintos tratamientos (p < 0,05) (Fig. 2C).
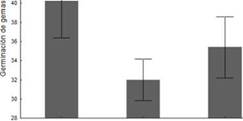
Fig. 1: Porcentaje de germinación de gemas de L. cruciata en los distintos tratamientos. Las barras indican media ± ES (n= 100; ANOVA de una vía, prueba de Tukey post-hoc, p > 0,05).
Bioacumulación de antraceno
Las plantas desarrolladas en presencia de antraceno presentaron un aumento significativo de la intensidad de fluorescencia entre 450495 nm (34682 ± 2441 y 40731 ± 2945 UA respectivamente) siendo significativamente diferentes al control (28448 ± 2072 U.A; p < 0,05) (Fig. 3). Por otra parte, el porcentaje de absorción de antraceno por las plantas fue diferente entre los distintos tratamientos. El mayor porcentaje promedio de absorción correspondió a las plantas sometidas a 100 pM de antraceno (24,2 %), mientras que las plantas desarrolladas en 280 pM presentaron un porcentaje de 9,4 %.
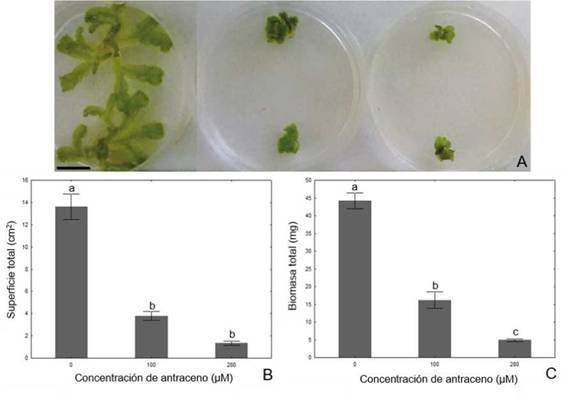
Fig. 2: Cultivo in vitro de L. cruciata, de izquierda a derecha: control, 100 y 280 pM (A). Se observó una morfología de apariencia “arrosetada” en las plantas expuestas al contaminante. Escala= 1 cm. Superficie (B) y biomasa (C) total de L. cruciata desarrollada en los distintos tratamientos. Las barras indican la media ± ES. Letras diferentes indican diferencias significativas (n= 3; ANOVA de una vía, prueba de Tukey post-hoc, p < 0,05).
Contenido de clorofila
Se encontró que el contenido total de clorofila (mg/g) no difirió entre las plantas control y aquellas desarrolladas en las diferentes concentraciones de antraceno (p > 0,05) (Fig. 4A). Sin embargo, las plantas control presentaron mayor porcentaje de clorofila a (70,1 ± 0,8 %) con respecto a los
tratamientos 100 pM (66,9 ± 0,8 %) y 280 pM antraceno (67,7 ± 0,5 %) (p < 0,05; Fig. 4B). Por otro lado, las plantas desarrolladas en presencia de antraceno presentaron un mayor porcentaje de clorofila b que el control, siendo los valores para 100 pM = 33 ± 0,8 %; 280 pM = 32 ± 0,5 %; control = 29,8 ± 0,8 % (p < 0,05) (Fig. 4C). Por último, la relación de clorofila a y b disminuyó en las plantas expuestas al antraceno con respecto al control (p < 0,05) (Fig. 4D).
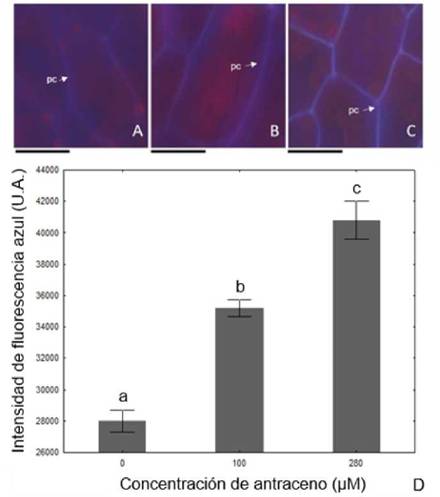
Fig. 3: Imágenes de microscopía de fluorescencia de plantas de L. cruciata desarrolladas en los tratamientos control (A), 100 pM (B) y 280 pM (C). Las flechas indican la pared celular (pc), observándose la mayor intensidad de fluorescencia azul en los tratamientos con antraceno. Escala= 20 pm. Intensidad de fluorescencia azul (UA) en paredes celulares correspondiente a los tratamientos control, 100 y 280 pM de antraceno (D). Las barras indican la media ± ES. Las letras diferentes indican diferencias significativas entre los tratamientos (n= 3; ANOVA de una vía, prueba de Tukey post hoc, p < 0,05).
Discusión y Conclusiones
En este trabajo se estudiaron los cambios morfológicos y fisiológicos de L. cruciata en respuesta a la presencia de antraceno, para determinar su rol como organismo indicador de contaminación por HAPs. Dado que la principal forma de dispersión de L. cruciata es mediante la producción de gemas, la germinación de los mismos se utilizó para evaluar el efecto de la contaminación por antraceno. Se encontró que este contaminante no afecta el proceso de germinación, por lo tanto, no tendría un efecto tóxico sobre las gemas. También, Spinedi et al. (2019) demostraron que el antraceno no afecta la germinación de las gemas de Marchantía polymorpha. Por lo tanto, para la especie de estudio, la germinación de gemas no sería un indicador factible para medir estrés por toxicidad mediados por HAPs.
Las plantas de L. cruciata fueron capaces de sobrevivir y desarrollarse en las diferentes concentraciones de antraceno. Se ha documentado que esta especie es tolerante a la contaminación por metales pesados (Carginale et al, 2004; Alam & Sharma, 2012). Aunque L. cruciata demostró ser resistente a la contaminación por antraceno, presentó una disminución del crecimiento y una morfología de apariencia “arrosetada”, muy diferente a su desarrollo natural. Resultados similares se han encontrado en M. polymorpha, cuyo crecimiento y morfología se vieron alteradas en presencia de antraceno (Spinedi et al., 2019). En plantas vasculares, el antraceno causa disminución de biomasa, junto con alteraciones en el crecimiento y el fenotipo (Wieczorek & Wieczorek, 2007; Jajoo et al., 2014). Las alteraciones en la fisiología y morfología en respuesta a la contaminación ambiental son útiles para establecer organismos bioindicadores (Garrec & Van Haluwyn, 2002). Por lo tanto, el cambio en la morfología y la disminución del crecimiento de L. cruciata en presencia de antraceno sitúa a esta especie como un promisorio bioindicador de contaminación por HAPs.
Se ha demostrado que varias especies de briofitas pueden absorber HAPs en forma gaseosa y en partículas sólidas, acumulándose principalmente en la pared celular (Keyte et al., 2009; Spagnuolo et al, 2016). En este trabajo, las plantas expuestas al antraceno presentaron mayor fluorescencia azul en las paredes celulares, indicando la localización de este contaminante en dicha estructura. Dada la naturaleza hidrofóbica del antraceno, se asocia a varios componentes de la pared celular, tales como pectinas, lignina, hemicelulosa y celulosa (Harms, 1996). Se ha documentado que el transporte de nutrientes y contaminantes es apoplásico en las briofitas (Giordano et al., 1989; Carginale et al., 2004), esto explicaría por qué el antraceno quedó retenido entre las paredes celulares. Por otra parte, se registró que L. cruciata satura su capacidad de acumulación de antraceno a concentraciones iguales o mayores a 100 pM. Si bien en plantas vasculares, la tasa de absorción de HAPs del suelo está correlacionada con la concentración del contaminante (Abdel-Shafy & Mansour, 2016), los resultados demuestran una rápida saturación de bioacumulación de antraceno a concentraciones por encima de 100 pM. El hecho de que L. cruciata haya bioacumulado antraceno es un claro indicio de que esta planta disipó el HAP del medio.
Mediante el estudio del contenido de clorofila y la relación clorofila a/b se puede medir la actividad fotosintética en plantas expuestas a HAPs (Marwood et al., 2001). Aunque el contenido total de clorofila no difirió estadísticamente en las plantas de L. cruciata desarrolladas en presencia y ausencia de antraceno, el contenido relativo de clorofila a disminuyó en presencia del contaminante. Se ha documentado en plantas vasculares expuestas al antraceno una disminución del contenido de clorofila (Huang et al., 1997; Jajoo et al., 2014). Esto se puede deber a la interacción de los HAPs con la molécula del pigmento o por la inhibición de su síntesis (Kummerová et al., 2006; Oguntimehin et al., 2010). Ciertas especies de briofitas expuestas a hidrocarburos presentaron una disminución del contenido de pigmentos fotosintéticos y de la eficiencia de la fotosíntesis (Nydahl et al., 2015). El antraceno, al ser un compuesto hidrofóbico puede incorporarse en las membranas de los tilacoides y generar un disturbio en el transporte de electrones deteriorando los fotosistemas (PSII y PSI) (Mallakin et al, 2002; Aksmann & Tukaj, 2004). En trabajos recientes, se ha encontrado que el antraceno afecta principalmente al PSI dado el bloqueo del transporte de electrones provenientes del PSII (Huang et al., 1997; Jajoo, 2017). Dado que la clorofila a es el pigmento más abundante en el PSI (Taiz & Zeiger, 2006), su disminución en L. cruciata estaría indicando que el antraceno podría estar afectando principalmente al PSI. Además, dado que la clorofila b es más abundante en el PSII, su aumento en plantas de L. cruciata expuestas al antraceno indicaría que el PSII no estaría siendo afectado por el contaminante. Por lo tanto, el cambio en el contenido de pigmentos fotosintéticos podría inducir cambios en el proceso de la fotosíntesis, afectando al crecimiento y la producción de biomasa en las plantas (Jajoo, 2017).
En conclusión, el antraceno no afectó estadísticamente la germinación de gemas de L. cruciata, por lo que dicho parámetro no sería un buen indicador de estrés por toxicidad causada por el HAP. Sin embargo, el cambio en la morfología junto con la disminución del crecimiento en plantas expuestas al antraceno, podrían ser parámetros útiles como bioindicadores. Por otro lado, esta especie fue capaz de absorber y bioacumular el contaminante principalmente en la pared celular. Aunque L. cruciata podría ser útil como organismo secuestrador del contaminante, su capacidad de acumulación saturó a concentraciones iguales o mayores a 100 pM. Por otra parte, el contenido total de clorofila no se vio afectado estadísticamente en plantas expuestas al antraceno, sin embargo, se registró una disminución del contenido relativo de clorofila a y un aumento de la clorofila b. Esto podría indicar que el antraceno estaría afectando el proceso de fotosíntesis, causando una disminución del crecimiento en las plantas.
Contribución de los autores
SR y SN realizaron los experimentos y los análisis de datos. AE llevo a cabo el análisis de antraceno mediante HPLC. SF se encargó del aislamiento in vitro de L. cruciata. SJM realizó el diseño experimental del manuscrito, estuvo a cargo de la dirección y planificación general, así como también concibió la idea original del estudio. Todos los autores participaron en la escritura del manuscrito.
Agradecimientos
Este trabajo fue posible gracias al financiamiento de la Agencia Nacional de Promoción Científica y Tecnológica (PICT 2019-00073) y de la Universidad Nacional del Comahue (PIN I-04 / B216), los cuales fueron obtenidos por SJM. La colaboración de la Dra. Aranda para la obtención de datos a través del contrato Ramón y Cajal (RYC-2013-12481) del Ministerio de Economía y Competitividad y fondos FEDER.












 uBio
uBio 

