1. INTRODUCCIÓN
En las últimas décadas, en la provincia de Santiago del Estero, se están impulsando las forestaciones con Prosopis alba Griseb. (Fabaceae, Mimosoideae); árbol que ocupa una posición dominante en la vegetación leñosa nativa de zonas áridas y semiáridas de América por sus características ecofisiológicas (Fagg y Stewart, 1994; Villagra, 2000). Además, posee una madera muy valorada por sus propiedades físico-mecánicas (Martínez et al., 2017) y sus frutos son utilizados como alimento humano y como forraje para animales (Fagg y Stewart, 1994; Ewens y Felker, 2010; Sciammaro et al., 2015).
Actualmente se está avanzando en investigaciones para lograr un manejo sustentable de las plantaciones de P. alba. En la bibliografía se destacan estudios sobre crecimiento; densidad de plantación; tratamientos de poda, técnicas de raleo, productividad y costos (Juárez de Galíndez et al., 2005; 2008; Coronel de Renolfi et al., 2014; Kees et al., 2018, entre otros). Asimismo, conocer sobre el estado sanitario y en particular sobre la presencia de insectos perjudiciales es clave para el buen desarrollo de las plantaciones. Sobre este tema en la literatura se citan estudios referidos a insectos que ocasionan daños a P. alba en su hábitat natural (Fiorentino y Diodato de Medina, 1991; Fiorentino et al., 1995) y en etapa de vivero (Diodato y Carabajal de Belluomini, 2006; Carabajal de Belluomini y Fiorentino, 2006; Carabajal de Belluomini, 2009) donde la presencia de insectos fitófagos produce mayores daños.
En la mayoría de las plantaciones forestales de América se describen graves daños producidos por hormigas cortadoras de hojas (HCH) (Braga et al., 2010; Zanetti et al., 2014; Zanuncio et al., 2016; Lemes et al., 2016). Sin embargo, existen escasos antecedentes sobre las especies, ecología, comportamiento, impacto y métodos de control de las HCH en plantaciones de P. alba de la provincia de Santiago del Estero.
El control de las HCH puede realizarse aplicando distintos métodos mecánicos, físicos, biológicos, culturales y químicos (Boaretto y Forti, 1997). Este último es el más utilizado a pesar de sus desventajas ambientales y económicas que lo convierten en un método poco viable para el control de estos insectos (Córdoba, 2010), por lo que es imprescindible la búsqueda de otras alternativas (Montoya-Lerma et al., 2012).
Una alternativa biológica para el control de HCH es la utilización de hongos entomopatógenos. Estos son organismos que tienen un importante valor ecológico, por ser reguladores de poblaciones de insectos, formando parte de una opción viable para la elaboración de bioplaguicidas (Delgado y Murcia-Ordoñez, 2011). Entre las principales especies habitualmente utilizadas como agentes de control biológico se encuentra Beauveria bassiana (Cañedo y Ames, 2004). En la bibliografía se citan varios estudios sobre el control de HCH con esta especie arrojando resultados promisorios (Escobar et al., 2002; Santos et al., 2007; Castro y Martínez, 2008).
Otra alternativa para el control biológico de HCH es el uso de cepas de hongos antagonistas (Ortiz y Orduz, 2001). Este método consiste en inducir la colonización y destrucción de los jardines del hongo simbionte, del cual se alimentan las hormigas, a través de la aplicación de una cepa antagonista (López y Orduz, 2003). Tal es el caso de Aspergillus sp., y Penicillium sp., que son hongos de amplia distribución en la naturaleza y que han demostrado resultados aceptables (Serratos-Tejeda et al., 2017).
Desde una perspectiva más artesanal, los productores agroecológicos de Centroamérica utilizan el “moho verde” de la naranja para controlar a las HCH. Se trata de un conjunto de cepas, conocido como “moho verde”, que está formado principalmente por Penicillium spp. (Ochoa et al., 2007) que actuaría como antagonista del hongo cultivado por las HCH (Serratos-Tejeda et al., 2017).
Su forma de aplicación es variable y centrada en su traslado al interior del nido por parte de las hormigas (dispersión del moho sobre los caminos y entradas al nido, aspersión de soluciones acuosas, cebos tóxicos como por ejemplo los granos de arroz que son ampliamente utilizados, entre otros) (Dávila-Pino, 2018).
Por los antecedentes planteados, en el presente trabajo se propone: 1) identificar la especie de hormigas cortadoras de hojas más frecuente en una plantación de P. alba, del departamento Capital de Santiago del Estero; 2) caracterizar los nidos; 3) aplicar hongos entomopatógenos y antagonistas para el control y 4) evaluar insecticidas químicos.
2. MATERIALES Y MÉTODOS
El estudio se realizó en una plantación experimental de Prosopis alba ubicada en la localidad de San Martín, departamento Capital, Santiago del Estero (27º 56´ 46.9” S 64º 13´ 17.4” N). La plantación fue establecida en el año 2008, en una superficie de 6 ha y nunca se realizó ningún tipo de manejo para el control de HCH.
En primera instancia se recorrió la plantación en su totalidad registrando nidos activos de HCH. Luego se seleccionaron al azar 18 nidos de apariencia semejante, considerando tamaño, número de orificios de entrada, forma del montículo de tierra y con actividad de forrajeo.
En cada nido seleccionado se realizó una descripción de la superficie del mismo detallando el tamaño, para lo cual se midieron el eje más largo y el más ancho para luego obtener la superficie de los mismos. Se contó la cantidad de orificios de entrada y se observó la presencia/ausencia de vegetación sobre el área del nido.
La intensidad de la actividad de forrajeo de los nidos seleccionados se determinó mediante un muestreo (Muestreo 0). Para ello, se utilizaron 5 trampas de caída ubicadas alrededor del nido a un metro de distancia del orificio de entrada principal. Las trampas fueron cebadas con cáscara de naranja para asegurar la captura de HCH (Bestelmeyer et al., 2000; Anglada et al., 2013) y estuvieron activas por 24 h por dos días consecutivos. La muestra corresponde a la suma de las cinco trampas y la variable a considerar es el número de individuos capturados por día. Los individuos capturados fueron identificados a nivel específico mediante la utilización de claves taxonómicas (Kusnezov, 1956; 1978; Mackay y Mackay, 2002; Fernández, 2003). Finalmente, la superficie, número de orificios de entrada de cada nido y la cantidad de individuos capturados fueron correlacionados mediante el coeficiente de Sperman, con el programa Infostat (Di Rienzo et al., 2011).
Para los ensayos de control químico y biológicos con hongos entomopatógenos y antagonistas respectivamente, se agruparon los nidos seleccionados en tres grupos de seis nidos cada uno de acuerdo a su proximidad (50 m a 100 m entre nidos del mismo grupo y 300 m a 400 m entre nidos de grupos distintos), de manera de garantizar la introducción al nido del correspondiente agente de control.
El primer tratamiento consistió en la aplicación de un insecticida formulado como cebo granulado, cuyo principio activo es sulfluramida (N-etil perfluorooctano- sulfonamida) al 0,3 %. La dosis de aplicación fue de 10 g del producto por metro cuadrado de tierra removida del hormiguero.
El segundo tratamiento consistió en la aplicación de un control biológico mediante granos de arroz contaminados con una cepa comercial B. bassiana. Para ello, 250 g de arroz fueron impregnados con 200 ml de la solución comercial, que contiene los conidios del hongo. La dosis de aplicación de este preparado fue de 10 g de granos de arroz por metro cuadrado de tierra removida del hormiguero.
En el tercer tratamiento se aplicó un cebo artesanal formado por granos de arroz contaminados con “moho verde”. Éste fue obtenido mediante la pudrición de un kilogramo de cáscaras de naranjas, una vez que se observó la presencia del moho se mezclaron con un kilogramo de arroz, luego se separaron los granos y se aplicó con una dosis igual al de los tratamientos anteriores.
Para evaluar la eficiencia de los métodos de control aplicados se realizaron tres muestreos, con la misma metodología que se detalló anteriormente para el muestreo 0. Los muestreos se realizaron a los 10 días (Muestreo 1), a los 30 días (Muestreo 2) y a los 60 días (Muestreo 3) de las aplicaciones
Todos los datos obtenidos en los cuatro muestreos fueron analizados mediante la prueba no paramétrico de Kruskal-Wallis debido a que no se pudo verificar el cumplimiento de los supuestos de normalidad y homogeneidad. Para ello se utilizó el programa estadístico Infostat (Di Rienzo et al., 2011)
3. RESULTADOS Y DISCUSIÓN
Identificación de la especie y caracterización de los nidos
Se capturaron en total 18.650 hormigas, las cuales fueron identificadas como Acromyrmex striatus Roger (Myrmicinae: Attini). A. striatus. Es endémica de América del Sur y, en Argentina, habita en regiones áridas y semiáridas entre las provincias de Jujuy y Rio Negro (Kusnezov, 1956; Bonetto, 1959, Farji-Brener y Ruggiero, 1994, Delabie et al., 2011, Simões-Gomes et al., 2016), por lo que se infiere que es natural su presencia en el sitio de estudio.
Los 18 nidos seleccionados se caracterizaron por presentar un área circular libre de vegetación de aproximadamente de 2,80 m. donde se encuentran 1 a 2 orificios de entrada (tabla 1). Se destaca en estos nidos la ausencia de un domo de tierra o un montículo de material vegetal seco, como es frecuente en la mayoría de HCH del género Acromyrmex (Farji-Brener, 2000; Farji-Brener y Sasal, 2003). Algunas especies de hormigas clarean la vegetación que crece sobre y alrededor del nido, con el fin de modificar características físicas circundantes como mayor disponibilidad de luz y de temperatura (Meyer et al., 2011). Los individuos de A. striatus tienen preferencia por temperaturas superiores a los 25 ºC. Esto explica la estructura superficial y el comportamiento de limpieza de la superficie de los nidos. Estas hormigas eliminan toda la vegetación sobre la superficie de las cámaras de cultivo de hongos con el objetivo que los rayos del sol impacten directamente sobre el nido y así la temperatura del suelo alcance valores elevados (Gonçalves, 1961; Nobua-Behrmann, 2014).
En el muestreo 0 se capturaron en promedio de 75,06 y 33,11 individuos por nido en los dos días respectivamente, observándose diferencias significativas entre los valores (H = 4,10; P = 0,042). No se detectaron diferencias significativas en la cantidad de hormigas capturadas entre los 18 nidos (H = 9,39; P = 0,09). El tamaño de los nidos y la cantidad de orificios de entrada no evidenciaron una correlación con la cantidad de individuos capturados (ρ = 0,20; p = 0,25 y ρ = 0,10; p = 0,54 respectivamente).
Tabla 1 Tamaño y cantidad de orificios de entrada de los nidos de Acromyrmex striatus estudiados, en la plantación de Prosopis alba en el departamento Capital de Santiago del Estero, y cantidad de producto aplicado en los distintos métodos de control.

Efectividad de los tratamientos aplicados
Según los valores observados en la tabla 2, existen diferencias significativas en la cantidad de individuos de A. striatus capturados en los muestreos realizados antes y después de la aplicación de los tratamientos.
La actividad de los seis nidos, donde se aplicó el control químico (Sulfluramida al 0,3 %), cesó de tal forma que en los últimos muestreos no se capturaron individuos de A. striatus (Tabla 2). Entre los métodos químicos de mayor efectividad se encuentra el empleado en este estudio, ya que las hormigas lo transportan fácilmente hacia el interior del hormiguero por la acción de un atrayente. El cebo utilizado contiene un ingrediente activo biodegradable en poco tiempo, conocido como Sulfluramida (Vergara, 2005), el cual resulto muy efectivo al eliminar el 100% de los nidos tratados, al poco tiempo de su aplicación. La dosis de aplicación de Sulfluramida está basada en la superficie que ocupa cada nido (Zanuncio et al., 2000). En este sentido, la dosis aplicada alcanzó resultados satisfactorios por lo que puede ser recomendada su administración en este tipo de plantaciones forestales. Sin embargo, el uso de Sulfluramida se encuentra cuestionado (Nuñez-Crespo y Olmedo, 2013), como consecuencia de que no es un insecticida específico y pueden causar efectos tóxicos indeseables para especies no objetivo, además, pueden contaminar el suelo y el agua.
Los cebos a base de arroz son sumamente atractivos para las HCH (Anglada et al., 2013), lo que originó conductas de aceptación hacia los dos métodos alternativos realizados. De esta forma B. bassiana y el “moho verde” fueron aceptados y cargados al interior de los nidos en su totalidad.
En el tratamiento con B. bassiana se observa que en el muestreo 1, luego de la aplicación, el número de individuos capturados aumentó con respecto al muestreo 0 y en los siguientes fue disminuyendo. Se observa que la menor cantidad de individuos se registra en el muestreo 0 y la mayor en el muestreo 1. Todos los valores obtenidos presentan diferencias significativas (Tabla 2). En los nidos donde se aplicó los granos de arroz contaminados con el “moho verde”, al igual que en el anterior, la cantidad de individuos capturados fue menor en el muestreo 0 y la mayor cantidad se obtuvo en el muestreo 1, sin embargo, entre los muestreos 1, 2 y 3 no se evidencian diferencias (Tabla 2).
Los datos obtenidos arrojan resultados no definitivos, lo que podría atribuirse a factores bióticos (susceptibilidad del hospedero, relación con los hospederos, presencia de medios de propagación, dispersión y persistencia de los hongos) y abióticos (rayos ultravioleta, temperatura y humedad relativa) que juegan un rol clave para que se produzca con éxito la manifestación epizoótica de los hongos utilizados (Hajek, 1997). Por ejemplo, varios autores demostraron que los rangos de temperatura para el crecimiento óptimo B. bassiana son de 15 a 25 °C (Doberski, 1981; Hallsworth y Magan, 1999). Por lo que probablemente B. bassiana no pudo desarrollarse en el interior de los nidos, por el comportamiento de A. striatus que eleva la temperatura dentro de los mismos, como se explicó anteriormente (ubicación, estructura exterior y limpieza de la superficie de los nidos), los que serían mecanismos de defensa efectivos contra entomopátogenos.
Por otro lado, algunos autores refieren a que la forma de aplicación de los hongos entomopatógenos es decisiva para lograr el control efectivo de HCH. Por ejemplo, Castro y Martínez (2008) observaron mayor probabilidad de éxito diluyendo los hongos con agua y aplicándolos directamente dentro de los nidos y en los caminos. Escobar y colaboradores (2002), probaron que la aplicación de cepas comerciales de B. bassiana, en forma de cebos preparados con avena y jugo de naranja, no afecta la actividad de forrajeo de las HCH. Estos autores atribuyen este resultado a la composición de los cebos fabricados para la comercialización de los productos biológicos, sumado a las condiciones ambientales del sitio, por lo que recomiendan identificar cepas nativas que garanticen una mayor eficacia.
La utilización del “moho verde” es una práctica artesanal y no se registran estudios científicos que corroboren o no su efectividad. Así también, existen pocos estudios referidos a la acción antagónica de Penicillium, hongo constituyente del “moho verde”, sobre las cepas del simbionte de las HCH. Serratos-Tejeda y otros (2017), son unos de los pocos autores que sugieren que este hongo es una alternativa agroecología para el control de las HCH. Sin embargo, estos autores afirman que la mayor efectividad de Penicillium se produce cuando se encuentra combinado con otros hongos antagonistas o con productos químicos.
En general, las HCH presentan comportamientos especializados de limpieza para eliminar agentes patógenos que puedan significar un riesgo para la colonia (Giraldo-Echeverri, 2009); junto a estrategias evolutivas que involucran a un tercer componente biológico dentro de la relación simbiótica, estas son bacterias que producen agentes antifúngicos que inhiben la germinación de los conidios del hongos (Currie, 2001; Currie et al., 2003; Santos et al., 2004), que también podrían haber originado los resultados observados.
Tabla 2 Promedio de individuos de A. striatus capturados en los muestreos realizados en la plantación de Prosopis alba, en la localidad San Martín, departamento Capital de Santiago del Estero.(D.E. = desviación estándar; prueba de Kruskal-Wallis, letras distintas (a, b y c) significan diferencias significativas P<0,05).
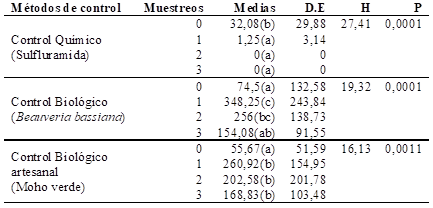
4. CONCLUSIONES
En el presente trabajo se exponen los primeros aportes en relación al empleo de diferentes alternativas de control para A. striatus asociada a P. alba en la localidad de San Martín, Departamento Capital, provincia de Santiago del Estero (Argentina).
Por los resultados obtenidos, se puede afirmar que para lograr con éxito el control de HCH con hongos entomopatógenos y/o antagonistas, es necesario, en primer lugar, conocer los requerimientos ecológicos de los hongos tales como la humedad relativa, temperatura, patogenicidad, virulencia y hospederos a los que infecta activamente (Meyling y Eilenberg, 2007); las relaciones ecologías entre insecto-entomopatógeno, es decir, los diferentes mecanismos que los hongos tienen para infectar a los insectos y los mecanismos que los insectos tienen para defenderse (Téllez-Jurado et al., 2009).
En consecuencia, se debe continuar realizando trabajos de investigación, con estos organismos u otros componentes alternativos que separados o combinados, presenten resultados similares a los logrados con productos químicos, pero con menos efectos nocivos en el ambiente y la salud. También es necesario estudiar la ecología y comportamiento de la diversidad de especies de HCH en la región y en particular las que se encuentran asociadas a plantaciones de Prosopis alba.














