Introducción
La obesidad es una enfermedad crónica multifactorial que altera la calidad de vida generando a nivel global un aumento de la morbimortalidad. Desde 1975, se ha casi triplicado en todo el mundo, siendo actualmente uno de los principales problemas de salud pública (1). La prevalencia de exceso de peso y obesidad en nuestro país, según los resultados de la 4° edición de la Encuesta Nacional de Factores de Riesgo, es de 61,6% y 25,3%, respectivamente. Evidenciándose una tendencia en aumento en comparación a las 3 ediciones previas (2). Múltiples paneles de expertos recomiendan que la base del tratamiento para las personas con obesidad es el abordaje integral de cambios en el estilo de vida, con el fin de inducir una pérdida mayor o igual al 5% del peso corporal, sumando el beneficio asociado sobre los factores de riesgo cardiometabólico (3-5).
El cambio de estilo de vida con métodos cognitivos conductuales y cambios en la alimentación sumados a la actividad física son los pilares del tratamiento de la obesidad, los cuales anteceden y acompañan al tratamiento farmacológico cuando correspondiera su indicación. Este último debe considerarse como parte de una estrategia integral del manejo de la enfermedad, permitiendo mantener la adherencia al tratamiento así como a prevenir y mejorar las comorbilidades relacionadas con la obesidad y la calidad de vida (6-10).
Según las Guías de práctica clínica canadienses para el tratamiento de la obesidad en adultos del año 2020, la farmacoterapia se puede utilizar (8):
En personas con un Índice de Masa Corporal (IMC) ≥30 kg/m2) o un IMC ≥27 kg/m2 con comorbilidades, junto con terapia médico nutricional, actividad física e intervenciones psicológicas (liraglutida 3 mg, combinación de naltrexona-bupropión, orlistat).
Para mantener la pérdida de peso que se ha logrado mediante cambios en el estilo de vida y para prevenir la recuperación de peso (liraglutida 3 mg u orlistat).
En personas con diabetes tipo 2 y un IMC ≥27 kg/m2 junto con cambios en el estilo de vida para perder peso y mejorar el control glucémico: liraglutida 3 mg, combinación de naltrexona-bupropión, orlistat.
En personas con prediabetes y sobrepeso u obesidad (IMC ≥27 kg/m2) para retrasar o prevenir la diabetes tipo 2 junto con cambios en el estilo de vida (liraglutida 3 mg; orlistat).
No se recomienda el uso de medicamentos recetados o de venta libre que no sean los aprobados para el control de peso.
Según la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), un fármaco efectivo para el descenso de peso es aquel que luego de un año de tratamiento, en al menos el 35% de las personas que reciban este fármaco, presente como resultado una pérdida del 5% del peso corporal total y ésta debe ser aproximadamente el doble en comparación con aquellos que reciben placebo (11). La eficacia de la farmacoterapia debe evaluarse después de los primeros 3 meses y periódicamente, al menos cada 3 meses. Se considera una pérdida de peso satisfactoria si esta es del 5% o más en personas con diabetes o del 3% o más, en personas sin diabetes. En el caso de no lograr dichos objetivos, la farmacoterapia debe ser suspendida (6,8,9).
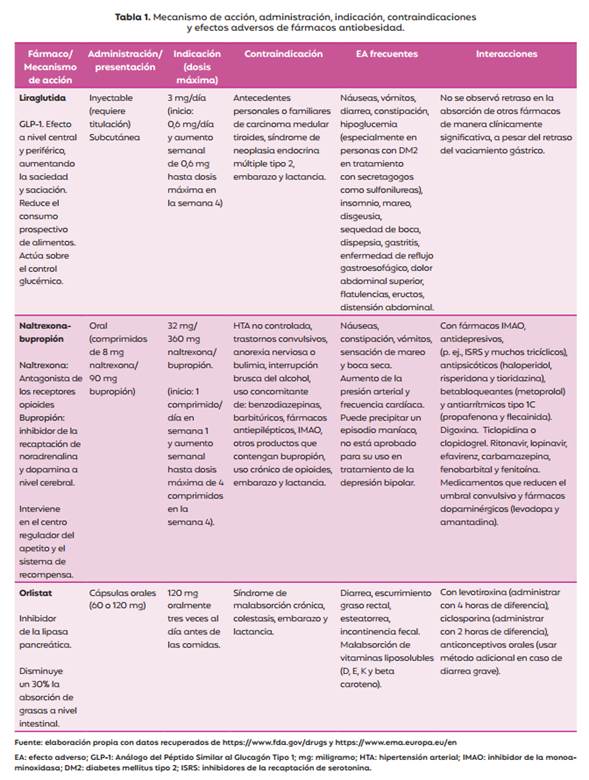
Hasta la actualidad las únicas drogas de uso específico a largo plazo para el tratamiento de la obesidad, autorizadas por la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica de la República Argentina (ANMAT) son: orlistat, naltrexona-bupropión y liraglutida; mientras que mazindol y fentermina son autorizadas para su uso, únicamente a corto plazo. Dichos fármacos también se encuentran autorizados para adultos, por la FDA y la Agencia Europea del Medicamento (EMA). El mecanismo de acción, la administración, indicación, las contraindicaciones y los efectos adversos (EA) de los fármacos, según los organismos mencionados se resumen en la tabla 1.
El objetivo de la presente revisión fue describir la evidencia actualizada y disponible a través de revisiones sistemáticas (RS) sobre la eficacia y seguridad de los fármacos aprobados en Argentina para el tratamiento a mediano y largo plazo de la obesidad en adultos.
Materiales y método
Se realizaron búsquedas en las siguientes bases de datos: Pubmed, Cochrane library, la Biblioteca Virtual en Salud (BVS) de la Biblioteca Regional de Medicina (BIREME), centro especializado de la Organización Panamericana de la Salud (OPS)/OMS, LILACS y Epistemonikos. La búsqueda se limitó a los idiomas español, inglés y portugués. Se crearon diferentes estrategias utilizando operadores booleanos y filtros. Los términos utilizados para la búsqueda se aplicaron al título y al resumen para aumentar la probabilidad de que la temática sea relevante en la publicación y se utilizaron las siguientes palabras clave: “obesity”; “obese”; “pharmacoterapy”; “pharmacological therapy”; “obesity medications”; “anti-obesity drugs”,“weight loss medications”; weight loss”; “adverse effects”; “efficacy”; “effectiveness”; “security”; “orlistat”; “naltrexone plus bupropion”; “liraglutide”; “systematic review”; “umbrella review”.
Con respecto a los criterios de elegibilidad, se seleccionaron revisiones sistemáticas (RS) con o sin metaanálisis, publicadas entre enero de 2015 y marzo de 2021, que hayan incluido ensayos clínicos controlados y aleatorizados (ECCAs), de fase 3 o 4, en los cuales se hayan comparado los fármacos orlistat, liraglutida o naltrexona más bupropión con un grupo control al cual se le haya administrado un placebo. Con respecto al tipo de resultado, se incluyeron revisiones que hayan evaluado la eficacia del fármaco a través de la pérdida de peso a los 12 meses de intervención, expresada en kilogramos o porcentaje de pérdida de peso y/o proporción de personas con pérdidas del 5 y el 10% del peso inicial. Por otro lado, que hayan evaluado la seguridad a través del reporte del tipo y/o la prevalencia de los EA de los fármacos. Con respecto al tipo de participantes, debían ser adultos de ambos sexos biológicos, con diagnóstico de obesidad (definida como la presencia de IMC ≥30 kg/m2), con o sin comorbilidades como diabetes, hipertensión arterial y dislipidemias. Se excluyeron revisiones con participantes pertenecientes a subpoblaciones específicas como personas con infección por el virus de la inmunodeficiencia humana (VIH), trasplante de órganos, síndrome de ovario poliquístico (SOP) y cáncer (12).
Adicionalmente a los indicadores utilizados en cada RS para expresar la pérdida de peso, se resumió dicha información a través del reporte de un rango del promedio de kilogramos (kg) adicionales de peso perdido en el grupo intervenido con el fármaco, en comparación con el grupo control. Dicho rango se construyó en base al valor mínimo y máximo de pérdida de peso reportada dentro de cada grupo de RS correspondientes al mismo fármaco. Los valores específicos de cada RS se reportaron posteriormente en las tablas correspondientes.
En relación a los métodos de selección de las revisiones, tres autoras realizaron una selección de los títulos y abstracts de manera independiente, para verificar el cumplimiento de los criterios de inclusión. Los textos completos fueron revisados por dos autoras por cada artículo, con el objetivo de confirmar la inclusión en la revisión. En el caso de desacuerdos, una tercera autora colaboró con la decisión final.
Los datos fueron extraídos a través de un formulario electrónico estandarizado basado en los ítems de la lista de verificación de la guía PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses) para la publicación de RS (13).
La evaluación de la calidad de las RS, se realizó a través de la herramienta de evaluación crítica de RS de estudios de intervenciones de salud, AMSTAR 2, la cual consiste en 16 dominios a través de los cuales se clasifican a las revisiones según cuatro niveles de confianza: alta, media, baja y críticamente baja (14).
Resultados
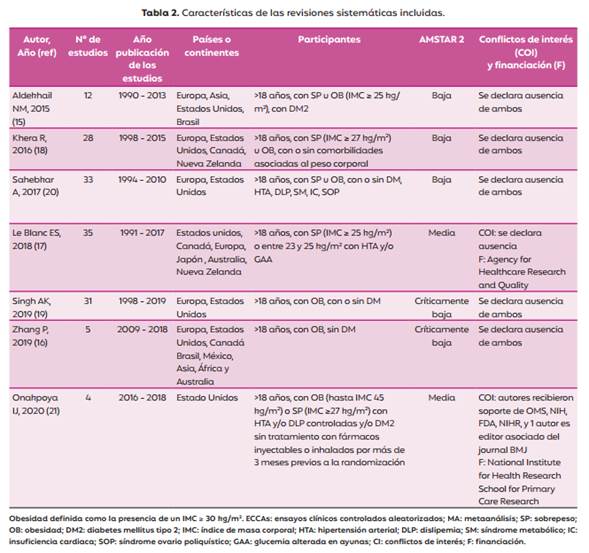
Se identificaron 183 RS potencialmente relevantes, de las cuales 7 fueron incluidas en la presente revisión, 6 de ellas con metaanálisis. El resto, quedó excluido por no cumplir con los criterios de elegibilidad o por estar duplicadas. Según la herramienta AMSTAR 2, ninguna de las RS incluidas presentó un nivel de confianza alta y 2 RS presentaron una calidad media (Tabla 2).
Entre los principales dominios críticos no cumplidos de la herramienta, se identificó la ausencia de un protocolo publicado, previo a la revisión y la ausencia de la lista de estudios excluidos con su correspondiente justificación.
Las revisiones incluyeron un rango de 5 a 35 ECCAs, realizados entre 1990 y 2019, principalmente en Estados Unidos y Europa (15-20). En 2 RS se incluyeron estudios realizados en Brasil como único representante de América del Sur (15,16). La herramienta Cochrane fue utilizada para evaluar la calidad de la evidencia de los ECCAs en 6 de las 7 RS. La revisión restante utilizó criterios desarrollados por “The U.S. Preventive Services Task Force” (USPSTF) (17).
Para reportar la pérdida de peso, se utilizó mayoritariamente la diferencia de medias (DM) o delta (∆) de la pérdida de peso expresada en kg, entre el grupo de intervención (fármaco) y el grupo control (placebo). Para reportar la cantidad de participantes que alcanzaron una pérdida de peso del 5% y del 10% o más, se utilizó el porcentaje (%) del total de participantes en cada grupo (intervención vs control) o el odds ratio (OR) entre dichos grupos.
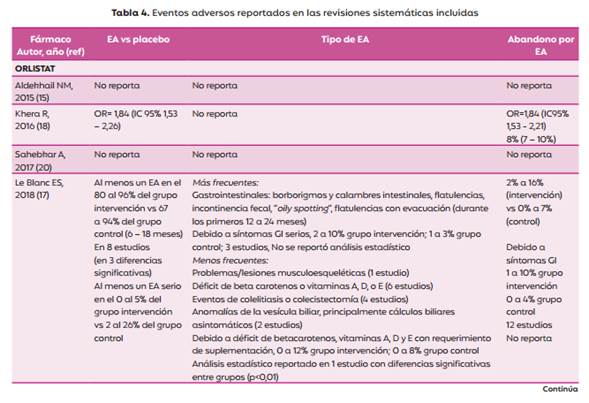
Los EA se reportaron utilizando una amplia variedad de indicadores como el OR entre el grupo de intervención vs. el grupo control, porcentaje de EA en cada grupo, y el tipo de EA más y menos frecuentes. En una RS (18) se reportó para todos los fármacos únicamente el OR de abandono del estudio debido a EA, sin especificar cuáles eran. Otras dos RS no informaron datos sobre los EA para orlistat (15,17).
El sesgo de publicación fue informado por 3 RS (16,18,19) a través de la utilización del funnel plots con ajustes “trim and fill” y el test de Egger, sin hallar evidencia de sesgo. 1 RS (17) no lo analizó debido a inconsistencias en el reporte de los resultados y 2 RS (15,20) no lo reportaron (Tabla 3).
Pérdida de peso
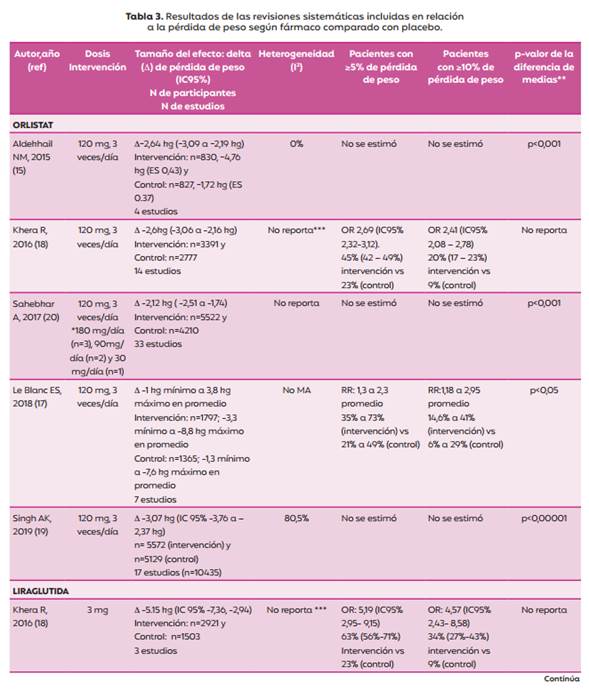
En todos los casos se hallaron diferencias significativas a favor del fármaco en cuanto a la pérdida de peso a los 12 meses de seguimiento. Las revisiones informaron los siguientes rangos promedio de diferencias de medias, expresadas en kg perdidos adicionales (delta de pérdida de peso) en el grupo de intervención en comparación con el grupo control:
Orlistat vs placebo: entre 2,12 a 3,07 kg con una dosis de 360 mg/día (5 revisiones)
Liraglutida vs placebo: entre 5,15 a 5,8 kg con una dosis de 3 mg (4 revisiones)
Naltrexona-bupropión vs placebo: entre 2,53 a 4,95 kg con dosis de 32/360 mg o 16/180 mg. En este caso se halló una mayor variabilidad en los resultados y en la dosis utilizada (4 revisiones).
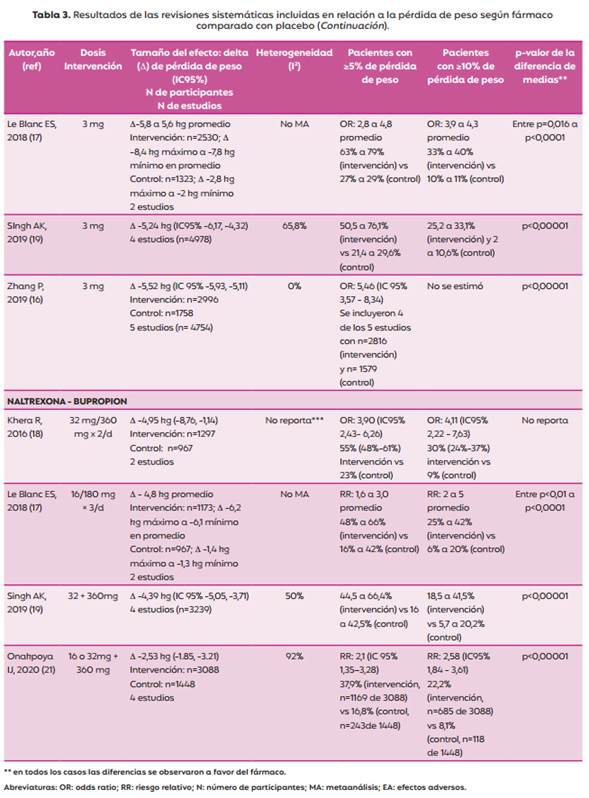
En la tabla 3 se puede visualizar con mayor detalle, el tamaño del efecto reportado en relación a la pérdida de peso, en cada RS incluida.
La heterogeneidad no fue reportada en 2 RS (18,20) y en 1 RS (17) no correspondió informarla ya que no se realizó un metaanálisis. En las 5 RS restantes, se observó principalmente una alta heterogeneidad (mayor al 50%) para todos los fármacos, excepto en 1 RS ante resultados sobre el orlistat (15) y en 1 RS con resultados sobre naltrexona-bupropión (19).
En relación con la cantidad de pacientes que alcanzaron una pérdida del 5 o 10% a los 12 meses de seguimiento, como indicador de relevancia clínica, se reportaron a través del OR o riesgo relativo (RR) del grupo de intervención respecto al grupo control y/o el porcentaje de pacientes que alcanzaron dichos resultados. Estos fueron diferentes según el fármaco como se detalla a continuación.
Pérdida del 5% del peso
El grupo intervenido con orlistat (2 de 5 revisiones), presentó entre 1,3 a 3 veces más probabilidad de alcanzar este porcentaje de pérdida de peso comparados con el grupo placebo y del 35 al 70% de los pacientes presentaron este resultado. En pacientes intervenidos con naltrexona-bupropión (4 de 4 revisiones), esa probabilidad fue algo mayor (entre 1,5 a 4 veces) y entre el 35 y el 70% de los participantes de este grupo. Por último, ante la administración de liraglutida (4 de 4 revisiones), se observó la mayor probabilidad (desde casi 3 a 5,5 veces más) respecto al grupo placebo y el resultado se observó en el 50 al 80% de los pacientes intervenidos con el fármaco (Tabla 3).
Pérdida del 10% del peso
En el grupo con orlistat (2 de 5 revisiones), la probabilidad de una pérdida del 10%, fue entre 1,2 a 2,9 veces más comparado con el grupo placebo y entre el 15 al 41% de los pacientes intervenidos con orlistat presentaron dicha pérdida. En relación al grupo con naltrexona-bupropión (4 de 4 revisiones), éste presentó entre 2 a 5 veces más probabilidad y en el 22 y el 42% se observó dicha pérdida. Finalmente, en el grupo con liraglutida (3 de 4 revisiones), se observó una probabilidad de 3,9 a 4,6 veces más que el grupo placebo y dicha pérdida se reportó en promedio, entre el 25 y el 40% de los pacientes intervenidos con el fármaco (Tabla 3).
Efectos adversos
Los diferentes EA del orlistat fueron descriptos en hasta el 96 y el 94% de los pacientes incluidos en el grupo intervención y placebo respectivamente, en 2 de 5 revisiones. Los más frecuentes fueron los gastrointestinales (GI) aunque, solo se reportó la prevalencia de los síntomas GI cuando éstos fueron serios, hallándose hasta 10% y 3%, dentro de los grupos intervención y placebo respectivamente.
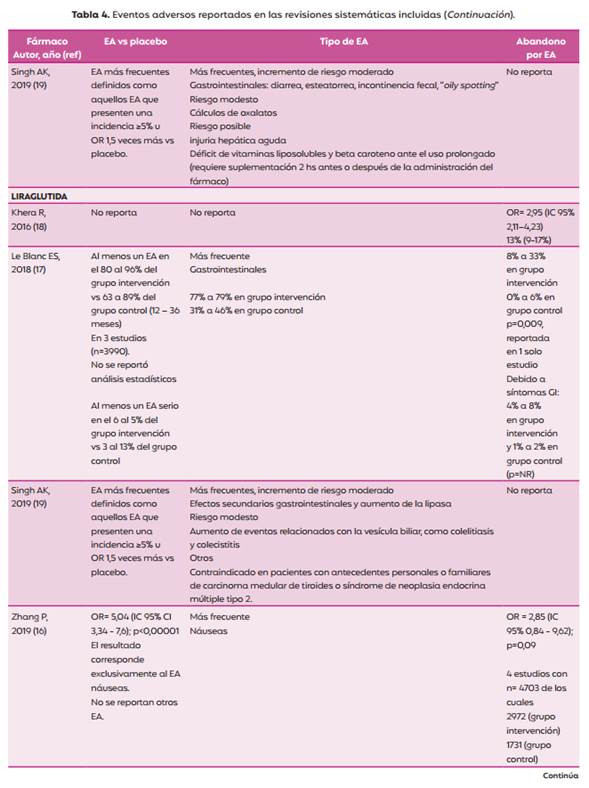
En el caso de la intervención con liraglutida, en 3 de 4 revisiones, también predominaron los EA GI, hasta un 79% comparado con hasta un 46% en el grupo placebo. En una de las revisiones (16), la probabilidad de presentar náuseas fue de 5 veces más en el grupo intervenido con el fármaco comparado con placebo.
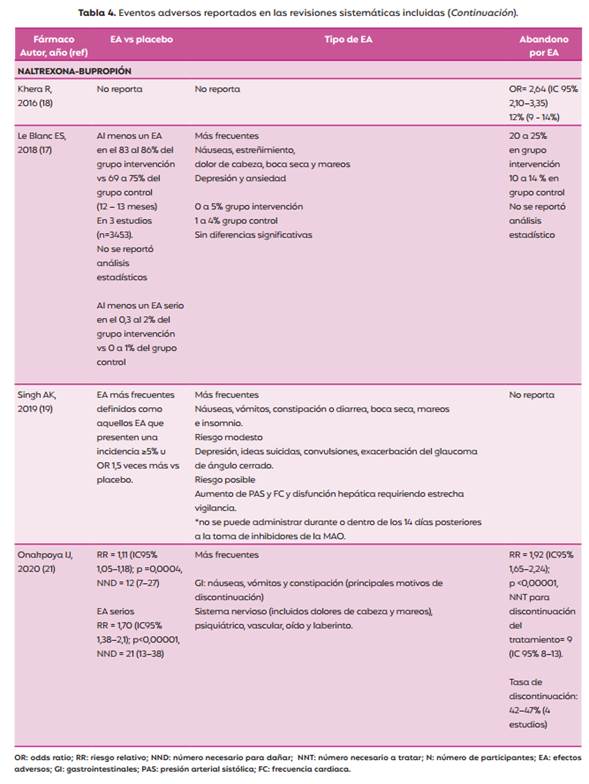
Por otro lado, ante la intervención con naltrexona-bupropión, en 3 de 4 revisiones, a los síntomas GI, se sumaron eventos relacionados con alteraciones en el sistema nervioso y la salud mental (insomnio, ansiedad, depresión, mareos, cefaleas), como los más frecuentemente observados. Al menos, uno de los eventos se presentó en hasta el 86% y el 75% de los casos dentro de los grupos intervención y control, respectivamente y al menos un evento serio en hasta el 2% y el 1% en los grupos mencionados respectivamente (Tabla 4).
Discusión
La presente revisión incluyó 7 RS de ECCAs y los resultados fueron comparados con los obtenidos en 2 revisiones de RS o umbrella reviews (UR), en todos los casos con un tiempo de intervención de 12 meses. La UR de Khalil H. et al. (22), incluyó 9 RS de 127 ensayos clínicos y la UR de Twells LK. et al. (23) incluyó 3 RS de un total de 61 ensayos clínicos sobre las intervenciones farmacológicas para la obesidad.
Con respecto a los efectos del orlistat, en nuestra revisión, los participantes del grupo intervención, perdieron un promedio de 2,12 a 3,07 kg adicionales, comparado con el grupo placebo, con una dosis de 360 mg/día en 5 RS de las 7 RS incluidas. De manera similar, en la UR de Twells LK. et al. (23) se halló, con orlistat utilizando la misma dosis (360 mg/día), una pérdida promedio de 2,6 kg adicionales, comparado con placebo en 1 RS; y en la UR de Khalil H. et al. (22), ante la misma dosis, se reportó una pérdida de 2,12 a 2,8 kg adicionales, comparado con placebo, en 5 RS.
La pérdida de peso con la administración de liraglutida en dosis de 3 mg diarios, hallada en nuestra revisión fue de 5,15 a 5,8 kg en promedio adicionales, en 4 RS. Twells LK. et al. (23), reportaron ante la misma dosis, una pérdida promedio de 2,9 a 5,2 kg más, comparado con placebo en 3 RS, observándose un rango más amplio de pérdida de peso adicional. Según Khalil H. et al. (22), la administración de liraglutida, evidenció una diferencia promedio de 1,31 kg con dosis de 1,2 mg diarios y de 1,7 kg con dosis de 1,8 mg diarios, comparados con placebo en 2 RS. En este caso se observan menores diferencias respecto al grupo placebo, debido a la inclusión de estudios en los cuales se administraron dosis menores a 3 mg.
Por último, las diferencias a favor de naltrexona-bupropión en nuestra revisión fueron en promedio entre 2,53 a 4,95 kg con dosis de 32/360 mg o 16/180 mg, en 4 RS. Estos fármacos presentaron un mayor rango en los resultados de pérdida adicional, en parte debido a las diferencias en las dosis administradas. Twells LK. et al. (23), reportaron una diferencia promedio de 5 kg a favor del fármaco ante una dosis de 32/360 mg en 1 RS, coincidiendo con el valor más alto del rango hallado en esta revisión, reflejando el mayor efecto de las dosis más altas. En la misma línea, en 1 RS analizada por Khalil H. et al. (22), la diferencia a favor de fármaco fue en promedio de 4,95 kg, comparado con placebo y con una dosis de 32/360 mg diarios. Las coincidencias en los resultados se deben en parte a que tanto Twells LK. et al. (23), como Khalil H. et al. (22), incluyeron una de las RS también analizada en esta revisión, habiendo superposición de artículos, aunque en nuestro caso se resumieron los datos de 4 RS en total y los otros autores analizaron solo 1 RS.
Los EA más frecuentes de todos los fármacos fueron los GI, influyendo en la discontinuación del tratamiento. Idénticos resultados se hallaron en la investigación de Khalil H. et al. (22), aunque en este caso relacionados principalmente al orlistat. Twells LK. et al. (23), no analizaron efectos adversos. La mayoría de la RS analizadas en nuestro trabajo, se basaron, en estudios realizados con la dosis máxima del fármaco, lo cual podría explicar, en parte, las altas tasas de EA y abandono del tratamiento. En este sentido, en otros estudios se ha identificado que una de las principales razones de la subprescripción de los fármacos para el tratamiento de la obesidad, son los EA, los cuales en su mayoría son dosis dependiente (24,25). En la práctica diaria, las prescripciones médicas difieren en las dosis y sus progresiones, según el tiempo de tratamiento, la tolerancia y los resultados individuales en la pérdida de peso, no alcanzando las dosis máximas en algunos casos. En Argentina, se agrega como barrera, el factor económico, ya que los fármacos presentan costos elevados, las coberturas por obras sociales y prepagas son variables y los fármacos no se encuentran cubiertos por el sistema público de salud. Esta situación también se ha observado en otros países (26,27).
Con respecto a las intervenciones adicionales en el estilo de vida, definidas como aquellas centradas en las modificaciones en la alimentación, actividad física y comportamiento, solo dos revisiones (15,18) describieron cointervenciones nutricionales y de actividad física. En los ensayos clínicos incluidos en dichas revisiones, se indicó mayoritariamente una reducción de 500 kilocalorías (kcal) del total de las recomendaciones de consumo energético diario, con una distribución estándar de macronutrientes o con reducción del porcentaje de grasas totales (menor al 30%), respecto del valor calórico total ingerido, característica de las dietas clasificadas como hipograsas. De la misma manera, es escasa la información sobre las intervenciones en la actividad física, ya que se halló este tipo de intervención en solo una RS incluida en nuestra revisión (18), a través de la indicación de realizar 150 minutos semanales de caminatas. La indicación de cambios en el estilo de vida agregada a las intervenciones farmacológicas para el descenso de peso, suelen ser moderadas a través de no más de una consulta mensual, posiblemente porque una intervención más intensiva podría enmascarar los efectos comparativos de la medicación (3,8).
Sin embargo, la adición de un fármaco para el tratamiento de la obesidad en programas intensivos de cambios en el estilo de vida, con participación de licenciados en Nutrición y especialistas en actividad física, ha demostrado mayor eficiencia, debido a la sinergia observada entre ambas intervenciones. En el estudio de Wadden TA. et. al. (28) se compararon intervenciones con abordaje intensivo en el estilo de vida exclusivamente en comparación con el mismo abordaje combinado con liraglutida 3 mg. A las 52 semanas, en el grupo con intervención no farmacológica, se observó una pérdida promedio del 6,1% del peso inicial, y el 44% perdió el 5% del peso o más. Los participantes que además recibieron liraglutida perdieron una media del 11,5% del peso inicial y el 70% perdió 5% del peso o más.
Por otro lado, las 4 RS analizadas en este trabajo, sobre los efectos de naltrexona-bupropión, incluyeron al estudio COR-BMOD (29). El mismo tuvo como cointervención a los fármacos y al placebo, el abordaje intensivo en el estilo de vida. En la semana 56 de seguimiento, los participantes tratados con naltrexona-bupropión en dosis de 32/360 mg/día, perdieron un 9,3 ± 0,4% del peso inicial, comparados con el grupo placebo, quienes perdieron el 5,1 ± 0,6% del peso inicial, observándose diferencias significativas.
La indicación de los cambios en el estilo de vida suele no reportarse o no describirse en detalle en las revisiones que incluyen ECCAs con fármacos antiobesidad, aunque dicha información es esencial, ya que la falta de adherencia tanto a los fármacos como a los cambios en el estilo de vida, refleja la gran heterogeneidad que presentan las personas con obesidad en cuanto a factores biológicos o de comportamiento, entre otros determinantes de la obesidad y este conocimiento puede orientar las diferentes decisiones terapéuticas. En este sentido, existe evidencia sobre el resultado de la indicación de este tipo de fármacos, teniendo en cuenta el fenotipo obesogénico de comportamiento ingestivo predominante. En el estudio de Acosta A. et al. (30), el grupo con intervención farmacológica guiado por fenotipo, presentó, a los 12 meses de seguimiento, una pérdida de peso casi 2 veces mayor al grupo con tratamiento no guiado por fenotipo (31). Las intervenciones nutricionales, no solo deberían ser adaptadas a las preferencias alimentarias, la cultura y estilos de vida de las personas con obesidad, sino también a los fenotipos de conducta alimentaria. En Argentina se ha validado la Escala de Fenotipos de Comportamiento Alimentario (EFCA), diseñada para identificar los fenotipos conductuales de la alimentación en adultos (32). Otro factor clave para obtener mejores resultados, es el abordaje por parte de equipos interdisciplinarios, que incluyan no solo médicos, sino también licenciados en Nutrición, especialistas en salud mental, profesores de actividad física y enfermeros, con una mirada integral de la persona (9).
Como limitaciones de la presente revisión, se puede mencionar que se ha incluido como variable resultado únicamente a la pérdida de peso. Por cuestiones de longitud del trabajo, no se incluyeron resultados en los parámetros cardiometabólicos y otras comorbilidades. Además, no se analizó el impacto de otros factores que influyen en la pérdida de peso, como los biológicos (sexo, gasto metabólico, edad, raza, etnia), calidad del sueño, fenotipo de conducta ingestiva, entorno obesogénico y adherencia a cambios en el estilo de vida, aunque como se mencionó anteriormente, los ECCAs sobre fármacos anitobesidad suelen describir de manera escueta o incompleta este tipo de factores o directamente no los tienen en cuenta. Además, los estudios se basan en los valores de IMC para identificar a las personas con obesidad, pero si bien los riesgos en la salud aumentan con el incremento del IMC, pueden variar según sexo, raza u origen étnico, edad y masa muscular, por lo que se sugiere la realización de estudios que analicen los efectos de las intervenciones en diversas poblaciones estratificadas no solo por IMC, sino también por los sistemas de clasificación emergentes, que incluyen la evaluación de la salud física, mental y funcional para caracterizar la gravedad de la obesidad (31,33-35). Finalmente, no se analizó el mantenimiento del peso perdido, donde surgen como barreras, la falta de modificaciones en el entorno obesogénico y los mecanismos adaptativos ante la pérdida de peso sobre el metabolismo y la regulación del apetito, como la disminución del gasto metabólico y el aumento del hambre, asociándose con la recidiva de la conducta alimentaria obesogénica y la reganancia de peso, por lo que se sugiere generar mayor evidencia al respecto para optimizar el abordaje en esta etapa (8).
Conclusión
Los fármacos estudiados para el tratamiento de la obesidad, a 12 meses de intervención, demostraron ser superiores al placebo en relación a la pérdida de peso. Entre los EA, que aumentan la discontinuación de los fármacos, predominan los GI. Es necesario evaluar el costo beneficio de su uso en cada caso en particular. La estrategia farmacológica se debería incluir en el marco de un tratamiento integral basado en intervenciones de cambio en el estilo de vida, dada la sinergia existente del abordaje multicomponente; y se debe considerar, entre otros factores, el fenotipo de conducta alimentaria, para realizar intervenciones de mayor precisión que optimicen los resultados en la pérdida de peso.