INTRODUCCIÓN
Las enfermedades crónicas no transmisibles (ECNT) representan la principal causa de morbimortalidad mundial y en Argentina1. Las consecuencias humanas, sociales y económicas afectan a todos los países, aunque el 75% de las muertes por ECNT ocurren en los de medianos y bajos recursos2.
La Organización Mundial de la Salud (OMS) estima que el cáncer será la principal causa de muerte y la barrera más importante para aumentar la esperanza de vida en todos los países del mundo en el siglo XXI3.
Según las últimas estimaciones para Argentina de la Agencia Internacional de Investigación sobre el Cáncer (IARC, por sus siglas en inglés), en 2018 el cáncer de mama (CM) fue el tumor maligno más frecuente con más de 21 500 casos, lo que representa aproximadamente un tercio de los cánceres femeninos. Para el cáncer colorrectal (CCR), en ambos sexos se estimaron aproximadamente 15 700 casos nuevos, cifra que lo posiciona en segundo lugar en incidencia respecto a las demás neoplasias3.
A nivel nacional, el CM es la principal causa de muerte por cáncer entre las mujeres con aproximadamente 5900 fallecidas por año (20% del total de muertes por tumores malignos en mujeres), y el CCR es responsable de aproximadamente 7600 muertes por año, lo que representa en Argentina el 12% del total de muertes por tumores malignos en ambos sexos4,5.
La mayoría de los cánceres son esporádicos, es decir, se desarrollan en individuos sin antecedentes personales ni hereditarios demostrados de la enfermedad. Sin embargo, la presencia de antecedentes familiares (AF) de CCR6 o CM7 supone un riesgo mayor y variable, según grado de parentesco y la edad del familiar al momento de ser diagnosticado.
Alrededor del 75% de los CCR son esporádicos, mientras que un 25% corresponden a personas con riesgo adicional, por ejemplo: antecedente personal de adenoma, enfermedad inflamatoria intestinal, AF de CCR o síndromes hereditarios de CCR8. Estos últimos representan aproximadamente un 5% de los casos de CCR (por ejemplo, síndrome de Lynch)9.
En las personas con CM existe un 20-30% de probabilidad de tener al menos un familiar con la enfermedad. Sin embargo, sólo el 5-10% corresponden a CM hereditarios, asociados a mutaciones en genes específicos, como BRCA1 y BRCA2, TP53 y PTEN10,11.
Los programas nacionales para CM12 y CCR8 del Instituto Nacional del Cáncer (INC) incluyen en sus recomendaciones la evaluación de AF para estos tumores, con el fin de establecer grupos con riesgo aumentado, susceptibles de pautas de tamizaje y vigilancia particulares. Sin embargo, existe escasa información respecto a la prevalencia de AF de cáncer en el país.
El estudio CESCAS I (de detección y seguimiento de factores de riesgo de enfermedad cardiovascular en el Cono Sur de Latinoamérica) constituye un estudio prospectivo de cohorte poblacional. Se inició en 2011 con el objetivo de investigar la prevalencia y distribución de los factores de riesgo, así como su asociación con la incidencia de enfermedades crónicas en Argentina, Chile y Uruguay13. En Argentina, el estudio ha reclutado a 3990 participantes en las ciudades de Bariloche y Marcos Paz.
El presente trabajo tuvo como objetivo describir la prevalencia de AF de CM y CCR, y estimar la incidencia de estos tumores en adultos de 35 a 74 años de las dos ciudades mencionadas.
MÉTODOS
Se realizó un estudio de base poblacional observacional, con un componente transversal y otro prospectivo. Como parte del seguimiento de la cohorte CESCAS I, en las ciudades de Marcos Paz y Bariloche se recolectó información individual sobre AF de CM y CCR, y se investigaron los casos de CM y CCR utilizando documentación médica respaldatoria.
En la fase basal de la cohorte, que se prolongó desde comienzos de 2011 hasta fines de 2012, se recolectaron datos respecto a factores de riesgo conductuales, metabólicos y socioeconómicos con instrumentos ampliamente validados para estudios de esta naturaleza. Los detalles sobre la metodología del estudio e instrumentos utilizados han sido publicados previamente13,14.
Durante 2016 y 2017, encuestadores entrenados y certificados realizaron una entrevista presencial a cada participante para relevar los AF de CM y CCR y para identificar los eventos neoplásicos pre-valentes e incidentes en la cohorte. Posteriormente, se investigó cada caso utilizando documentación médica respaldatoria para confirmar el evento. Todos los diagnósticos fueron evaluados por un médico oncólogo según protocolos estandarizados.
La población de estudio fueron adultos de entre 35 y 74 años de ambos sexos, residentes en las ciudades de Marcos Paz y Bariloche. La muestra final se obtuvo por muestreo aleatorio polietápico estratificado por sexo, categorías de edad y nivel socioeconómico. Se incluyó a todos los individuos no institucionalizados que aceptaron participar, contestaron la encuesta basal y asistieron a la visita clínica inicial. La etapa basal del estudio contó con un tamaño muestral total de 1991 participantes en Marcos Paz y 1999 en Bariloche.
El muestreo poblacional aleatorio y estratificado minimizó los posibles sesgos de selección. La investigación de eventos con documentación médica respaldatoria permitió mejorar la clasificación de los casos de cáncer respecto a la esperada únicamente por autorreporte del paciente, minimizando los sesgos de información. Además, se elaboró un manual de definiciones operacionales de cada evento para homogeneizar los criterios diagnósticos.
Para recolectar información referente a los eventos de cáncer de la cohorte, se utilizaron instrumentos específicos tomando como referencia los del estudio de cohorte internacional PURE (Prospective Urban and Rural Epidemiological Study)15. Para completar los formularios se utilizaron documentos fuente pertinentes, que respaldaran y permitieran confirmar la información del evento (epicrisis de alta, biopsias, informe de estudios por imágenes, protocolos quirúrgicos, historia clínica, prescripciones médicas, solicitudes de interconsulta, etc.). Para tal fin, se realizó la capacitación de recolectores de datos en los sitios del estudio. En todos los casos, se procuró obtener los documentos fuente que aportaran el mayor grado de certeza a la decisión de adjudicación. También se realizó la investigación de los pacientes fallecidos para identificar los eventos neoplásicos correspondientes, mediante documentos fuente o por autopsia verbal a los familiares16,17.
Al momento de definir la enfermedad, la decisión final de adjudicación fue realizada por un médico oncólogo para determinar si el evento cáncer podía ser confirmado o no y establecer con precisión la fecha de diagnóstico y sitio anatómico para los eventos prevalentes e incidentes. En el caso de tumores recurrentes, recidivas o diagnóstico de otro tumor posterior a un cáncer previo, se consideró el sitio anatómico y la fecha del primer diagnóstico de cáncer.
Los tumores fueron codificados según sitio anatómico mediante la Clasificación Internacional de Enfermedades (CIE-10). Para el CM se utilizaron los códigos C50 y D05 (sólo en caso de cáncer no fatal) y para el CCR, C18 a C20.
La descripción general de las variables cualitativas se realizó mediante proporciones. Las variables cuantitativas se expresaron como el valor de la media y su desviación estándar o mediana y rango según la distribución de la variable.
Para el cálculo de incidencia acumulada se consideraron eventos incidentes a los que poseían fecha de diagnóstico (verificada con documentación respaldatoria) posterior a la fecha de primer contacto con el participante al inicio del estudio. No se consideró como población en riesgo del evento (cáncer) a los participantes que habían reportado antecedente en la etapa basal de la cohorte y a los que no contestaron la encuesta actual (ya que en ellos se desconoce si han tenido o no algún tumor).
Para determinar la prevalencia de AF y la incidencia de cáncer, se consideró el efecto diseño correspondiente a la unidad de primera etapa de muestreo y se aplicaron las respectivas ponderaciones a partir de la relación entre el número de individuos incluidos en el estudio y los datos de cada localidad del Censo Nacional de Población y Viviendas 2010, a fin de representar a la población general de 35 a 74 años de los sitios de estudio.
Se utilizó el software estadístico STATA® 14.2 (College Station, Texas, Estados Unidos).
En lo que respecta a los aspectos éticos, el estudio se llevó a cabo siguiendo estrictamente las guías de protección de los derechos para los voluntarios humanos y las consideraciones de la Declaración de Helsinki. Se respetaron todos los aspectos de la Guía para Investigaciones en Salud Humana (GISH) de la Comisión Nacional Salud Investiga. El estudio cumple, además, con la Ley 25326 de Protección de los Datos Personales.
El protocolo y el consentimiento informado del estudio han sido revisados y aprobados por el Comité de ética de protocolos de investigación del Hospital Italiano de Buenos Aires y el Comité de Evaluación de Proyectos de Investigación del Hospital Zonal de Bariloche Dr. Ramón Carrillo. En la visita al hogar, el consentimiento informado fue explicado de forma adecuada a la cultura y capacidad de comprensión del participante y luego fue firmado por todas las personas que aceptaron participar. La información que se incluyó en la base de datos no posee identificación personal.
RESULTADOS
Del número basal de participantes en Argentina (n=3990), se contactó y entrevistó durante el período 2016-2017 a 3245 participantes (81,3%) en Bariloche y Marcos Paz, con una mediana de seguimiento de 4,92 años (rango: 3,48-6,59). En 640 individuos (16,0%) se pudo relevar el estado vital, pero no fue posible recoger datos sobre AF de cáncer, por lo que ellos fueron excluidos del presente análisis. Además, 69 participantes (9,3%) fallecieron durante el período de seguimiento, 19 (2,6%) decidieron no responder, y no fue posible contactar a 18 individuos (2,4%).
El 61,2% de la muestra estuvo conformada por mujeres, y la edad media en este grupo fue de 53,6 años (desvío estándar [DE]=10,5). La media de edad en hombres fue de 54,5 años (DE=10,6). En la Tabla 1 se pueden observar las características basales generales de los participantes incluidos en el presente análisis.
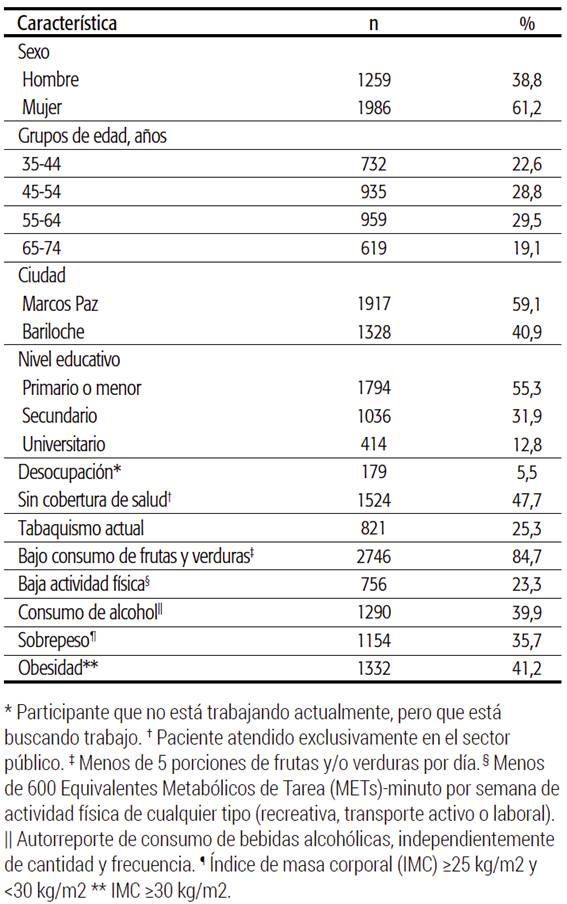
TABLA 1 Características basales generales de la población en estudio, adultos de 35 a 74 años de Marcos Paz y Bariloche, 2011
De los participantes encuestados, 229 adultos de ambos sexos consignaron que tenían algún familiar con diagnóstico de CCR y 274 mujeres presentaron AF de CM. En la Tabla 2 se puede observar la prevalencia declarada de AF de CCR y CM, según grado de parentesco y edad al diagnóstico del familiar afectado.
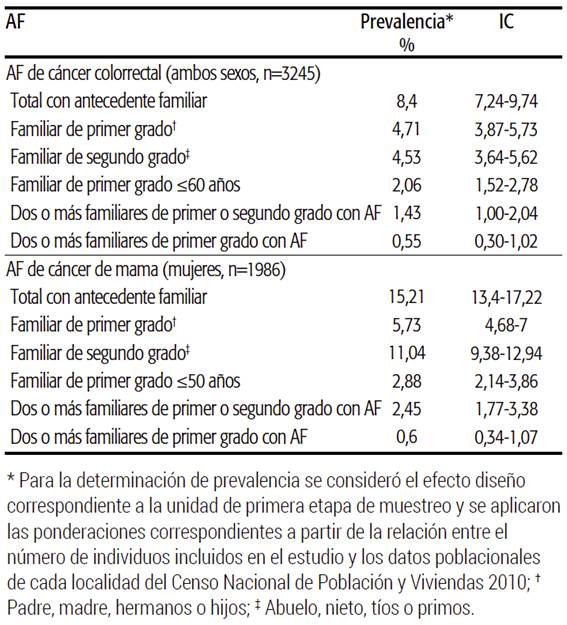
TABLA 2 Antecedentes familiares (AF) de cáncer colorrectal o de mama en adultos de 35 a 74 años, Marcos Paz y Bariloche, 2016-2017
Al inicio de la cohorte, 135 participantes manifestaron que habían tenido cáncer o presentaban la enfermedad al momento de la entrevista (29 casos de CM y 7 de CCR). En la última ronda de seguimiento, 99 participantes reportaron que se les había diagnosticado cáncer, de los cuales fueron confirmados 7 casos de mujeres con CM y 5 adultos con CCR.
Sobre la base de los casos prevalentes e incidentes donde se logró identificar la fecha de diagnóstico mediante documentación médica respaldatoria, la edad media al diagnóstico de las pacientes con CM fue de 59,5 años (DE=7,7; n=18), y para el CCR fue de 63,7 años (DE=6,2; n=6).
De los participantes que completaron el seguimiento, 1961 mujeres y 1256 hombres se encontraban libres del evento al inicio de la cohorte, y los casos de cáncer nuevos diagnosticados en esta población permitieron calcular la incidencia acumulada anual para el período 2011-2017 en adultos de 35 a 74 años de las dos ciudades estudiadas. Para el CM, la incidencia fue de 55,2/100 000 mujeres por año (IC95%: 22,8-133,7) y para el CCR fue de 38,5/100 000 adultos de ambos sexos por año (IC95%: 15,3-96,8).
DISCUSIÓN
Los resultados de este estudio contribuyen a conocer la situación sanitaria del CM y del CCR en Argentina, aportando información que es valiosa debido a la escasez de datos sobre la prevalencia de AF de estos tumores en el país.
Si bien es posible actuar sobre los factores de riesgo modifi-cables para reducir la carga de enfermedad por estos tumores, se trata de afecciones heterogéneas; tanto el CM18,19 como el CCR20,21 incluyen numerosos subtipos de tumores con diferentes mecanismos causales y fisiopatológicos, que no son fácilmente modificables con cambios en el estilo de vida. El tamizaje y la detección temprana se constituyen entonces en la estrategia central para disminuir la carga de enfermedad y mortalidad por estos tumores9,12.
La mayoría de los casos de CM y CCR son esporádicos, es decir, suceden en individuos sin historia familiar de la enfermedad. Sin embargo, la identificación de los pacientes con AF constituye un estándar de cuidado de la práctica clínica habitual y es importante para poder adecuar las estrategias preventivas correspondientes11,22.
Los resultados indican que casi 1 de cada 10 adultos de 35 a 74 años presentan al menos un familiar con CCR, que en aproximadamente la mitad de los casos es de primer grado (padre, madre, hermano o hijo). Por otro lado, el 15% de las mujeres tienen AF de CM (en un tercio de los casos en un familiar de primer grado; en la mayoría, de segundo grado).
El grado de parentesco es relevante para determinar la categoría de riesgo del individuo. Según una revisión sistemática y metaanálisis de 74 estudios, las personas con antecedentes de CM en un familiar de primer grado tienen el doble de riesgo de desarrollar CM (Riesgo relativo (RR): 2,1; IC95%: 2,0-2,2), con un incremento adicional si al familiar afectado se lo diagnostica antes de los 50 años (RR: 2,3; IC95%: 2,2-2,5)23. Además, de acuerdo con un reciente estudio de cohorte británico que incluyó a 113 000 mujeres, la presencia de dos o más familiares con CM se asocia con un aumento de riesgo de 2,5 veces (IC95%: 1,83-3,47)7.
En cuanto al CCR, en una revisión sistemática y metaanálisis se identificaron 47 estudios a partir de los cuales se estimó que el riesgo relativo de desarrollar CCR en personas con al menos un familiar de primer grado afectado es de 2,24 (IC95%: 2,062,43), que se eleva a 3,97 (IC 95%: 2,60-6,06) con al menos dos familiares afectados6.
Las causas del aumento de riesgo observado en pacientes con AF son multifactoriales; influyen factores endógenos (envejecimiento, factores de crecimiento, susceptibilidad genética) y extrínsecos (carcinógenos, virus oncogénicos, factores del estilo de vida)24. En parte, se debe a la agrupación de factores del estilo de vida entre miembros de la familia y al efecto acumulativo de polimorfismos genéticos relativamente comunes que aumentan el riesgo de enfermedad, en oposición a los síndromes hereditarios que influyen más fuertemente en el riesgo25,26. Tanto en el CM como en el CCR, los síndromes hereditarios asociados con mutaciones genéticas específicas representan aproximadamente el 5% de todos los casos10,27.
Las guías del INC y el Consenso Inter-Sociedades convocado por la Academia Nacional de Medicina establecen que los individuos con AF de CCR en un familiar de primer grado menor de 60 años o en dos familiares de primer grado, independientemente de la edad, constituyen un grupo de riesgo moderado para CCR y son susceptibles de recomendaciones de pesquisa y vigilancia especiales respecto a la recomendación poblacional para grupos con riesgo promedio8,28. Para el CM, entre otras pautas caracterizadas en la Guía Nacional, el diagnóstico de este tumor en un familiar menor de 50 años o la presencia de al menos dos casos en familiares cercanos (ya sea de primero o segundo grado) determinan la indicación de evaluación especial para asesoramiento genético oncológico11.
Los resultados del presente estudio señalan que la correcta evaluación de los AF del paciente es relevante para definir el impacto que se puede lograr en términos de prevención primaria y secundaria de estos tipos de cáncer.
Más allá de los AF, el presente estudio aporta datos de incidencia de CM y CCR en población general de 35 a 74 años de dos ciudades de Argentina utilizando fuentes primarias y contribuye así a investigar la carga de enfermedad por estos tumores en el país. Las estimaciones reportadas pueden diferir de las de modelos ampliamente difundidos como el Global Burden of Disease Study 29 o las recientes del Global Cancer Observatory (GLOBOCAN) para 20183. Sin embargo, no es apropiado realizar comparaciones directas. Las discrepancias podrían deberse a la distinta carga de enfermedad de las ciudades estudiadas respecto a los promedios a nivel nacional o a la distinta metodología empleada.
Los datos de incidencia de cáncer en Argentina provienen principalmente de los registros de base poblacional, y se puede observar una amplia variabilidad entre las tasas de las distintas ciudades incluidas en ellos30-32. Aunque estas diferencias pueden ser de naturaleza metodológica, cabe también atribuirlas a determinantes locales. En tal sentido, sobre la base del análisis del Registro de Cáncer de Base Poblacional de Córdoba realizado por Díaz, es interesante notar que a nivel geoespacial hay diferencias significativas en la incidencia de cáncer entre los departamentos provinciales31.
Si bien las tasas del presente estudio no permiten realizar comparaciones directas por los distintos grupos de edad representados, es importante enfatizar que existen variaciones en la carga de enfermedad según la ciudad del país. Esto amerita incrementar la cobertura territorial de la vigilancia epidemiológica del cáncer para identificar patrones geográficos y avanzar en el conocimiento de sus determinantes locales33.
La edad al diagnóstico reportada aquí es similar a la encontrada en otros estudios de Argentina. En los pacientes con CCR, la edad promedio es de 63,7 años, similar a la media de 65 consignada en un estudio retrospectivo de 99 casos en el Hospital Juan A. Fernández34. La media de edad al diagnóstico de CM es de 59,5 años, muy similar a la media de 59,9 hallada en un estudio transversal de 1544 casos, que incluyó centros públicos y privados del país35.
Una fortaleza del presente estudio reside en su adecuado diseño y tamaño muestral para la estimación de prevalencias poblacionales. Resulta elevada la tasa de seguimiento obtenida, y sin evidencia de pérdida no aleatoria de participantes36. Dada la naturaleza aleatoria del muestreo llevado a cabo, los AF reportados pueden ser considerados representativos de la población general de las ciudades estudiadas. Asimismo, la adjudicación de casos con documentación médica respaldatoria garantiza una mayor especificidad para determinar el diagnóstico del evento.
La principal limitación está relacionada con el tamaño muestral insuficiente para realizar estimaciones de incidencia de cáncer con alta precisión. Esto explica los amplios intervalos de confianza para los casos puntuales. Dado que se trata de población general, se requeriría un número muy elevado de participantes para estimar la incidencia de tumores con un nivel de precisión adecuado. Si bien el grupo etario considerado es el de mayor incidencia de CCR y CM, esta se mantiene elevada luego de los 75 años y no es posible capturar dichos casos en esta cohorte.
Tampoco se pueden ajustar las tasas por estructura poblacional, lo que limita la comparación con datos de otros estudios epidemiológicos. Existe la posibilidad de que algunos participantes desconozcan el diagnóstico de cáncer en sus familiares, lo que llevaría a subestimar la prevalencia de AF. También puede darse la situación inversa: que se hayan reportado diagnósticos que no correspondían realmente a casos de cáncer.
Para concluir, además de garantizar el acceso universal a los programas de tamizaje poblacional, se debe tener en cuenta la importancia de indagar sobre los AF de cáncer para identificar pacientes con riesgo aumentado, que requieren algoritmos particulares de detección temprana y vigilancia.
RELEVANCIA PARA POLÍTICAS E INTERVENCIONES SANITARIAS
El conocimiento de las prevalencias de factores de riesgo familiares para CM y CCR permite cuantificar grupos poblacionales susceptibles de pautas especiales de detección temprana y vigilancia, a fin de planificar mejor las políticas sanitarias.
RELEVANCIA PARA LA FORMACIÓN DE RECURSOS HUMANOS EN SALUD
La identificación y correcta caracterización de personas con riesgo incrementado de cáncer por presencia de AF es un estándar de cuidado, que debe ofrecerse y estar disponible como un componente de la práctica clínica habitual. La mejora en términos de reducción de la incidencia y mortalidad por estos tumores se inicia con una correcta evaluación personal y familiar del paciente.
RELEVANCIA PARA LA INVESTIGACIÓN EN SALUD
Ante un escenario con escasos estudios de población general que recolectan datos respecto a la incidencia de cáncer en el país, el presente proyecto contribuye a generar evidencia sanitaria a partir de estimaciones basadas en fuentes primarias. A medida que se incremente el tiempo de seguimiento de los participantes de la cohorte CESCAS, aumentará el poder estadístico y la capacidad del estudio para responder preguntas de investigación que contribuyan al conocimiento de los determinantes del cáncer.














