Introducción
La mastitis es una reacción inflamatoria de la glándula mamaria frecuente en el ganado lechero que daña el tejido secretor de leche. Cuando la ubre se lesiona ocurre una inflamación con acumulación de glóbulos blancos que, junto a células epiteliales del tejido productor de leche, constituyen las células somáticas (CCS).
Por otra parte, la mastitis subclínica se caracteriza por la presencia de microorganismos y un conteo elevado de células somáticas en la leche, pudiendo no tener tratamiento (1) y sin alteraciones evidentes en la ubre (2). Pero sí ocurren cambios en la composición de la leche a causa de las bacterias y componentes inflamatorios (3) .
El número de células somáticas puede ser usado como un índice para evaluar mastitis ya que existe una alta correlación entre un número elevado de células somáticas y presencia de mastitis (4–6) . Además, junto a los recuentos bacterianos en tanques a granel, los residuos deantibióticos y los valores nutricionales son mediciones de la calidad de la leche. (7)
Los cambios que pueden ocurrir en la composición de la leche son: disminución de la cantidad y la calidad de caseína sintetizada, disminución de la grasa butirosa, disminución de la lactosa, aumento de la concentración de sodio, aumento de los cloruros, aumento de las proteínas del suero sanguíneo, aumento de enzimas y aumento de las células somáticas. Por lo tanto, si la calidad de la leche no es buena puede conducir a una disminución en los rindes económicos (8) ya que se afecta el rendimiento del queso y la vida útil de todos los productos lácteos (9).
Existen suficientes evidencias que sostienen que las variaciones individuales en la respuesta inmune, ante la exposición a un agente patógeno, son consecuencia de factores genéticos y ambientales ( 10). Consecuentemente, existe un considerable interés en definir marcadores genéticos e inmunológicos que puedan ser utilizados para seleccionar animales a favor de la resistencia a mastitis, debido a que es una de las enfermedades más frecuentes en el ganado bovino lechero y la que ocasiona las mayores pérdidas económicas (11) .
La resistencia genética es un rasgo multigénico, es decir, determinado por muchos genes, entre los cuales se encuentran los del Complejo Principal de Histocompatibilidad (MHC). Para desencadenar una respuesta inmunológica apropiada en los mamíferos, los antígenos extraños, por ejemplo bacterias, que ingresan en los animales deben ser fragmentados y presentados a sus respectivos receptores o moléculas presentadoras de antígeno.
Los loci del MHC constituyen los principales genes candidatos para el estudio de asociación entre marcadores genéticos y resistencia/susceptibilidad a enfermedades infecciosas. Cada uno de sus genes a su vez tiene muchos alelos por lo que es también polimórfico. Este polimorfismo tiene un profundo efecto en el reconocimiento de los antígenos por las células T y la combinación de poligenia y polimorfismo extiende ampliamente el rango de péptidos que pueden ser presentados a las células T por un individuo (12).
En Bovinos el MHC se denomina Bovine Leukocyte Antigen (BoLA) y ha sido mapeado en el autosoma bovino 23 (BTA 23) dentro de una extensión de 4.000 Kb que contiene más de 154 genes estrechamente ligados (13).
El BoLA está conformado por genes de clase I, II y III y los polimorfismos de las moléculas de clase II han sido asociados en vacas lecheras con resistencia/susceptibilidad a enfermedades infecciosas tales como mastitis clínica, leucosis y neosporosis entre otras (14–18)
Las moléculas de clase II se subdividen en IIa y IIb. Los genes y los produc tos de clase IIa son los más estudiados porque presentan altos niveles de polimorfismo. Esta región comprende los grupos de genes DR y DQ. Se han identificado un total de catorce genes: la subregión DR es la más conservada a través de las especies y posee un locus DRA, tres loci DRB, cinco loci DQA (DQA1, DQA2, DQA3, DQA4, DQA5) y 5 loci DQB (19).
Se han reportado hasta el momento un total de 65 alelos DQA y 87 alelos DQB (20).
El BoLA-DQ es menos polimórfico que el BoLA-DR pero no por eso menos importante ya que se ha demostrado que su función es tan efectiva como la de las moléculas DR (19,21). Por esta razón, se considera que las duplicaciones de los genes BoLA-DQA y DQB contribuyen a la diversidad de moléculas presentadoras de antígenos en el ganado bovino.
Algunos individuos llevan una sola copia de DQA y DQB, mientras otros tienen haplotipos duplicados. Cerca de la mitad de los haplotipos de clase II presentan duplicación de los genes DQ (22) . Cuando los genes DQ se encuentran duplicados ambos conjuntos de genes DQ pueden expresarse (23,24).
Sin embargo, es poco el avance de las investigaciones para conocer si los loci específicos del BoLA de clase II están individualmente asociados con bajos y altos CCS como medida de resistencia/susceptibilidad, o si otros genes ligados son responsables de dicha asociación. Además, el BoLA parece tener influencia sobre otros rasgos tales como producción de leche y reproducción (11,25) y a variaciones en la respuesta inmune individual a antígenos.
En bovinos, diferentes trabajos han reportado asociaciones entre los alelos de clase II del BoLA y la resistencia/susceptibilidad a enfermedades infecciosas, tales como el linfoma inducido por el virus de la leucosis bovina (bovine leukemia virus, BLV) (17,18,26–30) y mastitis (4,6,11,14,16,26,31–34, 35).
Por lo tanto el objetivo general del presente estudio consistió en analizar los polimorfismos del gen BoLA-DQA1 y detectar su asociación con la resistencia / susceptibilidad a mastitis medida a través del conteo de células somáticas en leche.
Materiales y métodos
El estudio experimental se llevó a cabo en animales de la raza Holstein de la Provincia de La Pampa.
Se extrajeron muestras de 5 ml de sangre entera a 60 animales y las mismas se conservaron con anticoagulante a -20 ºC hasta su utilización. Estos individuos se seleccionarion porque presentaban registros de al menos dos lactancias.
Por otra parte, se registraron mensualmente los conteos de células somáticas (CCS) y registros de producción tales como litros de leche, porcentaje de grasa en leche y porcentaje de proteínas a lo largo de toda la lactancia durante cuatro años. El promedio de controles lecheros de los individuos seleccionados fue de 35 registros a lo largo de los 4 años de estudio.
DISEÑO EXPERIMENTAL
Los 60 animales se categorizaron en dos grupos: grupo caso y grupo control. El primero representado por individuos con conteos de células somáticas mayor o igual a 250.000 por mililitro leche (CCS
≥250.000 cel/ml). Este grupo incluyó animales que tuvieron mastitis al menos dos veces. El grupo control estaba conformado por individuos con registro de células somáticas menor a 250.000 células por mililitro de leche (CCS <250.000 cel/ml). Se tomó como referencia el límite de 250.000 células por mililitro de leche ya que es un indicador estándar de individuos con mastitis cuando lo superan ó de individuos fisiológicamente normales con menos de 250.000 cel/ml (36). El rodeo analizado en el presente estudio pertenecía a un establecimiento lechero que no poseía registros genealógicos pero sí registros de la procedencia de los animales. Esto último permitió verificar que el rodeo fue armado con animales de distintos tambos, por lo tanto, los animales estudiados no compartían madre o padre.
TIPIFICACIÓN DEL EXÓN 2 DEL GEN BOLA-DQA1 MEDIANTE PCR-RFLP (REACCIÓN EN CADENA DE LA POLIMERASA- POLIMORFISMO DE LONGITUD DE LOS FRAGMENTOS DE RESTRICCIÓN)
El ADN genómico se extrajo a partir de las muestras de sangre entera mediante el kit DNA Wizard (Promega, USA), según las indicaciones del proveedor. El gen BoLA-DQA1 se genotipo mediante PCR anidado (37). Para la primera ronda de amplificación del exón 2 se utilizaron los oligonucleótidos DQA1-intL2 CACAAATGAAGCCCACAATG y DQA1- 677R CCCTAGGGAAAAGGGAGTGA. Las reacciones se realizaron utili- zando 4 μl de ADN molde, 15,35 µl de agua, 2,5 µl de buffer, 2 µl de d NTPs, 1 µl de cebadores y 0,15 µl de Taq en un volumen final de 25 μl. El perfil térmico para la primera ronda incluyó una etapa de desnaturalización inicial a 94ºC durante 2 minutos, 15 ciclos de 94ºC durante 20 segundos, 60ºC durante 20 segundos, 72ºC durante 40 segundos y para terminar una extensión final de 1 ciclo 72ªC durante 4 minutos.
Con esta reacción se obtuvieron fragmentos de 355 pb que incluyen el exón 2 y sectores flanqueantes de los intrones 1 y 2 del gen BoLA- DQA1. La correcta amplificación se confirmó en un gel de agarosa al 1%.
Los productos de amplificación se digirieron con las enzimas Hae III, Mbo I, Hha I. Los fragmentos de restricción se resolvieron en geles de poliacrilamida 8% que se utilizaron para separar las bandas de los productos de la digestión enzimática (PCR-RFLP).
Luego para la visualización de las mismas los geles se tiñeron con nitrato de plata.
Los sitios de restricción de distintas enzimas para cada alelo se de- terminaron utilizando el software Webcutter2.0 (38) . Para cumplir dicho objetivo se bajaron las secuencias correspondientes a los alelos del BoLA-DQA1 de la página IPD-MHC Database (20,39).
La clasificación de los alelos se realizó teniendo en cuenta las com binaciones de los patrones de restricción obtenidos en forma independiente para las enzimas antes mencionadas.
La lectura de los alelos se basó en la nomenclatura del 5th BoLA workshop (BoLA Nomenclature, International, Society for Animal Genetics) (40).
TIPIFICACIÓN DEL EXÓN 2 DEL GEN BOLA-DQA1 POR PCR-SBT (REACCIÓN EN CADENA DE LA POLIMERASA-TIPIFICACIÓN BASADA EN SECUENCIACIÓN)
Para realizar esta técnica se emplearon los mismos cebadores que los utilizados para la tipificación por PCR-RFLP y las condiciones para las dos rondas de amplificación también fueron las mismas. Los amplificados se corrieron en geles de acrilamida al 6% 1X TBE y luego se tiñeron con Bromuro de Etidio
La secuenciación de los productos de PCR se llevó a cabo mediante un secuenciador de tecnología capilar MEGABACE 1000 (GE Healthcare, USA) utilizando el kit DYEnamic ET Terminator Kit (GE Healthcare). Las secuencias crudas fueron edita- das usando el programa (Sequence Analyzer (GE Healthcare) (41).
ANÁLISIS ESTADÍSTICO
La estimación de las frecuencias génicas y el número de alelos se realizó por conteo directo. La heterocigosidad observada (ho) y esperada (he) se calcularon de acuerdo a Nei (42) utilizando el programa ARLEQUIN 3.5 (43). Las desviaciones del Equilibrio de Hardy–Weinberg (EHW) se estimaron a través del índice FIS (44), utilizando el test exacto y el test de probabilidad incluidos en el programa GENEPOP 4.0 (45) . La significancia del estadístico FIS se calculó mediante el método de Markov Chain (46).
ANÁLISIS DE SECUENCIAS
Las secuencias de ADN se alinearon con el programa CLUSTAL-W 1.8 multiple alignment software (47) . La asignación de alelos se realizó mediante la utilización del programa HAPLOFINDER (48).
ESTUDIOS DE ASOCIACIÓN ENTRE EL CCS Y LA FRECUENCIA GÉNICA DEL BOLA-DQA1
Se realizaron mediante el test exacto de Fisher, el de Odds Ratio (OR) de Woolf-Haldane y los intervalos de confianza (CI). Estos cálculos se llevaron a cabo mediante el paquete de R Epitools (49).
Resultados
CARACTERIZACIÓN DE LOS POLIMORFISMOS PRESENTES DEL GEN BOLA-DQA1
Se genotipó el exón 2 del BoLA-DQA1 por PCR-RFLP en 60 animales y de esta manera se identificaron un total de 16 alelos. En la tabla 1 se pueden observar los resultados obtenidos de heterocigosidad esperada y observada, como así también las frecuencias génicas de los dos grupos estudiados: el grupo caso (CCS ≥250.000 cel/ml) y el grupo control (CCS <250.000 cel/ml).
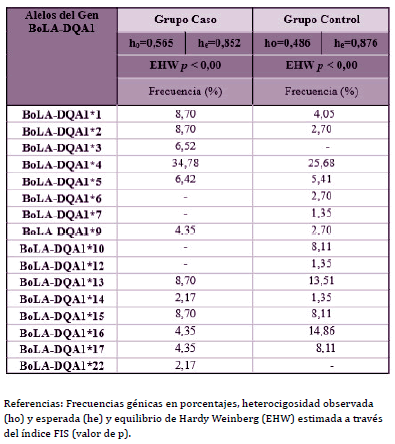
Tabla 1 Frecuencias génicas de los alelos definidos por PCR-RFLP para el gen BoLA-DQA1 en la población Holstein estudiada
Veintitrés de los animales analizados por PCR-RFLP fueron nuevamente tipificados mediante la técnica de PCR-SBT para confirmar los alelos detectados. Se encontraron un total de 8 alelos por medio de PCR-SBT y en todos los casos los resultados fueron coincidentes con los resultados obtenidos por PCR-RFLP. Estos alelos fueron: BoLA- DQA1*0204, *10011, *10012, *12012, *0102, *1203, *12021 y *0101.
ASOCIACIÓN DEL GEN BOLA-DQA1 CON EL NÚMERO DE CÉLULAS SOMÁTICAS
El test exacto de Fisher y el Odds Ratio (OR) de Woolf- Haldane también fueron utilizados para estudiar la asociación entre el CCS y los alelos del gen BoLA-DQA1 genotipados por PCR-RFLP (Tabla 2). Ninguno de los valores de OR calculados fueron significativos (p > 0,12).
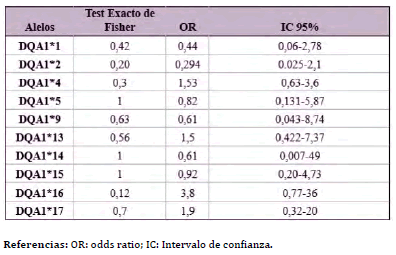
Tabla 2 Asociación de alelos del BoLA-DQA1, definidos por PCR-RFLP con el conteo de células somáticas (CCS) en la población Holstein estudiada.
También se estudió la asociación entre el CCS y los alelos del gen BoLA-DQA1 genotipados por PCR-SBT. Los valores de OR sólo se calcularon para aquellos alelos con frecuencias mayores o iguales al 15%, dado que el resto presentaron valores bajos de frecuencia génica.
Si bien el alelo BoLA-DQA1*0101, correspondiente al alelo BoLA- DQA1*16 tipificado por PCR-RFLP, fue el mayoritario en el grupo con bajo CCS, evidenció un valor de OR de 4 (p = 0,058), lo que indicaría una posible asociación entre dicho alelo y susceptibilidad a padecer la enfermedad (Tabla 3). Cabe destacar que el alelo del BoLA-DQA1*16 (PCR-RFLP) también mostró un valor de riesgo cercano a 4, aunque en este caso la probabilidad no fue significativa (p= 0,12) (Tabla 2).
En cuanto los alelos BoLA-DQA1*10012 y BoLA-DQA1*10011, que fueron los más frecuentes en el grupo con alto CCS con frecuencia génica del 25% presentaron valores de OR no significativos e inferiores a 1.
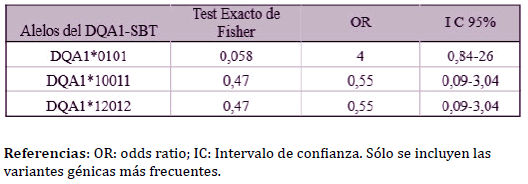
Tabla 3 Asociación de los alelos BoLA-DQA1, definidos por PCR-SBT, con con teo de células somáticas (CCS) en la población Holstein estudiada
Discusión
En el presente trabajo se caracterizaron los polimorfismos presen- tes en el exón 2 del gen BoLA-DQA1 en bovinos de raza Holstein de La Pampa, detectándose que ambos grupos analizados (caso y control) tenían como alelo más frecuente a la variante BoLA-DQA1*4 y a la menos frecuente al BoLA-DQA1*14 es decir se encuentran distribuídos de manera similar en ambos grupos del rodeo de raza Holstein analizado. Este resultado coincide con lo reportado por Miyasaka et al. (50) quienes analizaron rodeos de distintas razas bovinas de Japón.
En nuestros resultados se evidenció un aumento significativo de individuos homocigotas. El rodeo analizado no poseía registros genealógicos pero sí registros de la procedencia de los animales, esto permitió verificar que el rodeo fue armado con animales de distintos tambos. Pero no se descarta cierto grado de consanguinidad entre los animales del mismo tambo ocasionado por la propia dinámica de la cría, pudiendo existir estructuración poblacional.
Como los valores de ho dependen de las frecuencias génicas de origen de las muestras, se explicaría el aumento de individuos homocigotas. Takeshima et al(51) y Miyasaka et al. (50), propusieron que los individuos heterocigotos para el gen BoLA-DQA1 presentan ventajas contra enfermedades infecciosas provocadas por determinados patógenos, pero aún no se conoce claramente cuáles son los mecanismos de selección que favorecen a los genotipos heterocigotos. El aumento de la heterocigosidad se corresponde con el incremento de la resistencia a enfermedades infecciosas ya que favorece la diversidad de las células encargadas de presentar antígenos a los linfocitos T, generando de esta manera un diverso repertorio de éstas.
Así por ejemplo, estos autores reportaron que el genotipo BoLA-DQA1*0101/*0101 estaba asociado a susceptibilidad a mastitis causada por Streptococcus sp. y el genotipo BoLA- DQA1*10011/*10011 con susceptibilidad a mastitis provocada por Escherichia coli.
Una submuestra de animales a los que se tipificó el exón 2 del gen BoLA-DQA1 por PCR-RFLP, fueron también genotipados por PCR-SBT. El alelo BoLA-DQA1*0101 fue el más frecuente, en coincidencia con lo observado por Takeshima et al.(51) en una población Holstein de Japón, y por Misayaka et al.(50) en ganado Japonés Negro y Holstein. Kulaj et al. (52) encontraron resultados similares en una población de ganado Holstein Friesian (variedad negra y blanca) de Polonia. El alelo BoLA- DQA1*10012 fue el segundo alelo más abundante coincidiendo con lo reportado por Miyasaka et al. (50) en la raza Japonesa Negra. Takeshima et al. (51) encontraron que el alelo BoLA-DQA1*10012 se encontraba en una frecuencia moderada (alrededor del 10%) en la población de Holstein que analizaron. En tanto, Kulaj et al. (52) lo encontraron en una frecuencia del 2,82% en ganado Holstein de la población estudiada. Por otro lado, en el grupo con alto CCS analizado en el presente estudio los alelos BoLA-DQA1*10011 y *10012 (DQA1*4) fueron los más frecuentes.
El alelo BoLA-DQA1*12021 fue el más frecuente en el ganado Jersey (0,336), el alelo BoLA-DQA1*10012, fue el alelo más frecuente en el ganado negro japonés (0,332) y el alelo BoLA-DQA1*0204 lo fue en el Shorthorn japonés (0,23) según lo reportado por Takeshima et al. (51) . Se encontraron resultados similares en tres rebaños de ganado negro japonés, en los que el alelo BoLA-DQA1*10012 tenía una frecuencia de 0,32 a 0,42 (50) .
Se calcularon los OR para los alelos BoLA-DQA1 tipificados por PCR- RFLP pero ninguno evidenció una asociación significativa con resistencia/susceptibilidad a mastitis medida a través del CCS. En el caso de los alelos genotipados mediante PCR-SBT el alelo BoLA-DQA1*0101 presentó un valor de OR de 4 (p = 0,058), lo cual indicaría una tendencia a la asociación entre dicho alelo y la mastitis. Este resultado coincide con lo reportado por Takeshima et al. (51) quienes asocian esta variante con la susceptibilidad a mastitis causada por Streptococcus sp.
En el caso de los alelos BoLA-DQA1*10012 y *10011, los resultados obtenidos no evidenciaron valores significativos de OR. Por el contrario, Takeshima et al.(51) reportaron una asociación significativa entre el alelo BoLA-DQA1*10011 y mastitis provocada por Escherichia coli.
En recientes trabajos realizados por Takeshima et al. (53), compararon alelos del gen BoLA-DQA1 y BoLA-DRB3 para estudiar la carga proviral del virus de leucosis y encontraron una menor asociación en el marcador DQA1 que con el DRB3 en vacas Holstein de Japón (OR = 11,5 para el gen BoLA-DQA1; OR = 13,9 para BoLA-DRB3 y OR = 6,2 para los haplotipos de clase II del BoLA).
Conclusiones
De acuerdo a los resultados obtenidos y comparados con la bibliografía disponible, la distribución de las frecuencias génicas del locus BoLA-DQA1 difiere significativamente según la raza de ganado estudiada. En nuestro análisis, realizado en animales de la raza Holstein, el alelo BoLA-DQA1*0101, correspondiente al alelo BoLA-DQA1*16 tipificado por PCR-RFLP, evidenció una posible asociación entre dicho alelo y la susceptibilidad a padecer la mastitis.
Es importante destacar que diferentes patógenos están presentes en el medio ambiente de cada rodeo y el mismo alelo puede responder de manera diferente para cada uno de ellos. También pudieron estar comprometidos factores ambientales que involucran el manejo, el estado sanitario y la alimentación del rodeo en estudio.
Los estudios de asociación entre los genes del BoLA y mastitis basados en marcadores moleculares podrían constituir una efectiva herramienta para el control de enfermedades infecciosas, ya sea mediante su aplicación en los programas de selección genética o mediante el desarrollo de vacunas y, de esta forma, reducir los costos sanitarios que afectan a la producción lechera.
La resistencia/susceptibilidad en vacas con mastitis podría variar dependiendo de la combinación inter e intra alélica de los diferentes loci del BoLA.
En próximos estudios sería conveniente la genotipificación de otros genes candidatos para poder calcular con certeza la asociación entre las moléculas del BoLA con resistencia/susceptibilidad a enfermedades multifactoriales como la mastitis, mediante la aplicación de las nuevas técnicas, especialmente aquellas basadas en las tecnologías de NGS (Next Generation Sequencing), y así incluir el análisis simultáneo de los diferentes loci involucrados en la resistencia susceptibilidad a enfermedades infecciosas en vacas lecheras.














