Introducción
La sarcopenia se define como una combinación de baja fuerza y masa muscular con alteraciones en la función muscular1,2. El término se utilizó inicialmente para designar la pérdida de masa muscular y el rendimiento asociado con el envejecimiento. Ahora se sabe que las causas reconocidas de desarrollo de la sarcopenia también incluyen enfermedades crónicas (particularmente las inflamatorias), un estilo de vida físicamente inactivo, pérdida de movilidad y malnutrición. Si bien se publicaron estudios que describen la relación entre la sarcopenia y diversas enfermedades reumatológicas, la evaluación de la sarcopenia no es una práctica que se realice de manera rutinaria en la consulta ambulatoria. Su manejo requiere un enfoque multimodal que combine una nutrición adecuada con ingesta suficiente de proteínas de alto valor biológico, ejercicio físico y, de ser necesario, medicamentos antiinflamatorios.
En esta revisión narrativa hemos considerado: a) recomendaciones para el diagnóstico de la sarcopenia; b) herramientas útiles para la práctica clínica y la investigación; c) su relación con las enfermedades reumáticas.
Definición de sarcopenia
El término sarcopenia deriva del griego: “sarx” significa carne y “penia”, deficiencia. Evans y Campbell3,4 la describieron en 1993. Posteriormente, en 1997, Rosemberg publicó esta terminología definiendo el síndrome geriátrico5. En 2009, la European Union Geriatric Medicine Society (EUGMS) inició el European Working Group on Sarcopenia in Older People (EWGSOP), donde expertos de diferentes sociedades científicas desarrollaron el Consenso Europeo sobre la definición y el diagnóstico publicado en 20106. En 2018, el EWGSOP actualizó nuevamente los conceptos de ese Consenso luego de casi 10 años de investigaciones y, con la nueva evidencia, delinearon nuevos criterios y herramientas para definirla y caracterizarla. Esta actualización se enfoca en la importancia del diagnóstico precoz para aumentar las posibilidades de prevenir, demorar, tratar y eventualmente revertir la sarcopenia7.
Prevalencia
Varias revisiones de la literatura intentaron establecer la prevalencia de la sarcopenia, la mayoría en adultos mayores. Una revisión sistemática y meta-análisis publicada en 2017 reveló que una proporción sustancial de personas mayores tiene sarcopenia, incluso en poblaciones sanas. Sobre un total de 35 estudios y 58404 individuos, la prevalencia estimada entre 2009 y 2016 para adultos mayores sanos fue de 10% (IC 95%: 8-12%) en hombres y 10% (IC 95%: 8-13%) en mujeres8. Según los criterios utilizados y la metodología empleada para obtener la información de la fuerza y masa muscular, la prevalencia de sarcopenia reportada en personas mayores de 60 años va del 5 al 13%, mientras que en los mayores de 80 años los rangos van del 11 al 50%9.
Si bien la sarcopenia se ha asociado con el envejecimiento y el adulto mayor, hoy se conoce que el desarrollo comienza más tempranamente en la vida y que, como mencionó anteriormente, existen diversas causas que contribuyen a ello, como los procesos inflamatorios, más allá de la edad7. No obstante, no existen muchos estudios en la población menor de 60 años. Una publicación de 2020 buscó determinar la prevalencia de sarcopenia en la población mexicana mayor de 18 años utilizando la impedancia bioeléctrica (bioelectrical impedance analysis, BIA). En la muestra de 293 pacientes (74,5% mujeres) se encontró un 15,35% de sarcopenia en la población general. Por grupo etario, la prevalencia fue de 14,28% para los individuos de 18 a 39 años, 11,5% para el grupo de 40 a 59 años y de 22,53% para los mayores de 60 años10.
Categorías de sarcopenia
Existen categorías de clasificación de la sarcopenia descriptas básicamente para su aplicación en el ámbito clínico7. Se denomina sarcopenia primaria cuando se asocia a la edad (adultos mayores)11. La sarcopenia secundaria se atribuye a otro factor diferente a la edad (o sumado a ella), como puede ser una patología sistémica (especialmente donde hay presencia de procesos inflamatorios, incluyendo las enfermedades reumáticas), enfermedades oncológicas, falla orgánica (enfermedad renal, insuficiencia cardíaca, entre otras), inmovilidad, estilo de vida sedentario, incapacidad física y también por una inadecuada ingesta de energía y proteínas (que a su vez puede relacionarse con malabsorción, anorexia, acceso limitado a los alimentos, etc.).
En función del tiempo de evolución, se puede clasificar en aguda cuando se detecta en un lapso menor a 6 meses, generalmente asociada a injurias o enfermedades agudas, y crónica cuando es mayor a 6 meses. Esta última se observa principalmente en personas con enfermedades progresivas y crónicas, y aumenta el riesgo de mortalidad7.
En la práctica cotidiana los profesionales de la salud pueden asociar la sarcopenia a la delgadez, pero a pesar de esto puede presentarse en personas con sobrepeso y obesidad. La reducción de la masa magra corporal en un contexto de exceso de masa grasa o adiposidad se denomina obesidad sarcopénica7,12, que suele ser la más reportada en adultos mayores. Es de destacar que la adiposidad exacerba la sarcopenia, aumenta el infiltrado de grasa en el músculo, disminuye las funciones físicas e incrementa el riesgo de mortalidad7,12-15. En el Consenso publicado en 2022, la European Society for Parenteral and Enteral Nutrition (ESPEN) y la European Association for the Study of Obesity (EASO), en relación al diagnóstico y definición de la obesidad sarcopénica, proponen el uso de DEXA (dual-energy X-ray absorptiometry, absorciometría dual de energía de rayos X) y BIA para evaluar la composición corporal y el acceso al valor de la masa grasa16.
Diagnóstico
Una de las primeras diferencias en el actual Consenso Europeo sobre sarcopenia (EWGSOP) en referencia a la publicación de 2010, es que la nueva evidencia demostró que no es una entidad exclusivamente de la población adulta mayor, sino que comienza en etapas más tempranas de la vida7. De hecho, entre los 30 y 80 años se observa una reducción generalizada de la masa muscular de aproximadamente un 30%, lo cual resulta en una disminución cuantitativa y cualitativa de las fibras musculares17,18.
La segunda diferencia en el nuevo concepto de sarcopenia es que se la considera una enfermedad muscular caracterizada por baja fuerza muscular como determinante principal, por encima de la baja masa muscular, lo cual facilita la identificación del problema precozmente. Se define “sarcopenia probable” a la pérdida de fuerza muscular. Cuando se comprueba la pérdida de fuerza y masa muscular, la existencia de sarcopenia queda “confirmada”, y además si se altera el rendimiento físico se denomina “sarcopenia severa” (Figura 1).
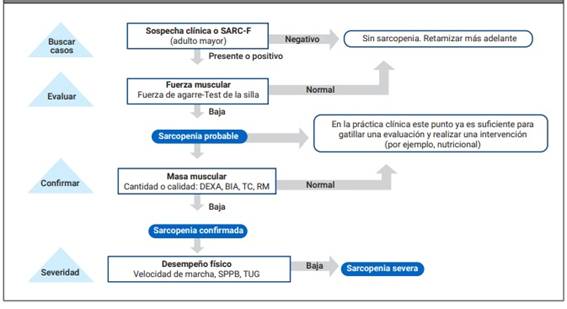
Figura 1: Algoritmo práctico para detección de sarcopenia, diagnóstico y severidad. SARC-F: cuestionario de tamizaje para detección de adultos mayores en riesgo de sarcopenia; DEXA: dual-energy X-ray absorptiometry (absorciometría dual de energía de rayos X); BIA: bioelectrical impedance analysis (impedancia bioeléctrica); TC: tomografía computada; RM: resonancia magnética; SPPB: short physical performance battery (batería corta de desempeño físico); TUG: timed up and go (test de la silla, levantarse de la silla sin apoyo y caminar).
En tercer lugar, la sarcopenia se asocia a baja cantidad de masa muscular y baja calidad, pero estos parámetros actualmente se orientan más a la investigación que a la práctica clínica porque ambos (cantidad de masa muscular y calidad) son complejos de medir en la cotidianeidad7.
Por último, la EWGSOP revisó los puntos de corte y los parámetros de medición de las variables de masa y fuerza muscular con el fin de proveer a los profesionales de la salud indicadores más precisos para la práctica clínica7. Esta nueva revisión significó no solo un cambio en las recomendaciones para el diagnóstico de la sarcopenia, sino también un llamado a la acción para todos los profesionales que traten personas con riesgo de sarcopenia dado que otorga herramientas fundamentales para promover la detección y el tratamiento precoz, así como para la investigación en el campo de la sarcopenia con el fin de prevenir o retrasar los resultados adversos para la salud de los pacientes.
Si bien hay diferentes herramientas y pruebas para realizar el diagnóstico de la sarcopenia, en la práctica cotidiana la búsqueda de casos debe comenzar cuando el paciente reporta síntomas o signos (sensación de debilidad, lentitud al caminar, desgaste muscular, patología que genere sospecha clínica de pérdida de masa muscular, etc.).
Para los adultos mayores se recomienda el cuestionario SARC-F para el tamizaje de pacientes que puedan tener signos de sarcopenia. Esta herramienta de screening ha sido evaluada en tres grandes estudios con diferentes grupos de población (afroamericanos, norteamericanos y chinos) y se considera válida para identificar adultos mayores en riesgo de sarcopenia7. En los pacientes en quienes el cuestionario resulta positivo para llegar al diagnóstico y estimar su severidad, se deben evaluar las siguientes variables: fuerza muscular, masa muscular y desempeño físico. En la Tabla 1 se resumen las metodologías y sus recomendaciones para determinar estos tres aspectos.
Tabla 1: Aplicabilidad de las herramientas existentes para abordar la sarcopenia.
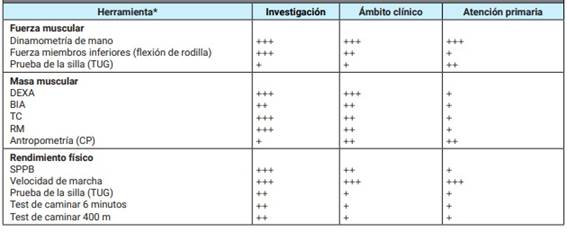
DEXA: dual-energy X-ray absorptiometry (absorciometría dual de energía de rayos X); BIA: bioelectrical impedance analysis (impedancia bioeléctrica); TC: tomografía computada; RM: resonancia magnética; CP: circunferencia de pantorrilla; SPPB: short physical performance battery (batería corta de desempeño físico); TUG: timed up and go (test de la silla, levantarse de la silla sin apoyo y caminar). +++ Herramienta más recomendada (1° elección). ++ Mejor herramienta alternativa (2° elección). + Herramienta menos recomendada (última opción). * La selección debe basarse en la disponibilidad de la herramienta, sus costos, tiempo requerido para la prueba, necesidad de personal entrenado y puntos de corte aplicables.
Fuerza muscular
La dinamometría de mano es un índice simple de medir. La baja fuerza de prensión de la mano es un potente predictor de pobres resultados en salud como incremento de la estancia hospitalaria, aumento de la disfuncionalidad física, baja calidad de vida asociada a la salud y muerte19,20. La fuerza de la mano se correlaciona moderadamente bien con la fuerza en otros compartimentos más complejos de evaluar, como las piernas7. Existen varios modelos de dinamómetros, pero los más utilizados porque han sido validados son los dinamómetros hidráulicos.
La prueba de la silla, también llamada timed up and go, puede utilizarse como indicador indirecto de la fuerza de las piernas (grupo muscular de cuádriceps); mide la cantidad de tiempo necesario para que un paciente se levante cinco veces desde una posición sentada sin usar sus brazos. Existe una variación de esta prueba que mide cuántas veces la persona puede levantarse de la silla sin usar los brazos en un intervalo de 30 segundos. Para realizar esta prueba se requiere fuerza y resistencia, por ese motivo se la considera óptima para evaluar la fuerza y también el desempeño7. Esta prueba se empleó ampliamente en varios estudios desarrollados en poblaciones con enfermedades reumáticas, en especial con artritis reumatoidea (AR). En este caso, su uso no se ha limitado solo al diagnóstico de la fuerza muscular, sino también para evaluar el progreso en la fuerza y el desempeño físico antes y después de la implementación de diversos tratamientos, como programas de ejercicios de resistencia, suplementación nutricional y rehabilitación en cuidados domiciliarios, entre otros21-24.
Masa muscular
La cantidad de masa muscular puede estimarse a través de varias técnicas. La cantidad de músculo se puede informar como masa musculoesquelética (MME), como masa musculoesquelética apendicular (MMEA) o como área de sección transversal del músculo de un grupo de músculos específico o localizaciones del cuerpo7. Para obtener los valores de estos indicadores de masa muscular existen diferentes metodologías. En el último Consenso Europeo de Sarcopenia7 se detallan: resonancia magnética (RM), tomografía computada (TC), DEXA, BIA y circunferencia de pantorrilla (CP).
Tanto la RM como la TC son consideradas el estándar de oro para la evaluación no invasiva de la cantidad y calidad de masa muscular, pero no son comúnmente utilizadas en la atención primaria debido a la dificultad en la portabilidad, la necesidad de personal altamente entrenado y capacitado, y los costos para el sistema de salud. Adicionalmente, los puntos de corte para la baja masa muscular no están completamente definidos para ambas metodologías7,13.
DEXA es la herramienta de elección para determinar la cantidad de masa muscular (masa magra corporal o MMEA), pero requiere que el equipamiento cuente con un software apropiado para realizar esta lectura. Es un método no invasivo, pero diferentes equipos de DEXA no dan los mismos resultados de manera consistente7. La masa muscular se correlaciona con el tamaño corporal, por lo tanto, al cuantificar de manera absoluta la MME o MMEA debe ajustarse por el tamaño corporal usando talla (T) elevada al cuadrado (MMEA/T2). Esto se conoce como índice de masa musculoesquelética (IMME). También puede ajustarse por índice de masa corporal (IMC) (MMEA/IMC). La ventaja del uso de DEXA es que se puede obtener MMEA en pocos minutos con mínima radiación, mientras que la desventaja es que no es una metodología sencilla de usar y accesible en todos los medios y poblaciones. Adicionalmente, DEXA puede mostrar resultados alterados por el estado de hidratación del paciente7,25,26. Considerando su posibilidad de portabilidad y accesibilidad en la práctica clínica diaria, en general se prefiere el uso de BIA7.
Existen diferentes métodos de análisis de BIA: frecuencia simple, multifrecuencia, impedancia bioeléctrica segmental, espectroscopía bioeléctrica, análisis localizado de impedancia bioeléctrica y análisis de vectores de impedancia bioeléctrica. Tanto los métodos mencionados de BIA como otros métodos de referencia (DEXA, RM, TC, dilución de isotopos, etc.) tienen limitaciones y toman presupuestos, como la constante de densidad en la masa libre de grasa para DEXA o la constante de hidratación del 73% en BIA, que pueden no ser válidos en todas las situaciones.
Cuando no es posible utilizar ninguno de los métodos mencionados, se puede recurrir a las mediciones antropométricas, como la medición de CP, que demostró poder predecir el desempeño y sobrevida en adultos mayores. La CP se mide con el paciente de pie y las piernas ligeramente separadas. Se coloca una cinta métrica inextensible alrededor de la pantorrilla en el punto de máxima circunferencia y se debe tener la precaución de no comprimir o presionar el tejido subcutáneo para hacer la lectura. El punto de corte general es de 31 cm, por debajo de ese valor se considera baja masa muscular7,13,27. Todos los puntos de corte para evaluar la fuerza y masa muscular recomendados y usados se detallan en la Tabla 2.
Tabla 2: Herramientas para evaluar la fuerza muscular, la masa muscular y el desempeño físico.

TUG: timed up and go (test de la silla, levantarse de la silla sin apoyo y caminar); MMEA: masa musculoesquelética apendicular; IMME: índice de masa musculoesquelética; SPPB: short physical performance battery (batería corta de desempeño físico).
Desempeño físico
El desempeño o rendimiento físico se define como una función de todo el cuerpo, medida objetivamente y relacionada con la locomoción. Este es un concepto multidimensional que no afecta únicamente a los músculos, sino también la función del sistema nervioso central y periférico, incluyendo el equilibrio28.
En función de la evidencia, se han propuesto diversas formas para evaluar o medir el desempeño físico, por ejemplo: la velocidad de la marcha, la batería corta de rendimiento físico (short physical performance batery, SPPB) y la prueba de la silla (TUG). Vale aclarar que existen situaciones en las cuales no siempre es posible utilizar estas medidas de rendimiento físico, por ejemplo, cuando un paciente está afectado por la demencia, por el trastorno de la marcha o un trastorno en el equilibrio.
Sarcopenia en enfermedades reumáticas
La búsqueda de sarcopenia en las enfermedades reumáticas debería ser sistemática, dado que existe estrecha relación entre ambos fenómenos y la misma puede comprometer severamente la calidad de vida de estos pacientes.
Existe una cercana relación entre el músculo, el hueso y el cartílago. Durante el proceso de envejecimiento, la funcionalidad de estos tres tejidos se encuentra afectada28-31. Un ejemplo de esta relación son las fracturas, donde se puede observar la coexistencia de sarcopenia y osteoporosis. A partir de esta combinación de sarcopenia y baja densidad mineral ósea surge el concepto de osteosarcopenia. Ambas tienen un origen multifactorial. Los cambios en el sistema musculoesquelético relacionados con el envejecimiento pueden dar luz, en parte, al desarrollo de la osteosarcopenia. Algunos ejemplos son la disminución del número y tamaño de las fibras musculares, y la disminución del número de osteoblastos en las unidades de recambio óseo. Basado en la relación entre hueso y músculo, este fenotipo se asocia a un mayor riesgo de caídas, fracturas, dependencia y costo sanitario que sus componentes por separado. Dadas sus características, se considera un síndrome geriátrico28,31. Un metaanálisis demostró que la prevalencia de osteosarcopenia varía entre el 5-37%, siendo más frecuente en mujeres que en hombres32.
La osteoartritis es una enfermedad articular, degenerativa y crónica que se presenta con dolor, rigidez articular y pérdida progresiva de la función con impacto considerable en la calidad de vida28. Existe una relación entre la sarcopenia y la osteoartritis30. En adultos mayores, la combinación de la disminución en la síntesis muscular y una mayor destrucción del cartílago conduciría a un deterioro funcional, inactividad física y aumento del IMC. La evidencia sugiere que un mayor IMC se vincula a una concentración elevada de células adiposas, induciendo una mayor producción de adipocinas como la leptina que genera fenómenos proinflamatorios28,29. Está descripto que la obesidad sarcopénica se asocia mayormente con osteoartritis de rodilla, demostrando que el tejido adiposo juega un papel importante en su desarrollo28-30. Dentro de las consecuencias más relevantes de esta relación entre sarcopenia y osteoartritis se puede mencionar un mayor deterioro funcional, una mayor dependencia, institucionalización, mortalidad y aumento del gasto sanitario31.
Las personas con enfermedades sistémicas autoinmunes, como lupus eritematoso sistémico (LES), AR, espondiloartritis y esclerosis sistémica, están especialmente predispuestas a desarrollar sarcopenia33 debido a fenómenos proinflamatorios, inactividad y dolor.
El desgaste muscular se asocia inevitablemente con el catabolismo miofibrilar y con la consecuente liberación de enzimas musculares a la circulación. Varias condiciones que conducen a la atrofia muscular involucran diferentes vías de señalización intracelular que desencadenan apoptosis. Algunos ejemplos son: mayor degradación de proteínas a través de la autofagia, liberación de proteasas dependientes de calcio (calpaínas y caspasas), activación del sistema de proteosomas y disminución de la activación de las células satélite, responsables de la regeneración muscular34.
La pérdida de masa y fuerza muscular es dos a tres veces más común en personas con AR. Estos pacientes tienen una disminución más rápida en la fuerza de la prensión palmar que se relaciona inversamente con la duración de la enfermedad y es independiente de la edad33,34. Un reciente metaanálisis sobre 17 estudios determinó una prevalencia de sarcopenia en personas con AR de 31% (IC 95%: 25,2-37,4%; p=0,003)33. En un estudio local, publicado en 2021, se reportó que los parámetros musculares más bajos (masa magra total, porcentaje de masa magra y MMEA) se observaron en mujeres. El índice MMEA fue significativamente menor en las mujeres con AR (AR 31,0% vs. grupo control 11,9%) sin diferencias con los hombres. Adicionalmente, la masa grasa y la mayoría de los índices adiposos fueron significativamente más altos tanto en mujeres como en hombres con AR. Las pacientes con AR del sexo femenino tuvieron mayor prevalencia de sarcopenia y obesidad sarcopénica36. En relación a los tratamientos en pacientes con AR, una revisión reciente de la literatura con metaanálisis sobre ensayos clínicos aleatorizados y estudios observacionales sobre el uso de drogas modificadoras de la enfermedad (DMARs), sintéticas y biológicas, demostró que estos medicamentos no parecen tener un efecto significativo sobre la masa muscular. A pesar de este hallazgo, los autores mencionan que se requieren más estudios para aclarar esta posible asociación67.
En pacientes con LES, la literatura reporta una prevalencia cercana al 10%, mientras que en personas con espondiloartritis y esclerosis sistémica la prevalencia reportada es aún mayor, del 62,7%34. En referencia a la fibromialgia (FM), existen pocos estudios publicados hasta la fecha que evalúen la prevalencia de sarcopenia o el estado nutricional general en profundidad. Una publicación reciente de 202137, que evaluó a 45 mujeres con FM usando BIA y dinamometría de mano, encontró valores de fuerza muscular significativamente más bajos que los controles, pero no halló diferencia en relación con la masa musculoesquelética.
La carga inflamatoria y los tratamientos como los corticoides empujan la creciente prevalencia de sarcopenia. Se espera que, a medida que la población mundial envejezca, ciertas enfermedades reumáticas se incrementen. En el año 2000, el número de adultos mayores de 60 años era de aproximadamente 600 millones. Para 2025 este valor se duplicará y para 2050 la población adulta mayor estará cercana a los 2 billones. La detección, el tratamiento precoz y la prevención de la sarcopenia son estrategias que pueden mejorar la vida de las personas con enfermedades reumatológicas33.
Implicancias de la sarcopenia
La relevancia para diagnosticar precozmente este tipo de patologías musculares radica en el impacto clínico, económico, social y en la calidad de vida de las personas38-46. La sarcopenia se correlaciona con la disminución funcional, la discapacidad y con el incremento de caídas17,38. Adicionalmente, se asocia con un aumento del 50% en el riesgo de ingreso hospitalario, fracturas, dificultad para realizar las actividades de la vida diaria, desórdenes de la movilidad, pérdida de la independencia, discapacidad cognitiva46, aumento de 20 días de la estancia hospitalaria e incremento del 34 al 58% en los costos de atención sanitaria7,34,35,47-49. Dentro de los componentes que definen esta patología, se reconoce que la baja fuerza muscular (dinapenia) es el elemento más importante para predecir estos resultados adversos, incluyendo el incremento de la mortalidad7,34,45.
Entre las posibles intervenciones para prevenir y tratar la sarcopenia, la nutrición y la actividad física juegan un rol clave50-52. Preservar el equilibrio energético es de vital importancia durante un período de poca o nula actividad física, pero también cabe recordar que la sobrealimentación no atenúa la atrofia muscular53,54. La sobrealimentación solo aumenta la deposición de grasa47, por lo tanto, es la reducción de la ingesta de proteínas lo que lleva a la aceleración de la pérdida muscular. La ingesta habitual de proteínas en un hombre sano de 75 kg es aproximadamente de 60 a 90 g de proteína al día (0,8 a 1,2 g proteínas por kg de peso corporal)51,56. La disminución de la ingesta de proteínas, por cualquier motivo, por debajo de 0,8 g por kg de peso corporal por día dificulta extremadamente mantener la masa muscular17.
La disminución de la masa de proteínas musculares es el resultado neto de un desequilibrio entre la síntesis de proteína (anabolismo) y la proteólisis (catabolismo). La síntesis de proteínas requiere un suministro adecuado de aminoácidos de la dieta44,59,60. Aún en condiciones de sobrepeso u obesidad, al modular la composición de la alimentación, se debe considerar la óptima ingesta de proteínas y también la reducción del consumo de energía (dietas hipocalóricas que generan déficit energético para lograr un descenso de peso).
Existen situaciones (por ejemplo, envejecimiento o estados inflamatorios) en las que no existe un trastorno basal en la renovación o síntesis de proteínas, sino un debilitamiento de la respuesta anabólica a la ingesta de alimentos conocida como resistencia anabólica. Hay estrategias dietéticas eficaces que pueden compensar tal resistencia anabólica al maximizar la respuesta posprandial de la síntesis de proteína muscular después de la ingesta de alimentos20. Esto puede lograrse proporcionando más proteínas por comida (20 a 30 g) y con fuentes de proteínas específicas51.
Como parte de esta terapia nutricional, se incluye también a la vitamina D por su rol en la proliferación y diferenciación del musculoesquelético y como factor anabólico apoyando la síntesis proteica. Los ácidos grasos omega 3 (EPA y DHA) podrían mejorar el anabolismo de la proteína muscular y reducir los niveles de citoquinas proinflamatorias55. Adicionalmente, se prioriza la selección de proteínas con alto contenido en leucina, aminoácido que estimula la síntesis proteica a través de la vía de la mTor (mammalian target of rapamicina). Reciente evidencia56-58 demostró que la suplementación con beta-hidroxibeta-metilbutirato (CaHMB), metabolito del aminoácido leucina, puede ser una herramienta prometedora para mitigar la disminución de la masa muscular y preservar la función del músculo. El CaHMB actúa al estimular la síntesis proteica (vía mTor) e inhibir su degradación a través de la vía de señalización ubiquitina/proteasoma; también bloquea la sobreactivación del NF-kB y modula la inflamación producida por la apoptosis celular57-58. La nutrición es considerada parte esencial de la salud musculoesquelética junto con el ejercicio físico17.
El ejercicio beneficia tanto la fuerza muscular como el rendimiento físico. Las intervenciones de actividad física deben incluir un programa progresivo de ejercicios de resistencia para lograr resultados en la fuerza muscular, la masa muscular y el rendimiento físico, sobre todo en adultos mayores59-62. La combinación con ejercicio aeróbico puede ayudar a mejorar la resistencia cardiovascular y disminuir la masa grasa59-61,63. Cruz Jentoft et al.64 recomiendan que la intervención con ejercicios debe tener una duración mínima de 3 meses para obtener un impacto en la función muscular.
En referencia a la terapia médica, aunque algunos estudios mostraron cierta mejoría en algunos parámetros (masa muscular) utilizando dehidroepiandrosterona (DHEA), no se llegó a un consenso en su utilización. La mayoría de los estudios no evidenció mejoría consistente en la fuerza ni el rendimiento físico en pacientes con sarcopenia65-67. Hasta el momento no hay consenso para el uso de DHEA en pacientes con sarcopenia13,68,69. Del mismo modo, el estudio de Baltimore70 demostró aumento de la incidencia de cáncer de próstata en adultos mayores tratados con testosterona. En el caso de las mujeres, los estrógenos tampoco demostraron aumentar la masa o fuerza muscular. Si bien algunas drogas anabólicas, como la oxandrolona y los moduladores selectivos del receptor de andrógenos parecen ser prometedoras, se requieren más investigaciones antes que puedan formularse recomendaciones sobre su uso en sarcopenia. En estos momentos, no existe fármaco registrado para su tratamiento13,68-70.
Conclusiones
Actualmente están definidas las recomendaciones para el diagnóstico de la sarcopenia. A partir de la revisión del Consenso Europeo de 2018, se establece la pérdida de la fuerza muscular como un estado de sarcopenia probable, el cual se confirma con la certificación de baja masa muscular.
Hoy en día contamos con varias herramientas que permiten diferenciar la masa muscular, la densidad mineral ósea y la masa grasa corporal con diferentes grados de complejidad (DEXA, TC, RM, BIA, antropometría). De estos métodos en el ámbito clínico, el más recomendado es la DEXA y en la atención primaria, la antropometría por medición de la CP.
Varios estudios demostraron que la sarcopenia en las enfermedades reumáticas tiene una prevalencia mayor que en la población general52-54,57,58. Sería beneficioso mejorar el conocimiento de la interacción entre ambos grupos de enfermedades y su potencial tratamiento debido a las consecuencias y el impacto que pueden tener en la salud de los pacientes52.














