Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista argentina de cardiología
On-line version ISSN 1850-3748
Rev. argent. cardiol. vol.85 no.4 Ciudad Autónoma de Buenos Aires Aug. 2017
ARTÍCULO ORIGINAL
La cirugía miniinvasiva de la válvula mitral, ¿es posible en pacientes complejos?
Is Minimally Invasive Mitral Valve Surgery Possible in Complex Patients?
GERMÁN A. FORTUNATO, MATÍAS N. RÍOS, ROBERTO BATTELLINI, MARCELO HALAC, TORSTEN DOENST*, VADIM KOTOWICZ**
RESUMEN
Introducción: Los pacientes con riesgo preoperatorio alto de morbimortalidad, endocarditis mitral y aquellos con cirugía cardíaca previa son considerados "limitantes" para ser operados por vía cirugía miniinvasiva.
Objetivos: Evaluar resultados en pacientes complejos sometidos a cirugía miniinvasiva. Primario: mortalidad posoperatoria dentro de los 30 días. Secundario: resultados técnico-quirúrgicos y complicaciones posoperatorias tempranas.
Material y métodos: Análisis retrospectivo de las cirugías mitrales realizadas en el Hospital Italiano de Buenos Aires desde enero de 2010 hasta abril de 2016. Se realizaron 135 cirugías mitrales, 63 de ellas mediante técnica miniinvasiva (46,6%). Los pacientes considerados "complejos" fueron 45 (71,4%), incluyéndose aquellos con riesgo > 10% del STS PROMM, los pacientes con endocarditis activa y/o los pacientes con cirugía cardíaca previa.
Resultados: El 73,3% (n = 33) fueron cirugías electivas, el 22,2% (n = 10) de urgencia y el 4,4% (n = 2) de emergencia. El STS PROM% y el STS PROMM% fueron de 6,08 ± 10,8 y de 26,7 ± 16,8, respectivamente. Se incluyen 6 pacientes con cirugía cardíaca previa, 5 pacientes con endocarditis en tratamiento activo. Se realizaron reemplazo valvular mitral (14 reumáticas) en el 62% (n = 28) y plástica mitral en el 38% (n = 17). No se constataron óbitos en plástica mitral ni mediastinitis. La mortalidad a los 30 días fue del 4,4% (n = 2). Hubo conversión a esternotomía en un caso.
Conclusiones: La mortalidad observada es inferior a la calculada por puntaje de riesgo (STS PROMM%: 6,08 ± 10,8 vs. 4,4). La minitoracotomía derecha videoasistida nos ofreció una excelente exposición e interpretación de la patología. La técnica de cirugía miniinvasiva puede ser utilizada en pacientes con cirugía cardíaca previa, endocarditis y/o pacientes con puntaje alto de riesgo preoperatorio.
Palabras clave: Cirugía miniinvasiva - Cirugía valvular mitral - Plástica valvular mitral - Video-asistido - Reoperación
ABSTRACT
Background: Patients at high risk of preoperative morbidity and mortality, mitral valve endocarditis or prior cardiac surgery are considered "limiting" cases to undergo minimally invasive cardiac surgery.
Objectives: The aim of this study was to assess the outcome of complex patients undergoing minimally invasive surgery. The primary endpoint was post-operative mortality at 30 days and the secondary endpoint was the analysis of technical-surgical results and early postoperative complications.
Methods: The study consisted in the retrospective analysis of mitral valve surgeries performed at Hospital Italiano de Buenos Aires from January 2010 to April 2016. A total of 135 mitral valve surgeries, 63 by minimally invasive technique (46.6%) were performed. Forty-five patients (71.4%) were considered as "complex", including those with >10% STS-PROMM risk, active endocarditis, or prior cardiac surgery.
Results: Surgeries were elective in 73.3% of cases (n=33), urgent in 22.2% (n=10) and emergent in 4.4% (n=2). Percent STS-PROM and %STS-PROMM were 6.08±10.8 and 26.7±16.8, respectively. Six patients with prior cardiac surgery and 5 with endocarditis in active treatment were included. Mitral valve replacement (14 rheumatic) was performed in 62% of patients (n=28) and mitral valve repair in 38% (n=17). No deaths were registered in mitral valve repair or mediastinitis. Mortality at 30 days was 4.4% (n=2) and conversion to sternotomy was necessary in one case.
Conclusions: The observed mortality is lower than the one calculated by the risk score (%STS-PROMM 6.08±10.8 vs. 4.4). The right video-assisted minithoracotomy offered excellent exposure and interpretation of the disease. The minimally invasive surgical technique can be used in patients with prior cardiac surgery, endocarditis and/or patients with a high preoperative risk score.
Key words: Minimally Invasive - Mitral Valve Surgery - Mitral Valve Repair - Video-assisted - Reoperation
Abreviaturas
| ARM | Asistencia respiratoria mecánica |
| CCMI | Cirugía cardíaca miniinvasiva |
| CCP | Cirugía cardíaca previa |
| CEC | Circulación extracorpórea |
| CLP | Clampeo aórtico |
| El | Endocarditis infecciosa |
INTRODUCCIÓN
La cirugía miniinvasiva de la válvula mitral a través de un abordaje por toracotomía videoasistido fue reportado por primera vez en 1996 por Carpentier, (1) seguido al poco tiempo del primer reemplazo mitral por Chitwood. (2) El Heart Center Leipzig presentó en 1998 el sistema de ports y clampeo aórtico endoluminal. (3) Desde entonces, un gran número de investigadores han demostrado la factibilidad de realizar esta técnica en pacientes seleccionados. (4, 5) Aquellos con riesgo preoperatorio alto de morbimortalidad, endocarditis mitrales y antecedentes de cirugía cardíaca previa (CCP) mediante esternotomía fueron considerados "limitantes" para la cirugía miniinvasiva. Más de 7000 publicaciones están disponibles sobre la técnica de cirugía cardíaca miniinvasiva (CCMI) y todavía no hay acuerdo universal sobre la vía de abordaje.
En la endocarditis infecciosa (EI), la mortalidad reportada intrahospitalaria y a los 6 meses es del 18-27% y 22-27%, respectivamente. (6, 7) En 2014, Mihos y colaboradores discuten la hipótesis de que un abordaje miniinvasivo de la válvula mitral nativa puede reducir el trauma quirúrgico y las complicaciones posoperato-rias en EI. (8)
Las reoperaciones por esternotomía aumentan la morbimortalidad perioperatoria por sangrado: lesión de un injerto permeable, ventrículo derecho u otra estructura cardíaca, taponamiento cardíaco y mediasti-nitis. La dificultad en la exposición de la válvula mitral representa un desafío, por lo que la técnica de CCMI fue introducida para el abordaje mitral alternativo.
La mayoría de los reportes refieren que la calidad de la reparación o del reemplazo, así como la seguridad en el procedimiento, no se ven afectados por un abordaje miniinvasivo cuando se comparan con la es-ternotomía. (9-14) La videocámara cumple una función primordial en el diagnóstico.
En este trabajo nos planteamos ciertas preguntas para llegar a determinados objetivos. Dentro de las primeras consideramos: 1) ¿Es factible la utilización de cirugía miniinvasiva de la válvula mitral en pacientes con riesgo elevado de morbimortalidad? 2) ¿Es el uso de la videocámara un problema para los cirujanos cardíacos, destacando que en cirugía torácica y abdominal ya es la regla? 3) A través del tiempo los procedimientos aórticos, incluyendo la aorta ascendente, se han realizado por vía miniinvasiva, ¿por qué no se ha extendido para la válvula mitral? (12-15)
EIC Espacio intercostal
EPOC Enfermedad pulmonar obstructiva crónica
ETE Ecografía transesofágica
NV Aguja de venteo
PM Plástica mitral
RVM Reemplazo de válvula mitral
El objetivo propuesto fue evaluar la evolución clínica de los pacientes complejos sometidos a cirugía miniin-vasiva de la válvula mitral. Como objetivo primario se analizó la mortalidad posoperatoria a los 30 días, y el secundario comprendió el análisis de los resultados técnico-quirúrgicos y las complicaciones posoperatorias tempranas.
MATERIAL Y MÉTODOS
Se analizaron retrospectivamente las historias clínicas electrónicas de todos los pacientes sometidos a CCMI mitrales desde enero de 2010 (inicio del programa) hasta abril de 2016, lo que permitió el 100% de seguimiento (mediana: 19 meses). Durante este período se realizaron 135 cirugías mitrales, de las cuales 63 fueron por vía miniinvasiva (46,6%). El número de pacientes CCMI complejos fue de 45 (71,4%).
Criterios de inclusión: Pacientes intervenidos por CCMI con riesgo de morbimortalidad > 10% por STS (The Society of Thoracic Surgery Predicted of Risk of Mortality), endocarditis mitral activa o CCP. Se excluyeron los pacientes sometidos a cirugía mitral por esternotomía mediana y aquellos que no cumplían el criterio de paciente complejo. En estos pacientes se evaluaron las siguientes variables independientes: edad, sexo, clase funcional preoperatoria, etiología valvular, STS PROM% y PROMM%, estado preoperatorio (electivo, urgencia, emergencia), tiempo de circulación extracorpórea (CEC), tiempo de clampeo aórtico (CLP), procedimientos asociados, sangrado torácico a las 6, 24 y 48 horas del posoperatorio, tiempo de asistencia respiratoria mecánica (ARM) intrahospitalario y días de internación.
Siguiendo a Mihos (8), Tang (16) y Holzhey (17) definimos paciente "complejo" al que presentaba:
1. Factores de riesgo para STS PROMM > 10% de morbi-mortalidad.
2. Endocarditis activa: Todo paciente cursando internación y tratamiento con antibióticos por dicho cuadro infeccioso.
3. CCP: Pacientes sometidos previamente a cirugía cardíaca a través de esternotomía. Estos fueron estudiados previamente con tomografía de tórax para evaluar adherencias. Complicaciones tempranas: Se consideraron la necesidad
intraoperatoria de conversión a esternotomía convencional, arritmias cardíacas (bloqueo auriculoventricular, fibrilación auricular), accidente cerebrovascular por anticoagulación, neumonía intrahospitalaria, insuficiencia renal (creatinina +1 del basal o requerimiento de hemodiálisis).
Mortalidad posoperatoria temprana: Este criterio se definió como el óbito dentro de los 30 días posoperatorios. Se evaluó mortalidad al año de seguimiento.
Técnica quirúrgica: Abordaje de 7 cm por minitoracoto-mía derecha por el 4to-5to espacio intercostal (EIC). Se usaron dos puertos accesorios (5 mm) para la inserción del clamp aórtico de Chitwood (3to EIC derecho, línea media axilar) y videocámara (4to EIC derecho). Se utilizaron: retractor atrial, modelo Mohr (Geister®), instrumentos largos para cirugía miniinvasiva (Geister®) y anudadores largos. Se usó videocámara (Storz®) con brazo mecánico, mientras que para el manejo de CEC se emplearon cánulas arteriales y venosas largas (Edwards® o Medtronic®) a través de una incisión mínima (3-4 mm) en arteria y vena femoral. En todos los casos la posición de las cánulas fue guiada y controlada mediante ecografía transesofágica (ETE). La cardioplejía utilizada fue la Bretschneider® en dosis única de 2000 ml. Con el fin de lograr el desaireamiento se empleó un tercer aspirador una vez cerrada la auriculotomía izquierda más aguja de venteo aórtico (NV). Se continuó en CEC reduciendo la perfusión hasta detener la bomba de CEC con la NV colocada. Una vez asegurada por ETE la ausencia de burbujas en el corazón, se reinició brevemente la CEC para retirar la NV y agregar punto extra de hemostasia.
Análisis estadístico
La información obtenida se ingresó en una base de datos. Cada una de las variables observadas se volcó en una tabla de frecuencias con el objetivo de analizar su distribución. Las variables continuas con distribución normal se expresaron como media y desviación estándar. Las variables con distribución no paramétrica se expresaron como mediana con rango intercuartil 25-75%. Las variables discretas, por su parte, se expresaron como porcentajes.
Consideraciones éticas
El estudio se llevó a cabo siguiendo las recomendaciones para la investigación en humanos y las normativas legales vigentes. Dado que se realizó una revisión de historias clínicas y no se reportaron datos que permitieran identificar a sus titulares, no se obtuvo consentimiento informado de los pacientes (salvo en el caso de datos faltantes, en cuyo caso se realizó un llamado telefónico). Los miembros del estudio implementaron medidas para proteger la privacidad y confidencialidad de los datos de acuerdo con la normativa legal vigente (Ley 25.326 de Protección de Datos Personales).
RESULTADOS
Características preoperatorias
Las características preoperatorias de los pacientes se detallan en la Tabla 1.
El 73,3% (n = 33) fueron cirugías electivas, el 22,2% (n = 10) de urgencia (insuficiencia cardíaca congestiva, disnea grave o endocarditis) y el 4,4% de emergencia. Se consideraron de emergencia los pacientes con shock cardiogénico, edema agudo de pulmón y requerimientos de inotrópicos y ARM (n = 2). Seis pacientes habían tenido CCP por esternotomía mediana y otros 5 padecían de endocarditis activa preoperatoria (Figura 1). Las seis cirugías de los pacientes con CCP fueron comisurotomía mitral, plástica mitral (PM), reemplazo de válvula mi-tral (RVM), cirugía combinada de reemplazo mitral más revascularización miocárdica, Bentall de Bono, siendo esta a su vez la quinta reoperación luego de múltiples cirugías aórticas, y un caso con antecedente de Bentall de Bono más endocarditis activa.
El STS PROM% y el STS PROMM% fueron de 6,08 ± 10,8 y de 26,7 ± 16,8, respectivamente.
Los resultados en cuanto a la etiología valvular se grafican en la Figura 2, con sus respectivos porcentajes. Se destaca como principal causa la degenerativa/mixoi-
| Tabla 1. Características preoperatorias de mediante cirugía miniinvasiva | pacientes intervenidos | ||
| Variable | Media ± DE o n (%) | ||
| Pacientes | 45 (100) | ||
| Edad, años | 68 ± 14,7 | ||
| Edad, mediana | 71 | ||
| Sexo femenino | 32 (71,1) | ||
| NYHA | 2,4 ± 0,9 | ||
| STS PROM% | 6,08 ± 10,8 | ||
| STS PROMM% | 26,7 ± 16,8 | ||
| Cirugía cardíaca | previa | 6 | |
| Endocarditis | 5 | ||
DE: Desviación estándar. NYHA: New York Heart Association.
40 35 30 25 20 15 10
STS < 10%
(n = 34)
Reoperación (n = 6)
Endocarditis (n = 5)
Fig. 1. Clasificación de grupos considerados "complejos".
Características quirúrgicas y posoperatorias
Los procedimientos asociados fueron: Maze (n = 5), exéresis de trombo auricular (n = 1) y cierre de foramen oval permeable (n = 1). Las cirugías realizadas fueron: RVM [n = 28 (62%), 19 con válvula biológica y 9 mecánica], PM [n = 17 (38%), 15 con neocuerda y 2 sin neocuerda]. Los resultados intraoperatorios y posoperatorios se presentan en la Tabla 2, mientras que las diferentes técnicas realizadas se muestran en la Figura 3.
El tiempo promedio de internación hospitalaria fue de 16,5 ± 14,8 días.
Complicaciones y mortalidad
Solo una paciente que recibió RVM requirió conversión intraoperatoria a esternotomía mediana debido a sangrado a nivel del surco auriculoventricular. No se constataron óbitos en plásticas mitrales ni se registraron mediastinitis ni sangrados por la raíz de la aorta.
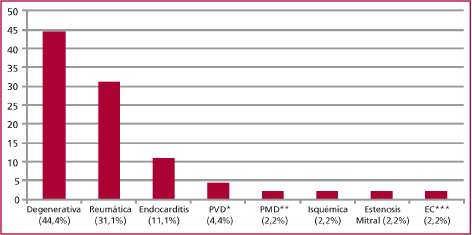
Fig. 2. Patologías preoperatorias. PVD: Prótesis valvular disfuncionante. PMD: Plástica valvular disfuncionante. EC: Lesión valvular por endocarditis curada.
Tabla 2. Resultados intraoperatorios y posoperatorios de pacientes intervenidos mediante cirugía miniinvasiva
| Variable | Media ± | DE (rango) o n (%) |
| Tiempo CEC, min | 191,8 | ± 63,9 (121-350) |
| Tiempo clampeo, min | 115,8 | ± 63,9 (87-182) |
| Plástica mitral | 17 (38) | |
| Reemplazo mitral | 28 (62) | |
| Prótesis biológica | 19 (42) | |
| Prótesis mecánica | 9 (20) | |
| Conversión intraoperatoria | 1 | |
| Sangrado posoperatorio, ml | ||
| 6 horas | 211,2 | |
| 24 horas | 413 | |
| 48 horas | 529,2 | |
| Tiempo de internación, días | 16,5 | ± 14,8 (5-70) |
RVM mecánica (n = 9)
RVM biológica (n = 19)
Plástica mitral (n = 17)
Fig. 3. Proporción de técnicas quirúrgicas utilizadas.
Mortalidad: El primer caso fue una mujer de 76 años a quien se le realizó RVM y conversión a esternotomía
para descalcificación del anillo mitral; falleció el día 7 por falla multiorgánica. El segundo caso, un hombre de 82 años en tratamiento activo por endocarditis y antecedentes de cirugía combinada previa (cirugía de revascularización miocárdica + RVM), a quien se le realizó re-reemplazo mitral. Fallece el día 21 por accidente de anticoagulación (hematoma subdural y de tronco encefálico).
La mortalidad a los 30 días fue del 4,4% (n = 2). La mortalidad de la serie al año de seguimiento fue del 8,8% (n = 4). Un óbito se produjo el día 60 luego de un accidente cerebrovascular por anticoagulación y otro el día 80 posterior a neumonía intrahospitalaria. Las complicaciones posoperatorias dentro de los 30 días se resumen en la Tabla 3.
DISCUSIÓN
La definición de "paciente complejo" es un tema contro-versial en la literatura, probablemente por la variada disponibilidad de predictores de riesgo (EuroSCORE II y STS score) y la falta de ellos en la discriminación de los límites superiores de riesgo quirúrgico. Debido a la ausencia de una definición precisa de complejidad por EuroSCORE II o STS, adoptamos la definición de Mihos y colaboradores, (8) que incluyeron EI, enfermedad pulmonar obstructiva crónica (EPOC) (40,9%) y reoperaciones (18,1%), Tang y colaboradores, (16) que incluyeron pacientes con insuficiencia renal crónica y disnea en clase funcional IV (NYHA) (43%), reoperaciones (37,7%), EI (17,7%) y EPOC (22,2%), y Holzhey y colaboradores, (17) que incluyeron pacientes mayores de 70 años y reoperaciones (14,7%), EPOC (8,6%), EI (4,9%) y fracción de eyección del ventrículo izquierdo inferior al 30% (4,9%). (18)
| Tabla 3. Complicaciones posoperatorias de mediante cirugía miniinvasiva | pacientes | intervenidos |
| Variable | n (%) | |
| Fibrilación auricular | 8 (17,7) | |
| Bloqueo AV | 4 (8,8) | |
| Insuficiencia renal aguda | 3 (6,6) | |
| Hemorragia SNC por ACO | 3 (6,6) | |
| Reexploración por sangrado | 1 (2,2) | |
AV: Auriculoventricular. SNC: Sistema nervioso central. ACO: Anticoagulación.
Se discute que la canulación arterial femoral podría generar aumento de accidente cerebrovascular embólico en caso de arteriopatía periférica (por retro-perfusión). (19) Nuestros pacientes fueron evaluados previamente con eco-Doppler arterial de vasos femorales descartándose la patología vascular oclusiva, lo cual se vio reflejado en la ausencia de dicha complicación.
El abordaje a través de una minitoracotomía derecha podría realizarse rutinariamente, con resultados favorables cuando las estrategias de perfusión y de clampeo se seleccionan cuidadosamente. Es elemental realizar el desaireamiento de la manera explicada previamente. Así, el riesgo de microembolia aérea y de sangrado aórtico no son mayores que con la cirugía convencional. (20) No tuvimos tromboembolia aérea, coincidiendo con la serie de Misfeld. (21)
Los pacientes prefieren la miniinvasividad si esta se les ofrece. ¿Por qué no ha prosperado? ¿Podría estar sucediendo que los cirujanos de hoy no deseen adoptar técnicas de CCMI solo porque presumiblemente son más complejas? Un argumento contra la cirugía miniinvasiva mitral es que dada la combinación de miniinvasión más el uso de cámara e instrumentos largos puede ser más demandante para enseñar, constituyéndola en una subespecialización. En la actualidad son escasos los programas de entrenamiento sistematizados al estilo de las válvulas percutáneas y sus programas de formación. Aunque hay programas de fellowship en CCMI (Leipzig y Berlín), no hay "proctorización" estructurada para esta cirugía. Además, los tiempos de CEC y CLP mayores generan dudas entre los cirujanos.
La técnica de CCMI ha mostrado, a través de los años, suficiente evidencia de una tasa baja de mortalidad y stroke en el corto y largo plazo. (8, 9) Se ha asociado con disminución del sangrado posoperatorio, transfusiones, tiempo de ARM, tiempo de internación hospitalaria, menor dolor posoperatorio y reinserción laboral precoz. (22) No obstante, la CCMI debería quizás limitarse a centros especializados y entrenados en la técnica quirúrgica y el manejo perioperatorio. Si se pudieran ofrecer resultados constantes de baja mortalidad, reoperación y una tasa alta de reparación, esta técnica podría llegar a ser de primera elección. Nuestro campo no podrá desarrollarse si los cirujanos continúan siendo escépticos y limitan el crecimiento como ha demostrado la historia con otras innovaciones quirúrgicas. En base a los desarrollos actuales en el campo cardiovascular, uno debe preguntarse: ¿Actuaríamos de acuerdo con la evidencia, incluso si la tuviéramos? (23)
Finalmente, nos adherimos a Joseph E. Bavaria en su Presidential address (2017): "La línea delgada entre proveer tratamientos de calidad y abrazar la innovación puede a veces hacernos sentir atrapados a los cirujanos cardíacos entre metas conflictivas. Pueden colisionar unas con otras, lo cual es un desafío que tenemos que sortear." (24)
CONCLUSIONES
La minitoracotomía derecha videoasistida nos ofreció una excelente exposición e interpretación de la patología, minimizando la necesidad de disección quirúrgica y la morbimortalidad. La técnica de CCMI se pudo utilizar en pacientes con CCP, EI y/o pacientes con puntaje de riesgo preoperatorio alto cuando el hemitórax derecho se encontró libre de adherencias.
El sangrado a las 24 horas fue escaso (211-413 ml/%), con un solo caso que requirió reexploración por sangrado posoperatorio. No hubo complicaciones embólicas. La mortalidad observada en esta serie fue inferior que la del cálculo previo del puntaje de riesgo (STS PROM% 6,08 ± 10,8 vs. 4,4). Las complicaciones posoperatorias fueron de baja magnitud.
Los beneficios potenciales de la CCMI, la baja incidencia de sangrado, la movilización precoz y los resultados cosméticos pueden ser solo factores débiles que impulsan a adoptar esta técnica. Creemos que el desarrollo hoy en día es impulsado por factores no basados en la evidencia, como el aumento en la demanda de los pacientes y de los médicos de referencia, así como por la necesidad personal de pertenecer a un grupo de expertos altamente especializados.
En resumen, nuestra disposición a seguir evidencias y guías podría estar sustancialmente influida por factores de confusión no científicos (complejidad del procedimiento, competencia con otros centros o disciplinas), y por último, pero no menos importante, por la demanda del paciente. En el futuro, así como la cirugía miniinvasiva aórtica intenta competir contra TAVI, la cirugía miniinvasiva mitral se encuentra en mejores condiciones para competir contra TMVR (transcatheter mitral valve repair), ya que la reparación percutánea de la enfermedad degenerativa es muy inferior al tipo Mohr por CCMI.
Finalmente, afianzamos nuestra creencia de que el desarrollo de un equipo interdisciplinario en valvulo-patías (Heart Team mitral) es imprescindible para la toma de decisiones y tácticas quirúrgicas.
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
BIBLIOGRAFÍA
1. Carpentier A, Loulmet D, Carpentier A, Le Bret E, Haugades B, Dassier P, et al. Open heart operation under videosurgery and mini-thoracotomy. First case (mitral valvuloplasty) operated with success]. C R Acad Sci III 1996;319:219-23.
2. Chitwood WR Jr, Elbeery JR, Chapman WH, Moran JM, Lust RL, Wooden WA, et al. Video-assisted minimally invasive mitral valve surgery: the "micro-mitral" operation. J Thorac Cardiovasc Surg 1997;113:413-4. http://doi.org/bnghsq
3. Mohr F^ Falk V, Diegeler A, Walther T, van Son JA, Autschbach R. Minimally invasive port-access mitral valve surgery. J Thorac Cardiovasc Surg 1998;115:567-74. http://doi.org/c42rpz
4. McClure RS, Athanasopoulos LVJ McGurk S, Davidson MJ, Couper GS, Cohn LH. One thousand minimally invasive mitral valve opera-tions: early outcomes, late outcomes, and echocardiographic follow-up. J Thorac Cardiovasc Surg 2013;145:1199-206. http://doi.org/cbcf
5. Modi P, Rodriguez E, Hargrove WC 3rd, Hassan A, Szeto WY, Chit-wood WR Jr. Minimally invasive video-assisted mitral valve surgery: a 12-year, 2-center experience in 1178 patients. J Thorac Cardiovasc Surg 2009;137:1481-7. http://doi.org/dg2rzn
6. Hasbun R, Vikram HR, Barakat LA, Buenconsejo J, Quagliarello VJ. Complicated Left-Sided Native Valve Endocarditis in Adults Risk Cíassificatión for Mortality. JAMA 2003;289:1933-40. http:// doi.org/cwgsv6
7. Wallace SM, Walton BI, Kharbanda RK, Hardy R, Wilson AF¡ Swan-ton RH. Mortality from infective endocarditis: clinical predictors of outcome. Heart 2002;88:53-60. http://doi.org/b8csv9
8. Mihos CG, Santana O, Pineda AM, Lamas GA, Lámelas J. Right anterior minithoracotomy versus median sternotomy surgery for native mitral valve infective endocarditis. J Heart Valve Dis 2014;23:343-9. http://doi.org/bhvqsm
9. Botta L, Cannata A, Bruschi G, Fratto P, Taglieri C, Russo CF, et al. Minimally invasive approach for redo mitral valve surgery J Thorac Dis 2013;5(Suppl 6):S686-93.
10. Seeburger J, Borger MA, Falk V, Passage J, Walther T, Dolí N, et al. Minimally invasive mitral valve surgery after previous sternotomy: experience in 181 patients. Ann Thorac Surg 2009;67:709-14. http://doi.org/bhvqsm
11. Kızıltan HT, ídem A, Salihi S, Demir AS, Korkmaz AA, Güden M. Mitral valve surgery using video-assisted right minithoracotomy and deep hypothermic perfusión in patients with previous cardiac operations. J Cardiothorac Surg 2015;10:55. http://doi.org/f69x5t
12. Glauber M, Ferrarini M, Miceli A. Minimally invasive aortic valve surgery: state of the art and future directions. Ann Cardiothorac Surg 2015;4:26-32.
13. LaPietra A, Santana O, Pineda AM, Mihos CG, Lámelas J. Outcomes of aortic valve and concomitant ascending aorta replacement performed via a minimally invasive right thoracotomy approach. Innovations 2014;9:339-42. http://doi.org/cbch
14. Joshi D, Santana O, LaPietra A, Lamelas J. Minimally invasive valve surgery with bypass to the right coronary artery. Innovations 2013;8:440-2. http://doi.org/cbcj
15. Mihos CG, Santana O, Pineda AM, La Pietra A, Lamelas J. Aortic valve replacement and concomitant right coronary artery bypass grafting performed via a right minithoracotomy approach. Innova-tions 2014;9:302-5. http://doi.org/cbck
16. Tang P, Onaitis M, Desai B, Gaca JG, Milano CA, Stafford-Smith M, et al. Minithoracotomy versus sternotomy for mitral surgery in patients with chronic renal impairment: a propensity-matched study. Innovations (Phila) 2013;8:325-31. http://doi.org/cbcm
17. Holzhey DM, Shi W, Borger MA, Seeburger J, Garbade J, Pfan-nmüller B, et al. Minimally invasive versus sternotomy approach for mitral valve surgery in patients greater than 70 years old: a propensity-matched comparison. Ann Thorac Surg 2011;91:401-5. http://doi.org/bmxx8d
18. Svensson LG, Gillinov AM, Blackstone EH, Houghtaling PL, Kim KH, Pettersson GB, et al. Does right thoracotomy increase the risk of mitral valve reoperation? J Thorac Cardiovasc Surg 2007;134:677-82. http://doi.org/bg3mvf
19. Moscarelli M, Fattouch K, Casula R, Speziale G, Lancellotti P, Athanasiou T. What is the role of minimally invasive mitral valve surgery in high-risk patients? A meta-analysis of observational studies. AnnThorac Surg 2016;101:981-8. http://doi.org/f793pv
20. Schneider F, Onnasch J F, Falk V, Walther T, Autschbach R, Mohr F W. Cerebral microemboli during minimally invasive and conven-tional valve operations. AnnThorac Surg 2000;70:1094-7. http://doi. org/bdvdcd
21. Misfeld M, Mohr F W. Video-atlas on minimally invasive mi-tral valve surgery- the Mohr technique. Ann Cardiothorac Surg 2013;2:825-7.
22. Barbero C, Marchetto G, Ricci D, El Qarra S, Attisani M, Filippini C, et al. Right minithoracotomy for mitral valve surgery: impact of tailored strategies on early outcome. Ann Thorac Surg 2016;102:1989-1994. http://doi.org/f9g3h5
23. Doenst T, Lamelas J. Do we have enough evidence for minimally-invasive cardiac surgery? A critical review of scientific and non-scientific information. (Comunicación Personal, en prensa).
24. Bavaria J. Presidential Address on "Quality and Innovation in Cardiothoracic Surgery: Colliding Imperatives?" STS 53rd Annual Meeting 2017.














