Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. vol.84 no.6 Ciudad Autónoma de Buenos Aires dic. 2016
CARTAS CIENTÍFICAS
Pericarditis constrictiva crónica tras cirugía cardiovascular
La pericarditis constrictiva posterior a cirugía cardíaca (PCP) es una entidad única, con características distintivas respecto de otras etiologías de pericarditis constrictiva. Desde su descripción inicial en 1972 se han publicado varios casos aislados pero muy pocas series, ya que su verdadera incidencia probablemente sea subestimada por su presentación inespecífica y sutil, por lo que requiere una alta sospecha clínica. (1)
En esta presentación describimos el caso de un paciente que desarrolló PCP tras una cirugía cardíaca. Se trata de un paciente masculino de 61 años con factores de riesgo cardiovascular: sobrepeso, extabaquista y dislipidemia. Tiene antecedentes de radioterapia por linfoma de Hodgkin a los 23 años, implante de marca-pasos por bloqueo AV de tercer grado (2008), fibrilación auricular, cirugía de reemplazo de la válvula aórtica mecánica por estenosis aórtica grave (2013), sintomática con disnea en clase funcional (CF) I-II.
Luego de la cirugía cardíaca persistió por meses con síntomas progresivos, disnea en CF III-IV, astenia e hiporexia, internaciones reiteradas por insuficiencia cardíaca descompensada con paracentesis evacuadoras por ascitis, congestión hepática, pérdida de peso, ingurgitación yugular y signo de Kussmaul. En el estudio de su etiología se le diagnosticó anemia hemolítica, por lo que se sospechó y se confirmó una fuga (leak) periprotésica, que fue tratada por medio de implante del Amplatzer vascular plug 4. Intercurrió con taquicardia mediada por marcapasos, con ritmo de base FA de alta respuesta ventricular. También se descartó mal funcionamiento de la válvula aórtica protésica.
Tras descartarse los distractores antes mencionados como causa de su probable disnea e insuficiencia cardíaca y continuar con la misma sintomatología, se sospecha pericarditis constrictiva crónica (PCC), por lo que se realiza una tomografía computarizada multicorte de tórax, que evidencia engrosamiento pericárdico en la cara anterolateral de 12 mm de espesor (Figura 1). Se repite el Doppler cardíaco, que informa variabilidad respiratoria anormal en el flujo del tracto de salida del ventrículo izquierdo, en la velocidad diastólica de las venas pulmonares y en el flujo tricuspídeo. Cavidades derechas levemente dilatadas con septum interauricular e interventricular volcado a cavidades izquierdas. Engrosamiento del pericardio, por material homogéneo, no calcificado de 8 mm de espesor que envuelve la cavidad ventricular, que genera fisiología constrictiva con marcados signos de congestión sistémica. Función sistólica preservada y disfunción diastólica de grado III.
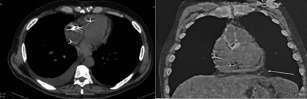
Fig. 1. Tomografía computarizada multicorte de tórax que muestra el engrosamiento del pericardio.
Luego de confirmarse la PCP se realizó la pericar-diectomía. El estudio anatomopatológico del pericardio informó un proceso inflamatorio crónico con fibrosis, calcificación y reacción gigantocelular de tipo cuerpo extraño (Figura 2). Unos meses luego de la pericardiec-tomía encontramos que hubo una paulatina y progresiva mejoría. El paciente se encuentra con disnea en CF II, estable, disminución de los edemas en los miembros inferiores y de su ascitis, con aumento de peso (por incremento de la masa muscular) y mejoría de su estado general. Continúa solamente con tratamiento médico para insuficiencia cardíaca congestiva.
La pericarditis constrictiva es la fase final de un proceso inflamatorio del pericardio. La etiología más frecuente es la idiopática (48%), seguida en orden de frecuencia por la posquirúrgica, la lesión por radiación y la tuberculosis en países en desarrollo.
La PCP es una complicación inusual, de la que se estima una incidencia del 0,025-0,3%. (2) El tiempo de presentación puede ser extremadamente variable, con un rango reportado de entre 1 mes y 240 meses después de la cirugía cardíaca. Por esta razón debe mantenerse un alto nivel de sospecha en el seguimiento posoperatorio y a largo plazo. El perfil que caracteriza a los pacientes afectados por PCP es la edad avanzada, una alta prevalencia de sexo masculino, historia de infarto de miocardio y diabetes. Otros factores que han sido implicados en el desarrollo de la PCP incluyen radiación previa, infección de la herida posoperatoria y osteomielitis. (3)
Su fisiopatología permanece poco clara y es probable que sea multifactorial. La mayoría se desarrollan con el pericardio abierto al finalizar la cirugía. La acumulación de sangre es el estímulo inicial para el desarrollo de adherencias. Existe una respuesta inflamatoria aumentada con elevación de citoquinas (IL-6, IL-1 y TFN-α) y aumento del estrés oxidativo, lo cual genera un síndrome pospericardiectomía que puede progresar a una pericarditis exudativa. El aumento de los factores de crecimiento en este proceso produce fibrosis y posterior constricción. Otro factor probablemente asociado es cierto grado de contaminación bacteriana del pericardio que potenciaría el cuadro inflamatorio. La resolución incompleta de este cuadro es el paso inicial hacia la cronicidad. Las distintas respuestas inflamatorias entre los pacientes (extensión de la fibrosis, inflamación y neovascularización) explica la variabilidad del intervalo de tiempo entre la cirugía y el diagnóstico de PCP.
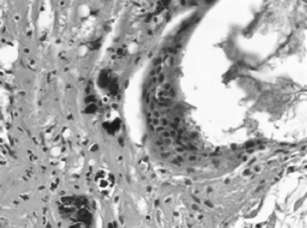
Fig. 2. Anatomía patológica del pericardio con su proceso inflamatorio.
Aunque los signos clínicos, la ecocardiografía y la tomografía computarizada pueden aumentar la sospecha de PCP, el patrón oro diagnóstico sigue siendo la medición directa del igualamiento de las presiones en diástole de las cuatro cámaras y el registro de la dip-plateau. La resonancia magnética es la técnica más sensible para el diagnóstico de pericardio engrosado o calcificado. Sin embargo, se han reportado casos de PCP sin engrosamiento pericárdico, como también de engrosamiento pericárdico sin fisiología de constricción pericárdica, llevando al diagnóstico incorrecto de esta entidad. (4)
La pericardiectomía es el único tratamiento para la constricción permanente. Las indicaciones se basan en la sintomatología, los hallazgos en la ecocardiografía, la resonancia magnética/tomografía computarizada y el cateterismo cardíaco. Este procedimiento es de alto riesgo, con una mortalidad del 5-21%. Su beneficio puede ser pobre en pacientes en los que no se realiza una pericardiectomía extensa y en pacientes con PCC por radioterapia. (5) La recuperación de la capacidad funcional (mejoría clínica) puede tomar semanas a meses y se correlaciona con persistencia de alteraciones en el llenado ventricular en el ecocar-diograma. Puede que hasta un tercio de los pacientes no mejoren o continúen con signos de insuficiencia cardíaca. Cambios crónicos y a veces irreversibles como la fibrosis y la atrofia del miocardio adyacente pueden ser un importante marcador pronóstico pospericardiectomía. La baja fracción de eyección, la presión diastólica elevada, la insuficiencia renal, la insuficiencia tricuspídea moderada a grave y la edad avanzada también son predictores de incremento de la mortalidad y pobre resultado a largo plazo. (6)
La PCP tiene una fisiopatología peculiar y distintiva que difiere en parte de las otras causas de pericarditis constrictivas y, aunque su explicación no sea concluyente, se debe sospechar sobre todo cuando se descartan otras causas de disnea e insuficiencia cardíaca durante el seguimiento de pacientes que tuvieron cirugía cardíaca.
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
José Quiñones, Luis Mantilla, Heber Sucasaca, Daniel Aragón, Eli Arado, Carlos Schmidt
Sanatorio Adventista del Plata, Entre Ríos, Argentina joseluis.quinones@sanatorioadventista.com.ar
BIBLIOGRAFÍA
1. Kutcher MA, King SBII, Alimurung BN, Craver JM, Logue RB. Constrictive pericarditis as a complication of cardiac surgery: reconig-tion of an entity. Am J Cardiol 1982;50:742-8. http://doi.org/ff9s8c
2. Peset A, Marti V, Cardona M, Montiel J, Guindo J, Domínguez J. Resultados de la pericardiectomía por pericarditis constrictiva crónica. Rev Esp Cardiol 2007;60:1097-101. http://doi.org/cfqscp
3. Dardas P, Tsikaderis D, Ioannides E, Bisbos A, Smirlis D, Arditis I, et al. Constrictive pericarditis after coronary artery bypass surgery as a cause of unexplained dyspnea: a report of five cases. Clin Cardiol 1998;21:691-4. http://doi.org/cvg8q3
4. Gaudino M, Anelmi A, Pavone N, Massetti M. Constrictive pericarditis after cardiac surgery. Ann Thorac Surg 2013;95:731-6. http:// doi.org/bvfd
5. Sagristà-Sauleda J. Síndromes de constricción cardiaca. Rev Esp Cardiol 2008;61(Supl 2):33-40.
6. Braunwald E, Bonow R, Mann D, Zipes D, Libby P. Tratado de cardiología: Texto de medicina cardiovascular. 9ª ed. Barcelona: Elsevier; 2013. p 1684-88.
Rev Argent Cardiol 2016;84:603-604. http://dx.doi.org/10.7775/rac.es.v84. i6.9430
Disección coronaria espontánea: una causa poco frecuente de shock cardiogénico en mujeres jóvenes
La disección coronaria espontánea (DCE) es una causa infrecuente de síndrome coronario agudo (SCA). Se presenta en mujeres jóvenes, en ocasiones con elevación del segmento ST y se asocia con displasia fibromuscular (DFM). (1-4) Puede manifestarse como disección con rotura intimal o como hematoma intramural. En general se resuelven espontáneamente con buen pronóstico a largo plazo, (1, 2, 4, 5) pero en ocasiones la evolución es más compleja, como los casos que presentamos.
Caso 1: Mujer de 46 años, sin factores de riesgo. Consultó por angor de 3 horas de duración asociado con síntomas vagales. ECG sin cambios isquémicos, troponina ultrasensible 281 ng/L (VN < 14 ng/L) y ecocardiograma con hipocinesia anterolateral y medioa-pical. La CCG evidenció una lesión grave proximal en la subdivisión inferior del primer ramo diagonal (Dg), optándose por tratamiento médico. Treinta minutos luego de la CCG presentó TV polimorfa (TVP) y paro cardiorrespiratorio (PCR). El ECG presentaba supra-desnivel del ST (SST) de 3 mm de V2-V4. Se repitió la CCG, observándose progresión de lesión previa. Se intentó angioplastia (ATC), que resultó fallida. A los 20 minutos repitió angor, TVP y PCR. La tercera CCG mostró vasoespasmo grave en el tronco de la CI, la arteria DA ocluida a nivel proximal y la Cx con lesión moderada a nivel ostial y proximal que impresiona grave por vasoespasmo. Se asistió con balón de contrapulsación intraaórtico (BCIA), asistencia respiratoria mecánica (ARM) e inotrópicos. Se realiza infusión intracoronaria de nitroglicerina, con mejoría del vasoespasmo del TCI y la Cx con posterior ATC en la DA.
Ante la persistencia de inestabilidad hemodinámica se decidió avanzar con cirugía coronaria de emergencia (LIMA-DA y PV-Cx). En el posoperatorio persistió en shock cardiogénico, por lo que se inició asistencia ven-tricular mecánica (AVM) con ECMO V-A como puente al trasplante. A las 48 horas se realizó trasplante cardíaco. En el seguimiento ambulatorio a 8 meses no presentó nuevos eventos cardiovasculares. La anatomía patológica cardíaca reveló DFM de las coronarias con disección en la DA y la Cx, focos isquémicos cicatrizales e infartos en diferentes períodos evolutivos.
Caso 2: Mujer de 30 años. Migrañosa con consumo de ergotamina trisemanal. Consulta por angina en reposo de 10 minutos de duración con ECG sin cambios isquémicos, troponina ultrasensible 186 ng/L. Ecocardiograma con hipocinesia a nivel apical. A los pocos minutos presenta angor y SST V2-V5; se realizó una CCG, que evidenció DCE de los tercios proximal y medio de la DA comprometiendo toda la extensión de la arteria, por lo que se realizó una ATC con stent. A las dos horas repitió angor, SST lateral y shock cardio-génico. La CCG mostró disección del TCI distal y de la Cx en el tercio medio; se realizó ATC en ambas arterias con stent y se asistió con BCIA, ARM e inotrópicos, con respuesta favorable. En el seguimiento ambulatorio a 8 meses no presentó nuevos eventos cardiovasculares. Se realizó una angiotomografía, sin evidencia de enfermedad en otros lechos vasculares.
Discusión: La etiología de la DCE es multifactorial, se asocia con enfermedades del tejido conectivo, condiciones inflamatorias sistémicas, período periparto y DFM..(2, 4, 5)
La angiografía es indispensable para el diagnóstico y en pacientes con hematomas intramurales (1) (Figura 1) se requieren estudios más sensibles como el ultrasonido intravascular (IVUS) o la tomografía de coherencia óptica (OCT) (1, 4) para diferenciarlo de una lesión arteriosclerótica. Debido a la fuerte asociación con la DFM, debería realizarse rutinariamente su búsqueda al diagnosticarse un caso de DCE, siendo la angiografía invasiva más sensible que la angiotomografía. (6)
No hay consenso sobre el tratamiento de la DCE. El manejo depende del estado hemodinámico del paciente, de su sintomatología y del grado de disección. En un paciente asintomático se sugiere un abordaje conservador, basado en datos observacionales que demuestran que en la mayoría de los casos las DCE tienden a la curación espontánea y debido a que la revascularización se asocia con tasas altas de fracaso. Incluye los fármacos utilizados en el tratamiento del SCA; su rol en la DCE es desconocido y discutido por la falta de estudios aleatorizados en esta patología. (1-3, 6) La aspirina y los betabloqueantes son los más ampliamente aceptados, mientras que la anticoagulación, los inhibidores de la enzima convertidora de la angiotensina y las estatinas son más controversiales. La revascularización está recomendada si el paciente está hemodinámicamente inestable, si la disección genera isquemia, arritmia ventricular o si compromete el TCI. Los trombolíticos deben evitarse porque pueden empeorar la disección. La ATC debe realizarse en los casos en que la anatomía sea adecuada; de lo contrario, debería considerarse la CRM. Además, la CRM es para casos con disección del TCI, disecciones extensas con compromiso proximal de arterias principales y con ATC fallida. (1-3, 6)
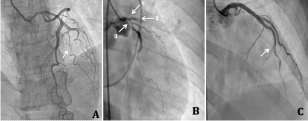
Fig. 1. A y B. Angiografía del TCI, DA y Cx del Caso 1. A. Primer cateterismo coronario: se visualiza ramo Dg con lesión grave proxi-mal de la subdivisión inferior (flecha). Los vasos arteriales presentan tortuosidades y estrechamiento liso distal, características angiográfi-cas de la DFM. B. Tercer cateterismo coronario: vasoespasmo grave en el TCI (flecha 1), DA ocluida a nivel proximal (flecha 2) y Cx con lesión moderada a nivel ostial y proximal que impresiona grave por vasoespasmo (flecha 3). C. Angiografía de la arteria DA del Caso 2. Se observa la línea de disección en el tercio medio de la arteria, con arteria angiográficamente normal proximal.

Fig. 2. Histología de las arterias coronarias con tinción con hema-toxilina y eosina. A. Arteria CD con aspecto arrosariado. B. Arteria DA con predominio de fibrodisplasia intimal. C. Arteria DA con área de predominio de displasia fibromuscular. D. Con tinción tricómico de Masson, se observa parte de la disección de la muscular.
La sobrevida a largo plazo es mayor del 90% y el porcentaje de recurrencia es variable (10-50%), según el tiempo de seguimiento. (1, 3, 5, 6)
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
María Paz Domínguez Pace, Álvaro Etchepare,
Adriana Acosta, Mirta Diez,
Mariano BenzadónMTSAC, Marcelo TriviMTSAC
Instituto Cardiovascular de Buenos Aires (ICBA) mariapazdpace@gmail.com
BIBLIOGRAFÍA
1. Saw J. Spontaneous coronary artery dissection. Can J Cardiol 2013;29:1027-33. http://doi.org/bws7
2. Vrints CJ. Spontaneous coronary artery dissection. Heart 2010;96:801-8. http://doi.org/dth3gg
3. Pate GE, Lowe R, Buller CE. Fibromuscular dysplasia of the coro-nary and renal arteries? Catheter Cardiovasc Interv 2005;64:138-45. http://doi.org/d27cjj
4. Alfonso F, Paulo M, Lennie V, Dutary J, Bernardo E, Jiménez-Quevedo P, et al. Spontaneous coronary artery dissection: long-term follow-up of a large series of patients prospectively managed with a "conservative" therapeutic strategy. JACC Cardiovasc Interv 2012;5:1062-70. http://doi.org/bws8
5. Saw J, Aymong E, Sedlak T, Buller CE, Starovoytov A, Ricci D, et al. Spontaneous coronary artery dissection: association with predis-posing arteriopathies and precipitating stressors and cardiovascular outcomes. Circ Cardiovasc Interv 2014;7:645-55. http://doi.org/bws9
6. Michelis KC, Olin J W, Kadian-Dodov D, d'Escamard V, Kovacic JC. Coronary artery manifestations of fibromuscular dysplasia. J Am Coll Cardiol 2014;64:1033-46. http://doi.org/f2twk5
Rev Argent Gardiol 2016;84:604-606. http://dx.doi.org/10.7775/rac.es.v84. i6.8167
Seudoaneurisma del ápex cardíaco después de TAVR
Descripción del caso: Paciente de sexo femenino, de 81 años, aquejada de disnea progresiva hasta pequeños esfuerzos durante el último año. Antecedentes: dislipidemia, hipertensión, neumonía, padre fallecido por enfermedad coronaria. En el examen físico se encontró hipertensión sistólica (148/78 mm Hg), taquipnea leve (23/min), soplo protosistólico III/IV en foco aórtico, murmullo vesicular disminuido en las bases. El ecocardiograma informó fracción de eyección del ventrículo izquierdo (FEVI) del 60%, hipertrofia concéntrica leve (106 g/m2), esclerosis valvular aórtica leve y compromiso importante de la apertura de todas sus cúspides, área valvular de 0,48 cm2, velocidad máxima 4,25 m/seg, gradiente de presión 72,3 mm Hg, dilatación moderada de la aurícula izquierda (48 ml/m2), aurícula derecha dilatada (31 ml/m2), disfunción diastólica de grado II, insuficiencia mitral de grado B e hipertensión pulmonar leve (47 mm Hg). En la coronariografía no había obstrucciones significativas.
Bajo el diagnóstico de estenosis aórtica grave, se realizó cambio valvular por vía percutánea ilio-femoral (transcatheter aortic valve replacement
-TAVR-), implantándose una válvula CoreValve de 26 mm. Continuó con manejo ambulatorio luego de permanecer cinco días hospitalizada. Siete meses después consultó por disnea. La radiografía de tórax evidenció múltiples consolidaciones en el parénquima pulmonar. Se inició manejo antibiótico por impresión diagnóstica de neumonía. El ecocardiograma de control reveló imagen sugestiva de seudoaneurisma en el ápex cardíaco. La resonancia con contraste reportó lesión quística multiseptada, de contornos lobulados de 70 × 40 × 53 mm (Figuras 1 a 3). El diagnóstico final fue seudoquiste ventricular y se decidió manejo expectante.
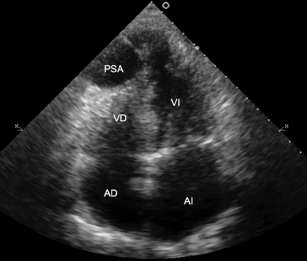
Fig. 1. Ecocardiograma bidimensional, que muestra el ligero efecto de masa sobre la punta ventricular derecha. AD: Aurícula derecha. AI: Aurícula izquierda. VD: Ventrículo derecho. VI: Ventrículo izquierdo. PSA: Seudoaneurisma.
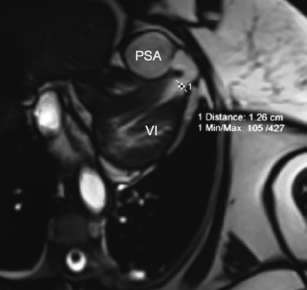
Fig. 2. Corte axial por resonancia magnética nuclear. VI: Ventrículo izquierdo. PSA: Seudoaneurisma.
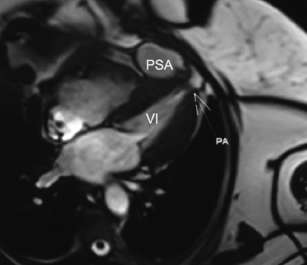
Fig. 3. Corte axial por resonancia magnética nuclear enfatizando el cuello del defecto. VI: Ventrículo izquierdo. PSA: Seudoaneurisma.
Discusión: El reemplazo valvular aórtico por vía percutánea es una alternativa valiosa en los pacientes que por sus comorbilidades no pueden ser llevados a procedimientos abiertos. Normalmente, el abordaje se realiza por vía iliofemoral, pero en los pacientes que adicionalmente tienen vasos tortuosos, el abordaje transapical es una opción válida. En la mayoría de los centros se protocoliza el acceso apical cuando el iliofemoral es inadecuado. (1)
El seudoaneurisma del ápex cardíaco es una complicación del TAVR por vía transapical. (2) Se cree que los factores condicionantes para esta vía comprenden edad avanzada, múltiples comorbilidades, miocardio frágil, sangrado, infarto miocárdico y debilidad localizada del tejido. Otras secuelas del acceso transapical son sangrado con y sin taponamiento, enfermedad cerebrovascular, insuficiencias mitral y aórtica y hematoma septal. (1)
Los casos reportados de seudoaneurisma apical secundarios a TAVR por vía transapical han sido exiguos. Paralelamente, no existe reporte en la literatura de seudoaneurisma en el ápex cardíaco secundario a un abordaje iliofemoral. Este sería, entonces, el primer caso reportado. Schamroth (3) sugiere que el mecanismo causal para los aneurismas de la aorta después de un TAVR es un desgarro lineal en el momento de la implantación, que luego, con el tiempo, se convierte en aneurisma. En nuestro caso, probablemente el mecanismo causal implicado sería un desgarro análogo del ápex ventricular por una de las guías empleadas durante el procedimiento.
Algunos autores consideran necesaria su reparación quirúrgica; (2, 4, 5) no obstante, si un paciente ha sido sometido a TAVR y no a cirugía abierta es, precisamente, porque el riesgo operativo es alto debido a las múltiples comorbilidades, lo que au-
menta significativamente el riesgo de reparación quirúrgica. (5) En esta situación, el cierre percutá-neo debe ser tenido en cuenta como una posibilidad de tratamiento.
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
Ricardo Poveda Jaramillo1, Gustavo Restrepo Molina2, Jaime López Torres3, Karen Estupiñan Perilla4
1 Fellow Anestesia Cardiovascular, Universidad CES,
Medellín, Colombia
2 Cardiólogo, Ecocardiografista, Docente Universidad CES,
Medellín, Colombia
3 Cardiólogo, Ecocardiografista
4 Cardióloga, Ecocardiografista ricardopovedamd@yahoo.com
BIBLIOGRAFÍA
1. Ramlawi B, Abu Saleh WK, Al Jabbari O, Barker CM, Kleiman NS, Reardon MJ. Minimally invasive repair of left ventricular pseudoan-eurysm after transapical transcatheter aortic valve replacement. Tex Heart Inst J 2016;43:75-7. http://doi.org/bwtc
2. Feldman T, Pearson P, Smart SS. Percutaneous closure of post TAVR LV apical pseudoaneurysm. Catheter Cardiovasc Interv 2015 Aug 1. Epub ahead of print
3. Schamroth C. Late false aneurysm formation after transfemoral TAVR. JACC Cardiovasc Interv 2016;9:100-1. http://doi.org/bwtd
4. Manning M W, Diaz L Jr, Weigner MB, Donnelly CL, Greenberg MR. Post Transapical Aortic Valve Replacement (TAVR) pseudoaneurysm. West J Emerg Med 2014;15:895-6. http://doi.org/bwtf
5. Merchan S, Li CH, Martínez FJ, Kliger C, Jelnin V, Perk G, et al. Novel percutaneous apical exclusion of a left ventricular pseudoan-eurysm after complicated transapical transcatheter aortic valve re-placement. JACC Cardiovasc Interv 2015;8:e227-8. http://doi.org/bwtg
Rev Argent Gardiol 2016;84:606-607. http://dx.doi.org/10.7775/rac.es.v84. i6.10126
Vacunación antigripal y antineumocócica en pacientes con enfermedad cardiovascular: proyecto piloto
Las infecciones por el virus de la influenza y por Strep-tococcus pneumoniae se asocian con un riesgo elevado de morbimortalidad en pacientes con enfermedades cardiovasculares. Las agencias gubernamentales internacionales y locales recomiendan el uso de vacunas; sin embargo, existe una subutilización en nuestro medio. (1) Diversas barreras pueden estar relacionadas con este comportamiento, desde la aceptación por parte del médico, los mitos y creencias por parte de los pacientes, así como las limitaciones económicas o de la provisión por el sistema de cobertura médica. Planteamos que la consulta a un especialista, o la internación en unidad coronaria (UCO), es una importante oportunidad para mejorar la tasa de adherencia a la indicación de las vacunas. Este trabajo tuvo por objetivo evaluar la tasa de inmunización de los pacientes luego de la indicación sistemática de las vacunas antigripal y antineumocócica en la UCO o en consultorio y, además, describir las eventuales barreras para la implementación de la vacunación.
Realizamos un estudio prospectivo durante 30 días consecutivos en temporada epidémica (15 mayo-15 junio) en un centro de Buenos Aires. Previa firma de consentimiento informado, se registraron los datos filiatorios, información acerca de vacunación previa y motivo de indicación de inmunización. En un lapso de 1 a 2 meses posteriores a la inmunización se realizaron llamados telefónicos y se recabaron datos acerca de vacunación efectiva, tipo de vacuna, efectos adversos y motivos de no inmunización (Figura 1). Se realizó un análisis estadístico convencional, se comparó la tasa de inmunización al egreso de UCO versus consultorios mediante la prueba de chi cuadrado. En base a datos del Ministerio de Salud de la Nación de 2012, la tasa de vacunación antigripal en pacientes de entre 2 y 64 años con factores de riesgo en la ciudad de Buenos Aires fue del 57%. (1) Asumiendo un error aceptado del 20%, un nivel de confianza del 95% y un 10% de pérdidas, se debían reclutar aproximadamente 80 pacientes, por lo que se estimó un mes de reclutamiento. Se utilizó el programa EpiInfo 3.5.3 y se consideró significativo un valor de p < 0,05.
Se incluyeron 80 pacientes, de los cuales el 68% eran varones, con una mediana de edad de 65 años (RIC 59-72 años), el 19% pertenecían a medicina prepaga y el resto a obras sociales. En 25 pacientes (31%), la indicación de inmunización se realizó al egreso de la internación en UCO o sala de cardiología; en el resto fue desde el consultorio externo. Las indicaciones más frecuentes fueron síndromes coronarios agudos (59%), edad > 65 años (50%), tabaquismo activo (16%), diabetes (12%) e insuficiencia cardíaca (10%), superponiéndose varias de ellas en algunos casos. El 38% recibían vacunación antigripal anual. Al 99% de los pacientes se les indicó la vacuna antigripal, pero a los 30 días solo el 73% se había inmunizado efectivamente. El principal motivo referido por los pacientes para no inmunización fue "decisión personal". En tres pacientes se describieron cuadros seudogripales luego de la inmunización. Con respecto a la vacuna antineumocócica, 15 pacientes (12%) se habían inmunizado previamente. Cuando se realizó el llamado telefónico, se evidenció que solo el 46% (32 pacientes) habían recibido la vacuna. Los tres motivos por los cuales no se efectuó la inmunización fueron: decisión personal (59%), falta de provisión por cobertura médica (24%) y el precio elevado (18%). No se registraron eventos adversos tras la inmunización. La indicación de la vacuna desde la UCO se asoció con una tendencia a mayor tasa de vacunación (52% vs. 42%), aunque la diferencia no fue significativa por bajo poder de la muestra (p = 0,2).
La principal causa de muerte en la Argentina es de origen cardiovascular (2) y presenta un patrón estacional, con picos de mortalidad cardiovascular en los meses invernales. Un estudio inglés ha demostrado una correlación significativa entre las consultas ambulatorias estacionales por cuadros gripales y la mortalidad por infarto agudo de miocardio, (3) evidenciando la correlación entre infección, inflamación sistémica y accidente de placa. Actualmente existen estudios ecológicos, caso-control, y estudios aleatorizados que evidencian la eficacia de la vacunación antigripal para reducir no solo las hospitalizaciones por neumonía, sino también las hospitalizaciones de causa cardiovascular y la mortalidad. (4) Con respecto a la vacunación an-tineumocócica, también se observa dicha asociación. Un estudio reciente, aleatorizado con más de 80.000 mayores de 65 años en Holanda, (5) demostró que la utilización de una vacuna antineumocócica más moderna, conjugada, presentó un 75% de eficacia para prevenir el primer episodio de enfermedad neumocócica invasiva. En un estudio de cohorte prospectivo, el efecto de la doble vacunación (antigripal y antineumocócica) en más de 36.000 personas mayores de 65 años se asoció con una reducción significativa de neumonías, accidente cerebrovascular, infartos, insuficiencia cardíaca, hospitalizaciones y mortalidad total. (6) Dentro de las barreras descriptas para la inmunización, en este estudio se superó la barrera del conocimiento médico, ya que las vacunas fueron indicadas sistemáticamente. Hallamos que el principal motivo para no inmunizarse fue la decisión personal. Creemos que esto se debe principalmente a mitos y creencias populares acerca de la falta de eficacia y riesgo de infecciones provocadas por las vacunas, pero también podría deberse a la falta de adherencia a las medidas indicadas por el médico, tal cual sucede con otras terapias farmacológicas. En este sentido, estudios poblacionales a gran escala sugieren que la adherencia a estrategias terapéuticas en cuadros con elevada mortalidad como los síndromes coronarios agudos es casi completa al alta de la UCO pero decae drásticamente en el seguimiento, tanto en países industrializados como en vías de desarrollo y en centros urbanos y rurales. La tendencia a una mayor tasa de inmunización al egreso de la UCO en comparación con el consultorio es una potencial oportunidad de intervención para mejorar la adherencia, que debería ser demostrada en estudios de mayor escala.
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
BIBLIOGRAFÍA
1. Ministerio de Salud de la Nación 2012 Recomendaciones de vacunación ProNaCei. www.msal.gov.ar
2. Sosa Liprandi MI, Harwicz P, Sosa Liprandi. Causas de muerte en la mujer y su tendencia en los últimos 23 años en la Argentina. Rev Argent Cardiol 2006;74:297-303.
3. Warren-Gash C, Bhaskaran K, Hayward A, Leung GM, Lo S V, Wong CM, et al. Circulating influenza virus, climatic factors and acute myocardial infarction: a time series study in England and Wales and Hong Kong. J Infect Dis 2011;203:1710-8. http://doi.org/ds5rkm
4. Udell JA, Zawi R, Bhatt DL. Association between influenza vac-cination and cardiovascular outcomes in high-risk patients. A meta-analysis. JAMA 2013;310:1711-20. http://doi.org/pzg
5. Bonten MJM, Huijts SM, Bolkenbaas M. Polysaccharide conjugate vaccine against pneumococcal pneumonia in adults. N Engl J Med 2015;372:1114-25. http://doi.org/bws5
6. Hung IFN, Leung AYM, Chu DWS. Prevention of acute myocardial infarction and stroke among elderly persons by dual pneumococcal and influenza vaccination: A Prospective Cohort Study Ivan. Clin Infect Dis 2010;51:1007-16. http://doi.org/bf3q9q
Rev Argent Gardiol 2016;84:607-609. http://dx.doi.org/10.7775/rac.es.v84. i6.5853
Ricardo VillarrealMTSAC, Ezequiel J. Zaidel,
Horacio G. Cestari, Eduardo F. MeleMTSAC,
María I. Sosa LiprandiMTSAC,
Álvaro Sosa LiprandiMTSAC
Servicio de Cardiología. Sanatorio Güemes Acuña de Figueroa 1240 - CABA - Argentina.














